Autores
Lima Silva, R. (UNIVERSIDADE DO ESTADO DO AMAZONAS) ; Pereira, D.S. (UNIVERSIDADE DO ESTADO DO AMAZONAS)
Resumo
O presente trabalho utilizou o processo de extração e de identificação da cafeína com o objetivo de contextualizar o tema pH trabalhado com alunos do 2° ano do ensino médio por ser a preparação e consumo de bebidas a partir do café uma atividade cotidiana para eles. Durante o processo de extração os alunos acompanharam as mudanças de pH do meio reacional utilizando fitas indicadoras. A cafeína obtida foi identificada pela a reação de Murexida. Através da aplicação de um questionário, foi possível verificar que a atividade experimental, além de aumentar o interesse dos alunos pelo tema, possibilitou que a maioria compreendesse o conceito de pH, além de detectar a necessidade de reforçar outros conceitos químicos como solubilidade e substâncias iônicas e moleculares.
Palavras chaves
Cafeína; ensino; extração
Introdução
Desconhecida por muitos e ainda assim consumida no mundo inteiro, a cafeína é um composto proveniente de fontes naturais, sendo as fontes mais conhecidas as sementes de cacau, café e de guaraná. A cafeína é uma substância presente em muitos produtos comercializados, apresentando teores variados em diferentes marcas de bebidas estimulantes ou energéticas, podendo causar problemas que vão desde uma dor estomacal até um ataque cardíaco, mas também podem aumentar a capacidade mental e de concentração (JESUS, et. al. 2010). Por ser a preparação e consumo de bebidas a partir do café uma atividade do dia-a-dia para a maioria das pessoas, e considerando os saberes adquiridos pelos elas através de sua prática cultural e da vivência de fato de seu cotidiano, resolveu-se utilizar uma atividade experimental que consiste na extração e identificação da cafeína presente em bebidas não alcoólicas estimulantes como uma estratégia de ensino para o estudo de pH na disciplina de química no 2º ano do ensino médio. Dessa forma quebra-se a relação teoria-teoria que vem causado nos alunos o desinteresse em prender química e se adota uma relação teoria-prática onde se valoriza os conhecimentos de vida do aluno.
Material e métodos
Para a extração e identificação da cafeína foi seguido o procedimento proposta na Apostila de Aula Prática de Farmacognosia UEL, conforme descrito a seguir. Foi aquecida até à fervura a mistura de 1,0 g do pó de café pulverizado, 5 ml de ácido sulfúrico diluído (10% v/v) e 5 ml de água. A mistura foi filtrada em papel de filtro previamente umedecido com uma mistura água-ácido sulfúrico e o filtrado foi alcalizado em cerca de 5 ml de hidróxido de amônia 6 M (verificando o ponto de neutralização com papel indicador). Em seguida o filtrado alcalizado foi transferido para um funil de separação e acrescentou-se 5 ml de clorofórmio, agitando-se manualmente. A fase clorofórmica depois de decantada foi filtrada para uma capsula de porcelana com cabo (a filtração foi feita por papel de filtro umedecido com o mesmo solvente puro). A cápsula de porcelana foi aquecida até completa evaporação do filtrado. Para identificação da cafeína pela reação de Murexida, ao resíduo frio na cápsula de porcelana acrescentou-se 3 gotas de ácido clorídrico 6M e 2 gotas de peróxido de hidrogênio concentrado. A mistura foi evaporada até a secura. Neste momento formou-se um resíduo vermelho e seco, no qual se adicionou algumas gotas de hidróxido de amônia 6M que adquiriu uma cor violeta. Durante todo o processo os alunos tiveram contato com a preparação e o uso de soluções além de outros conhecimentos de química. Com a finalidade de avaliar a aprendizagem dos alunos sobre os conhecimentos químicos envolvidos no experimento, aplicou-se um questionário com perguntas fechadas.
Resultado e discussão
Durante a parte experimental foram notórios o interesse e a participação dos alunos. Para avaliar a aprendizagem foi solicitado aos alunos que estabelecessem a relação entre o valor do pH medido e a acidez ou alcalinidade do meio, na mistura aquecida e após a adição de hidróxido de amônia. Percebemos que 100 % dos alunos souberam relacionar o pH e o meio da mistura, porém somente 65,6 % dos alunos acertaram a relação entre o pH e meio após a adição de hidróxido de amônia. Sugerindo que o conceito de equilíbrio químico precisa ser reforçado.
Uma segunda pergunta feita aos alunos se referia a forma da cafeína (iônica ou molecular) em meio ácido, onde somente 31,3% compreenderam que está na forma iônica. A terceira pergunta feita aos alunos se referia a onde ocorre maior solubilidade da cafeína molecular, se em meio polar ou apolar. O resultado mostra que 49,9 % responderam que era em meio polar. Isso indica que o conceito de solubilidade ‘semelhante dissolve semelhante” precisa ser reforçado.
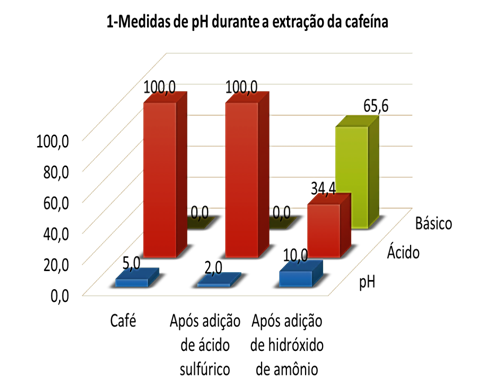
Durante o experimento foi medido o pH do meio reacional utilizando fitas de pH. O gráfico 1 mostra que a maioria dos alunos conhecem o conceito de pH ácido e pH básico.
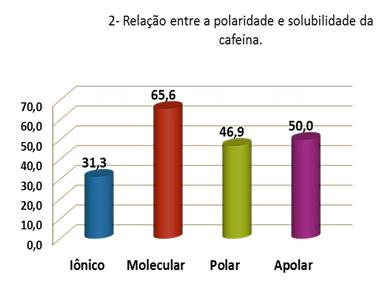
O gráfico 2 mostra a seguinte pergunta: Dependendo do seu pH a cafeína pode estar na forma iônica ou molecular após a adição do ácido sulfúrico. Também foi perguntado: Quando se adicionou o clorofórmio ao filtrado do café, em qual fase a cafeína estava.
Conclusões
A atividade experimental desenvolvida na sala de aula contribuiu para que o aluno compreendesse melhor o tema pH e com o aumento do interesse dos alunos pelos assuntos de química, além de possibilitar a avaliação de outras aprendizagens como a solubilidade de substâncias iônicas e moleculares, e equilíbrio químico. O experimento permitiu ainda que o aluno buscasse mais informações sobre a cafeína e sua influência sobre a saúde.
Agradecimentos
A Universidade do Estado do Amazonas (UEA) e ao professor Djalma da Silva Pereira.
Referências
Apostila de Aula Prática de Farmacognosia UEL. Identificação de metilxantinas. <http://sbfgnosia.org.br/Ensino/drogas_com_alcaloides_puricos.html> 25/09/15.
JESUS, C.C et al. Agroindústria, Qualidade de Vidas e Biomas Brasileiros: CONGRESSO BRASILEIRO DE QUIMICA,Cuiabá, 2010. Disponível em ˂http // www.abq.org.br/cbq/trabalhos/14/14-44-8053.htm ˃ . Acesso em 27 de Dez.2015. (BELKIN et al ., 1982, p76)

