Autores
Alves de Oliveira, M.D. (IFPI) ; Batista da Costa, F. (IFPI) ; da Silva Sousa, G.F. (IFPI)
Resumo
Aulas experimentais podem servir para estimular a curiosidade do aluno e desmistificar as idéias oriundas do senso comum, como as concepções alternativas. As atividades devem ser relacionadas a objetivos que desenvolvam habilidades importantes dos alunos, como aprender a partir da observação e da experimentação, para isso realizou-se uma pesquisa de campo com experimentação voltada às percepções do conhecimento teórico dos alunos,participaram quatorze estudantes do 3° ano do Ensino Médio da rede estadual de Teresina-PI, verificou a capacidade dos alunos em utilizar conceitos de átomo, íons e moléculas para explicar fenômenos observados em um experimento sobre condutividade elétrica. Os alunos mostraram que têm muita dificuldade em explicar fenômenos naturais usando a linguagem científica.
Palavras chaves
Ensino de química; experimentação; concepções alternativas
Introdução
A maioria dos alunos atravessa o ensino médio sem formar um conhecimento coerente sobre os conceitos de átomo, íons e molécula. Formam-se fragmentos de conhecimento que, em geral, estão mais próximos do senso comum do que do conhecimento científico. Além dos problemas gerais que perpassam a educação, no caso da Química, há o estereótipo da disciplina que se coloca como uma barreira antes mesmo da primeira aula, gerando medo de que a disciplina seja impossível de aprender. É necessário também que sejam consideradas as concepções alternativas dos alunos a respeito do tema a ser trabalhado, pois estas concepções podem criar obstáculos sérios para a compreensão de conceitos e a utilização deles para expressar fenômenos por meio da linguagem científica. Estas concepções são idéias construídas no decorrer da vivência das pessoas e, por isso mesmo, ficam enraizadas no modo de interpretar os fenômenos naturais. A sondagem e o tratamento das concepções alternativas tem sido objeto de estudo em diversos países e estas pesquisas mostraram que existe um certo padrão nestas idéias, independente do país onde foram observadas (MORTIMER, 1995).As atividades das aulas experimentais devem ser relacionadas a objetivos que desenvolvam habilidades importantes dos alunos, como aprender a partir da observação e da experimentação, onde o ensino alcançaria sua função de auxiliar a compreensão do estudante sobre a relação entre ciência e natureza. Logo, a experimentação não deve ter um fim em si mesmo (aprender a fazer o experimento) ou agir como legitimadora de proposições teóricas. É desejável, inclusive, que haja uma dose de surpresa, de resultados inesperados para estimular as observações e as discussões, ou seja, é necessário que seja um “experimento exigente (GIORDAN, 1999).
Material e métodos
Utilizou-se um LED de (6 V) conectado a pilhas e fios de cobre, que funcionaram como eletrodos. Em caso afirmativo de condução de corrente elétrica, a lâmpada acenderia, como mostra a figura 01.No primeiro teste confrontou-se a condutividade da água da torneira com a água destilada. Questionamentos como por que a lâmpada acendeu com a água da torneira e não acendeu com a água destilada foram levantados, como mostra a figura 02.No segunda teste confrontou- se o sal sólido e o açúcar sólido. Pediu-se a observação do LED e em seguida a resolução do questionamento proposto.No terceiro teste confrontou-se soluções de sal e água e soluções de açúcar e água.Pediu-se que relacionassem o fato anterior com o do momento e perguntou-se por que o LED acendeu neste caso e no anterior não.
Resultado e discussão
No experimento, as percepções dos estudantes sobre os fenômenos se mostraram
dominada pela cultura do senso comum.A diferença de condutividade entre a água
da torneira e a água destilada não foi explicada satisfatoriamente por nenhum
dos alunos, eles apenas citaram presença de substâncias – sais, minerais ou
nutrientes (não souberam especificar quais seriam) na água da torneira dando a
estes a função de condução de eletricidade. Em nenhuma explicação houve menção a
íons, elétrons, átomos e moléculas, deixando claro que eles não sabiam fazer a
relação do fenômeno observado com os entes químicos aos quais são atribuídas as
propriedades da matéria, neste caso específico, a condutividade elétrica.(BOFF
et, al. 1996) elaborou uma proposta pedagógica onde insere e utiliza os
conceitos de átomo, moléculas, e elétrons através de atividades que procuram
demonstrar a presença de cargas elétricas na matéria.Com relação às substâncias
sólidas testadas, as explicações para a não condutividade giraram em torno do
estado solido da substância, fazendo uso das palavras de um aluno “o sal está em
estado solido, ou seja, neutro, então não vai conduzir eletricidade para acender
o LED.”. Explicações como estas desconsideram o fato de que a grande maioria dos
condutores de eletricidade são sólidos, e sua condutividade se explica pela
movimentação constantes de seus íons para preencherem o espaço na matéria.Os
alunos expressaram a ideia de que a água apresenta “nutriente” que levariam a
condução de eletricidade, porém o que mais chama a atenção é que os alunos não
sabem explicar em termos científicos quais seriam estes nutrientes presentes ou
não em cada substancia e qual a característica que eles dariam às substâncias
para torná-las condutores de eletricidade.

Em caso afirmativo de condução de corrente elétrica pela solução apresentada, a lâmpada acenderia.
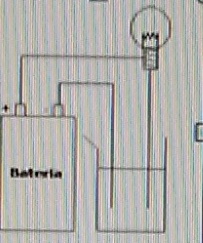
Em caso negativo da não condução de corrente elétrica nas soluções testadas, a lâmpada não acenderia.
Conclusões
Acredita-se que houve um aproveitamento significativo na construção do conhecimento dos estudantes tanto pelo caráter lúdico do experimento quanto pela simplicidade dos materiais utilizados.Constituindo um fator de estímulo à curiosidade,pois demonstram interesse pelos materiais usados na prática.O experimento se mostrou uma ferramenta eficiente para se introduzir ou recapitular os conceitos de íons,átomos e moléculas,pois a partir da experimentação os estudantes levantaram questionamentos fazendo a relação da teoria com a prática envolvida nos testes e destes com o cotidiano.
Agradecimentos
IFPI
Referências
GIORDAN, M.; O papel da experimentação no ensino de ciências. Química Nova na Escola. Nº 10, novembro, 1999.
MORTIMER, E.F.; Concepções atomísticas dos estudantes. Revista Química Nova na escola, v. 01, p. 23-26, maio, 1995.
BOFF, E. T. O.; FRISON, M. D.; Explorando a existência de cargas elétricas. Revista Química Nova na Escola, n. 03, p. 11-14, maio, 1996.

