Realizado em Tereseina/PI, de 11 a 13 de Setembro de 2019.
ISBN 978-85-85905-26-2
TÍTULO: INFLUÊNCIA DO SnCl2 COMO ADITIVO EM SISTEMAS CATALÍTICOS PARA METÁTESE DO ÁLCOOL CINAMÍLICO
AUTORES: Vieira, V.B. (UESPI) ; França, A.A.C. (UFPI) ; Almeida, F.S. (UESPI) ; Braga, S.D. (UFPI) ; Silva, T.T. (UESPI) ; Silva, T.T. (UESPI) ; Ramos, M.A.B. (UESPI) ; Santos, I.B.P. (UESPI) ; Barros, M.S.J. (UESPI) ; Sá, J.L.S. (UESPI)
RESUMO: Utilizou-se o SnCl2 como aditivo na autometátese do álcool
cinamílico (AC) na presença do catalisador de Grubbs de primeira geração
para sintetizar a molécula 1,5-difenil-2-penteno. Na proporção 1:1 mol
(Ru:AC), sem adição de SnCl2, 75% do produto C17H18 foi obtido.
Com adição de SnCl2, houve uma diminuição do produto formado.
Isto pode ter ocorrido devido ao efeito estérico de SnCl2. Na
proporção de 1:10 mol sem adição de SnCl2, não houve formação de
produto. Com adição de SnCl2, obteve-se um aumento esperado, um
máximo de 33,89% de C17H18, no qual SnCl2 influenciou o aumento
da formação do produto com efeito eletrônico, melhorando a atração Ru pelo
duplo olefínicas.
PALAVRAS CHAVES: Autometátese; Álcool Cinamílico; Cloreto de estanho
INTRODUÇÃO: Na última década, a metátese de olefinas tornou-se um importante método
sintético para obtenção de novas moléculas insaturadas a partir de dois
alcenos diferentes, onde ocorre um rearranjo do esqueleto carbônico, na qual
de ligações duplas carbono-carbono são redistribuidas (FREDERICO et al,
2005).
Desde seu descobrimento e até o final da década de 80, a aplicação das
reações de metátese de olefinas era reduzida devido à limitação quanto à
sensibilidade dos catalisadores utilizados (BAIBICH e GREGÓRIO, 1993). O
grupo de Grubbs desenvolveu sistemas catalíticos a base de Ru. Os
catalisadores de Grubbs são complexos Ru- alquilidenos que apresentam
atividade em reações de metátese de olefinas (NGUYEN et al, 1993),
mostrando-se ser bem mais resistentes a interferentes orgânicos permitindo
que os compostos de rutênio encontrem vasta aplicação como catalisadores
(FRENZEL e NUYKEN, 2002; DERAEDT et al, 2013).
A literatura relata que a adição de sais, tal como SnCl2 é uma
estratégia observada para o aumento da eficiência do catalisador de Grubbs
em determinadas reações(ROUBLES-DUTENHEFNER et al, 2000). Meyer e
colaboradores (2006), realizaram um estudo sobre a reatividade dos
catalisadores à base de Ru em reações de metátese, quando adicionados
halogenetos de estanho (II). Estes aditivos melhoraram a atividade do
catalisador de primeira geração de Grubbs (G1). Robert Grubbs também
observou maiores rendimentos de metátese por um complexo Ru-Sn, através da
reação de G1 com SnCl2 (MEYER et al, 2006).
O presente estudo propõe realizar reações de autometátese com o álcool
cinamílico, obtendo dímeros desse composto, avaliar a atividade do
catalisador de 1º geração de Grubbs com uma molécula simples, e a influência
do SnCl2 na reação.
MATERIAL E MÉTODOS: Todas as reações aconteceram com saturação com gás N2, por um período de 30
min. A reação iniciou-se com a adição de 10 mL de clorofórmio em um balão,
adicionando em seguida o substrato álcool cinamílico (AC). Após a
solubilização do AC, adicionou-se de 10 mg do catalisador G1 com relações
equivalentes de Ru: substrato, utilizando as proporções de 1:10 mol, 1:1
mol. As sínteses foram realizadas em um sistema de refluxo com óleo
termostatizado com temperatura controlada à 50 ºC pelo tempo de 24 h,
permanecendo em agitação constante. Transcorrido o tempo reacional, a reação
é finalizada com adição de 3 µL de etil vinil éter. Uma alíquota desta
mistura foi retirada para a análise por Cromatografia Gasosa acoplada a
Espectrometria de Massas (CG- EM). Além disso, também realizou- se sínteses
com adição de SnCl2, nas razões de Ru:SnCl2 1:1 mol,
1:2 mol, 1:3 mol, com o mesmo procedimento descrito anteriormente.
RESULTADOS E DISCUSSÃO: Os resultados foram analisados por CG- EM e demonstrados na Figura 1.
Em ambas as proporções, observa-se o 1,5-difenil-pent-2-eno como único
produto da reação. Com Ru:AC de 1:10 mol e 1:1 mol, tendo 5% e 76% de
rendimento. Os diferentes rendimentos indicam um caráter associativo nas
reações; sobre este caráter, ressalta-se que a principal variável de sistema
é a quantidade de substrato.
Realizou-se uma abordagem para a melhoria da atividade do G1, adicionando,
SnCl2. A Figura 2-A representa as reações nas proporções de 1:1 e
1:10 mol (Ru: AC) com a adição do SnCl2 nas proporções de Ru:Sn
1:1 mol, 1:2 mol e 1:3 mol.
Nas reações de 1:1 e 1:10 mol obtiveram o 1,5-difenil-pent-2-eno como
produto. Nas reações do AC com G1, na presença do aditivo nas proporções
Ru:Sn 1:1 mol, Ru:Sn 1:2 mol, e Ru:Sn 1:3 mol, obteve-se 42,8%, 21% e 64,8%
de rendimento respectivamente.
Observa-se que na proporção 1:1 mol Ru:AC foi maior sem o aditivo. Com
ligantes que não exercem impedimento estérico podem, em muitos casos,
minimizar a seletividade dos produtos formados (SÁ et al, 2013).
Também realizou-se as mesmas reações na proporção de Ru:AC de 1:10 mol
(Figura 2-B). Nas reações do AC com G1 na proporção Ru:AC 1:10 mol, com a
adição do SnCl2, tendo Ru:Sn 1:1 mol, Ru:Sn 1:2 mol e Ru:Sn 1:3
mol, cerca de 11,9%, 13,1% e 33,8% de rendimento, respectivamente.
Com os resultados da proporção de 1:10 mol com aditivos de SnCl2
observa-se uma maior formação de produtos, assim como a melhora do
desempenho de G1 na reação, concordando assim, com a literatura (SANFORD et
al.,2001; GRANATO, 2013).
Figura 1.
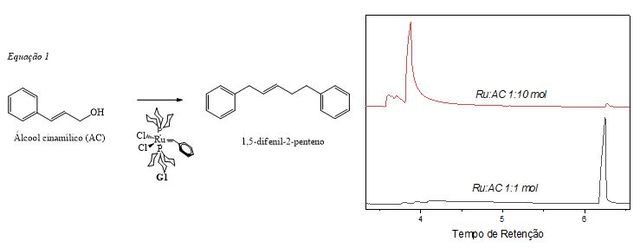
Figura 1. Ilustração da autometátese de AC e
cromatograma referente a síntese razão Ru:AC 1:1,
1:10 mol.
Figura 2
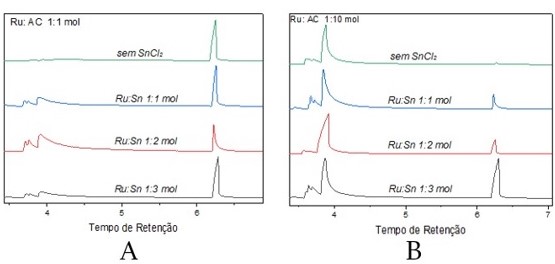
Figura 2. A: Ru:AC 1:1 mol, e SnCl2 nas proporções
1:1, 1:2 e 1:3 mol; B: Ru:AC 1:10 mol, e SnCl2 nas
razoes 1:1, 1:2 e 1:3 mol.
CONCLUSÕES: A metátese do AC foi realizada em diferentes condições reacionais com G1 como
catalisador. Na proporção de 1:1 mol (G1:AC), com aditivo Cloreto de estanho,
não foi considerado favorável para aumentar o rendimento da formação de
produtos.
Na síntese de 1:10 mol G1:AC sem aditivo, não houve boas conversões
em produto, e com a utilização do aditivo de Sn, notou-se aumento do
rendimento em favor das conversões em produtos. Isso mostra que este trabalho
pode contribuir para estudos de catálise ao proporcionar maior entendimento da
ação de catalisadores de Ru com adição de aditivos de Sn.
AGRADECIMENTOS: UESPI e agências de fomento CAPES e FAPEPI (Edital
06/2018 FAPEPI/CAPES) pelas concessões de bolsa de estudo e suportes à
pesquisa.
REFERÊNCIAS BIBLIOGRÁFICA: 1. BAIBICH, I. M.; GREGÓRIO, J. R. Metátese Catalítica de Olefinas. Quimica Nova, n° 2, 1993.
2. DERAEDT, C.; D’HALLUIN, C. M; ASTRUC, D. Metathesis Reactions: Recent Trends and Challenges . European Journal Inorganic Chemistry, 4881–4908, 2013.
3. FREDERICO, D.; BROCKSOM, U.; BROCKSOM, T. J. A reação de metátese de olefinas: reorganização e ciclização de compostos orgânicos. Química Nova, v. 28, 692-702, 2005.
4. FRENZEL, U.; NUYKEN, O. Ruthenium- based metathesis initiators Development and use in ring- opening metathesis polymerization. Journal Polymer Science Part A: Polymer Chemistry, n°40, v. 17, 2002.
5. GRANATO, A. V. Alil-aromáticos como matéria prima renovável para produção de arilbutenoatos via metátese cruzada de olefinas. Dissertação de Mestrado; Departamento de pós Graduação em química UFMG; Belo Horizonte; 2013.
6. JOHNS, A. M.; AHMED, T. S.; JACKSON, B. W.; GRUBBS, R. H.; PEDERSON, R. L. High Trans Kinetic Selectivity in Ruthenium-Based Olefin Cross-Metathesis through Stereoretention. Organic Letters, 772-775, 2016.
7. MATOS, J. M. E; BATISTA, N. C.; CARVALHO, R. M.; SANTANA, S. A. A.; PUZZI, P. N.; SANCHES, M.; LIMA-NETO, B. S. Metátese de olefinas no Brasil: -“BRAZIL IS ROMPING IT!”.Quimica Nova, n°30, 431-435, 2007.
8. MEYER, W. H.; McCONNELL, A. E.; FORMAN, G. S.; DWYER, C. L.; KIRK, M. M.; NGIDI, E. L.; BLIGNAUT, A.; SAKU, D.; SLAWIN, A. M. Z. Tin and iron halogenides as additives in ruthenium-catalyzed olefin metathesis. Inorganica Chimica Acta, nº359, 2910-2917, 2006.
9. ROBLES-DUTENHEFNER, P. A.; MOURA, E. M.; GAMA, G. J.; SIEBALD, H. G. L.; GUSEVSKAYA, E. V. Synthesis of methyl acetate from methanol catalyzed by [(ղ5-C5H5)(phosphine)2RuX] and [(ղ5-C5H5)(phosphine)2Ru(SnX3)] (X=F, Cl, Br): ligand effect.. Journal of Molecular Catalysis A: Chemical, v.164, 39-47, 2000.
10. SÁ, J. L. S.; NASCIMENTO, E. S. P.; FONSECA, L. R.; LIMA-NETO, B. S.; Ring opening metathesis copolymerization of norbornene with norbornadiene from solutions with different mole fractions of the comonomers catalyzed by Ru-amine complexes. Journal of Applied Polymer Science, nº127, 3578, 2013.
11. SANFORD, M. S.; LOVE, J. A.; GRUBBS, R. H. Mechanism and Activity of Ruthenium Olefin Metathesis Catalysts. Journal of the American Chemical Society, nº123, 6543-6554, 2001.
