Realizado em Tereseina/PI, de 11 a 13 de Setembro de 2019.
ISBN 978-85-85905-26-2
TÍTULO: Arachis hypogaea L. como biocatalizador em reações de biorredução de cetonas
AUTORES: Sousa, D.Y.X. (UFCA) ; Peixoto, L.P. (UFCA) ; Oliveira, J.D.F. (UFCA) ; Caldas, F.R.L. (IFCE) ; Pereira, A.K.L.S. (UFCA)
RESUMO: Muitas espécies vegetais são utilizadas em reações biocatalíticas como fonte de enzimas, biocatalisadores. A indústria demonstra grande interesse nas reações de bioreduções de compostos carbonilados, principalmente para a produção de fármacos, cosméticos e agroquímico. O objetivo é estudar o potencial biocatalítico de espécies vegetais, particularmente as da família Fabaceae, por exemplo, o amendoim, Arachis hypogaea L., para a biorredução de cetonas. A metodologia está fundamentada na redução de cetonas aromáticas e alifáticas a partir de enzimas redutases presentes em células íntegras do amendoim, a fim de obtermos seus álcoois correspondentes. Os bioprodutos foram purificados em cromatografia em coluna e identificados através de Cromatografia em Camada Delgada (CCD) e infravermelho (IV)
PALAVRAS CHAVES: Amendoim; Biocatálise; Álcoois
INTRODUÇÃO: As plantas têm sido consideradas sistemas enzimáticos adequados para serem empregados em biocatálise. A maioria das reações catalisadas por plantas são processos redox (redução de aldeídos e cetonas, oxidação de álcoois racêmicos (BIZERRA et al., 2010; FABER, 2011). Na indústria há registros de utilização da biocatálise a fim de obter produtos esteroespecíficos, visando maiores rendimentos em suas sínteses. Avanços recentes na produção de enzima por fermentação permitem a produção de enzimas mais baratas e mais fortes para uso industrial (ALCADE et al., 2006; ILLANES et al., 2012). O amendoim (Arachis hypogaea L.), é uma leguminosa tropical caracterizada por elevada diversidade genética e elevado potencial de produção, que se adaptam às mais diferentes condições ambientais, mas desenvolve-se melhor nos trópicos úmidos e quentes, sendo amplamente distribuído pelas Américas (OLIVEIRA et al, 2014). O objetivo é estudar o potencial biocatalítico de espécies vegetais, particularmente as da família Fabaceae, por exemplo, o amendoim, Arachis hypogaea L., para a biorredução de cetonas. A pesquisa na área de biocatálise vem se tornando maior a cada dia, e seu desenvolvimento é extremamente útil para a fabricação de novos materiais, e no melhoramento de processos, pois a obtenção de produtos enantiosseletivos, regioespecíficos, obtidos de forma limpa podem ser aplicados a diversos campos da ciência bem como no setor industrial (MORAES, 2014). A biocatálise está sendo hoje um dos campos mais promissores dentro das novas tecnologias para síntese de compostos de alto valor agregado.
MATERIAL E MÉTODOS: O biocatalisador utilizado para a realização das biorreduções foi sementes de amendoim (Arachis hypogaea) comprado no mercado do Pirajá no município de Juazeiro do Norte. Os substratos utilizados foram hexan-2-ona (1), alfa-tetralona (2), 4-aminoacetofenona (3) e 2,4-dicloroacetofenona (4). A metodologia a ser empregada foi aquela desenvolvida por Machado (2006). Em erlenmeyeres (250 mL) foram adicionados o biocatalisador (sementes de amendoim, 24 g), os substratos (200 mg) e 150 mL de água destilada, permanecendo em agitação por 72 h em um orbital shaker (150 rpm). 4 A mistura foi filtrada, submetida à extração líquido-líquido com AcOEt (3 x 50 mL), a fase orgânica foi seca com Na2SO4 anidro e concentrada em rota-evaporador, chegando ao extrato bruto da biorredução. Os bioprodutos: hexan-2-ol (1a), alfa-tetralol (2a), 1-(4-aminofenil)etanol (3a), 1-(2,4-diclorofenil)etanol (4a) foram purificados por coluna de gel de sílica. Os produtos das reações foram analisados por CCD [tendo como eluente hexano:acetato (8v:2v) e revelada em solução de vanilina] e IV.
RESULTADOS E DISCUSSÃO: A partir da análise por cromatografia em camada delgada verificou-se um halo em cada bioproduto (1a, 2a e 3a) da mesma altura que o álcool padrão de cada substrato (A) que é produto de síntese química convencional de redução do substrato em questão, bem como ausência de halo da mesma altura que os substratos (1, 2 e 3), nos levando a concluir que a reação de biorredução aconteceu em cada uma das cetonas, produzindo seus respectivos álcoois. No infravermelho do bioproduto (1a) observou-se a presença de banda de hidroxila de álcool próximo de 3.400 cm-1; não se observa banda de carbonila de cetona, próximo de 1.715 cm-1. Sugerindo que a reação de biorredução da hexan-2-ona ao seu álcool hexan-2-ol ocorreu com êxito, pois não há indícios de cetona no bioproduto.
O espectro de infravermelho do bioproduto 2a revelou a presença de banda de hidroxila de álcool próximo de 3.400 cm-1 e ausência de banda de carbonila de cetona conjugada, em torno de 1.680 cm-1. O que nos sugere que a reação de biorredução da α-tetralona ao seu álcool α-tetralol ocorreu com êxito, pois não há indícios de cetona no bioproduto.
O IV do bioproduto 3a revela a presença de banda de hidroxila de álcool próximo de 3.228 cm-1. A banda de carbonila de cetona conjugada, em torno de 1.680 cm-1, não é observada. E ainda observamos as bandas de N-H do grupamento amino (NH2) em 3.396 cm-1 e 3.337 cm-1. A banda em 1.652 cm-1 é referente à ligação C=C de aromático. O que nos sugere que a reação de biorredução da 4-aminoacetofenona ao seu álcool 1-(4-aminofenil)etanol ocorreu com êxito, pois não há indícios de cetona no bioproduto.
Tanto a análise em CCD quanto no IV revelam que não ocorreu a biotransformação do substrato 2,4-dicloroacetofenona (4) em seu álcool correspondente 1-(2,4-diclorofenil)etanol (4a).
Figura 1
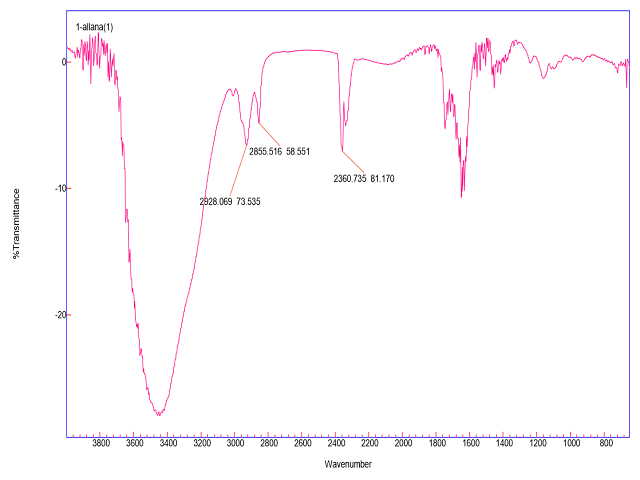
Espectro de IV do bioproduto de biorredução da hexan-2-ona, álcool hexan-2-ol
Figura 2
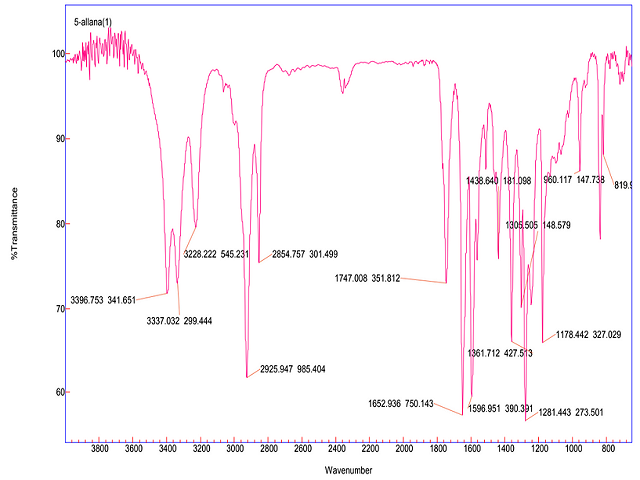
Espectro de IV do bioproduto de biorredução da 4-aminoacetofenona, álcool 1-(4-aminofenil)etanol
CONCLUSÕES: Os resultados obtidos a partir das biotransformações de cetonas utilizando o amendoim como biocatalisador, revelam a presença de enzimas redutases. Percebe-se isso através da análise das CCDs e análise dos espectros de infravermelho dos bioprodutos hexan-2-ol (1a), α-tetralol (2a) e 1-(4-aminofenil)etanol (3a) indicando que a biotransformação ocorreu nos substratos: hexan-2-ona (1), α-tetralona (2), 4-aminoacetofenona (3), e que não houve biorredução do substrato 2,4-dicloroacetofenona (4). Dessa forma, podemos afirmar que o amendoim atua como um promissor biocatalisador em biorreduções.
AGRADECIMENTOS: Ao CNPq, FAPEPI, UFPI, IFCE Campus Juazeiro do Norte e UFCA.
REFERÊNCIAS BIBLIOGRÁFICA: ALCALDE, M.; FERRER, M.; PLOU, F. J.; BALLESTEROS A. Environmental biocatalysis: from remediation with enzymes to novel green processes. Trends in Biotechnology, v.24, n.6, p.281-87, 2006.
BIZERRA, A. M. C.; GONZALO, G., LAVANDERA, I.; GOTOR-FERNÁNDEZ, V.; MATTOS, M. C; OLIVEIRA, M. C. F.; LEMOS, T. L. G.; GOTOR, V. Reduction processes biocatalyzed by Vigna unguiculata. Tetrahedron-Asymmetry, v.21, n.5, p.566-570, 2010.
FABER, K. Biotransformations in Organic Chemistry, 6a edição. Berlin: Editora Springer-Verlag, 2011.
ILLANES, A.; CAUERHFF, A.; WILSON. L.; CASTRO, G. R. Recent trends in biocatalysis engineering. Bioresource Technology, v.115, p.48-57, 2012.
MACHADO, L. L.; SOUZA, J. S. N.; MATTOS, M. C.; SAKATA, S. K.; CORDELL, G. A.; LEMOS, T. L. G. Bioreduction of Aldehydes and Ketones using Manihot species. Phytochemistry, v.67, p.1637-1643, 2006.
MORAES, M. I. Biorredução de aldeídos e cetonas utilizando células íntegras de espéciesvegetais cultivadas no Estado do Piauí. 2014. Dissertação (Mestrado em Química Orgânica) - Universidade Federal do Piauí, Edições UFPI, Teresina, Brasil, 2014.
OLIVEIRA, A. E. S.; SIMEAO, M.; MOUSINHO, F. E. P.; GOMES, R. L. F. Desenvolvimento do feijão-fava (phaseulus lunatus l.) sob déficit hídrico cultivado em ambiente protegido holos, vol. 1, 2014, pp. 143-151 Instituto Federal de Educação, Ciência e Tecnologia do Rio Grande do Norte Natal, Brasil.
