Realizado em Goiânia/GO, de 04 a 06 de Setembro de 2017.
ISBN: 978-85-85905-20-0
TÍTULO: Remoção de compostos fenólicos via imobilização de peroxidase de Extrato Bruto de Abobrinha Verde (Cucurbita pepo, L.) em polímero biodegradável de Caju Arbóreo do Cerrado (Anacardium othonianum, Rizz.)
AUTORES: Silva, T.M. (UNIVERSIDADE ESTADUAL DE GOIÁS) ; Souza, E.R.B. (UNIVERSIDADE FEDERAL DE GOIÁS) ; Caramori, S.S. (UNIVERSIDADE ESTADUAL DE GOIÁS)
RESUMO: Peroxidase de Abobrinha (Cucurbita pepo,L) (EBA) foi imobilizada em
caju arbóreo do Cerrado (Anacardium othonianum Rizz) (PEJU) via
adsorção física e ligação covalente. A quantidade de proteína do EBA foi de
2,69.10 -5 g.mL -1 e atividade enzimática (AE) de 23
UmL-1.Para adsorção física as melhores condições foram pH
7(fosfato de sódio 0,1 mol L-1), 120 min de agitação,10 mg
PEJU, 1mL de EBA, 42% da AE em 60°C, 7 usos repetidos e 50% de AE após 30
dias.Via ligação covalente foram 8 usos repetidos(21% da AE),pH 5 e pH
7(acetato e fosfato 0,1 molL-1, respectivamente),120 min de
agitação,20 mg PEJU, 1mL de EBA, 34% da AE em 60°C e 60% de AE (30 dias). A
redução de compostos fenólicos apresentou eficiência superior a 20%.
PALAVRAS CHAVES: Enzimas; Suporte biodegradável; Bioremedicação
INTRODUÇÃO: Compostos fenólicos ocorrem nos resíduos de uma ampla variedade de operações
industriais; quase todos são tóxicos (Liu et al, p.225,2002) sendo
incorporados na cadeia alimentar e gerando importantes problemas ambientais
(Gómez et al, p. 1016, 2006). Alguns métodos para sua remoção
envolvem o uso de microorganismos, carbono ativo ou oxidação química.
Contudo, tais métodos apresentam frequentemente desvantagens, tais como
baixa eficiência, alto custo ou o fato de gerarem produtos que são ainda
mais tóxicos do que os originais. Uma alternativa para tratar águas
residuais é usar enzimas imobilizadas (catalisadores biológicos) com
eficiência em condições amenas de reação, alta especificidade e
biodegradabilidade (Ramalho et al, p.50, 2016). Estudos preliminares
têm revelado na abobrinha (Cucurbita pepo) uma fonte rica de
peroxidase (Vieira et al, p.39, 2003) e polímeros naturais uma fonte
eficiente de imobilização de enzimas por ser de fácil obtenção,
biocompatível e biodegradável (Azevedo et al, p.27, 2007). No
Cerrado (presente em aproximadamente 22% do país), é encontrado o caju-
arbóreo-do-Cerrado (Anacardium othonianum Rizz)(Silva et al,
p. 46, 2001)com propriedades coloidais, espessantes, gelificantes,
emulsificantes, estabilizantes, aglutinantes (Bhushette e Annapure, in
press, 2017) e biodegradáveis (Akthar e Rui, in press,2017).
Neste sentido, a proposta deste trabalho é a de que o polissacarídeo do
caju-arbóreo-do-Cerrado ( A. othonianum ) é um suporte capaz de
imobilizar peroxidase de extrato de abobrinha verde (Cucurbita pepo
L) e ser aplicado (complexo polissacarídeo-peroxidase) para a remoção de
compostos fenólicos.
MATERIAL E MÉTODOS: Os nódulos exsudados dos cajueiros foram recolhidos, triturados e
dissolvidos em água (20% (p/v)) (Rinaudo-Milas, 1991). A solução foi
filtrada e precipitada com etanol absoluto (1:3, v/v). O polissacarídeo
(PEJU) foi triturado e armazenado a 4 °C até utilização. Para o PEJU tratado
com periodato de sódio (PEJUp), 0,05 g de PEJU foram agitados (30 min) com
2,0 mL de periodato de sódio 0,1 mol L -1 e 10 mL de tampão
fosfato de sódio 0,1 mol L -1, pH 7,0. O PEJUp foi precipitado
com etanol absoluto (1:3, v/v) por 24h. A análise morfológica de PEJU e
PEJUp foi realizada por microscopia eletrônica de varredura (Shimadzu,
modelo SSx 550, Japão) em 1000x. As amostras de abobrinha foram cortadas e
trituradas em tampão fosfato de sódio monobásico 0,1 mol L-1, pH
7,0 (1:1 (p/v), filtrada e armazenada a 4°C. A presença de proteínas no EBA
foi determinada por Bradford (1976). A atividade enzimática de peroxidase
(POX) foi determinada segundo Halpin e Lee (1987), sendo uma unidade de POX
considerada como um aumento de 0,1 absorvância/min. Para as técnicas de
imobilização foram variadas as concentrações de PEJU, PEJUp, EBA, pH de
imobilização, tempo, uso repetido, termoestabilidade e estabilidade em
armazenamento. Os testes com compostos fenólicos foram realizados conforme
Ramalho et al (2016). O EBA, PEJU-EBA e PEJUp-EBA foram incubados com
pirogalol, catecol, fenol, bromofenol, nitrofenol (1,0 mmol L-1)
e peróxido de hidrogênio (0,05 mol L -1). A concentração residual
de fenóis foi realizada conforme Lowry et al (1951). Teste T foi
aplicado utilizando o Software R Studio.
RESULTADOS E DISCUSSÃO: O PEJU apresentou superfície porosa irregular e cristalina (Fig. 1),com
massa extensa e amorfa, relevos ou depressões semelhantes ao polissacarídeo
de A. occidentale (Ramalho, 2014), favorecendo a aplicação deste em
processos como a imobilização de enzima. A atividade da POX de EBA foi de 23
U mL -1) e proteína de 2, 69.10 -5). gmL
-1). Na Tabela 1 encontram-se as melhores condições de
imobilização por adsorção e ligação covalente. A tecnologia de imobilização
de enzimas envolve a escolha de um suporte e método que resultem num
imobilizado ativo, estável e eficaz em condições variadas; sob este aspecto
percebe-se tanto via adsorção física (7 ciclos, 28% de atividade enzimática
(AE)) quanto ligação covalente (8 ciclos, 21% de AE) mostraram eficazes no
processo de uso repetido para o complexo EBA-PEJU e EBA-PEJUp,
respectivamente, fazendo destes, materiais promissores para aplicação
biotecnológica. A capacidade de remoção de fenóis através dos complexos EBA-
PEJU e EBA-PEJUp está mostrada na Tabela 2. EBA-PEJU e EBA-PEJUp são
eficazes para a remoção de fenóis, com remoção superior a 20% após 10 min de
reação. Não houve diferença estatística entre os tratamentos (p> 0,05)sendo
as duas técnicas eficientes na remoção dos fenóis. Singh e Singh (p. 127,
2002) através de HRP em pérolas de vidro via adsorção física obtiveram
resultados capazes de remover 95% dos compostos fenólicos após 30 min de
tratamento (Singh e Singh, p. 127, 2002) e 25% via imobilização por ligação
covalente (Lai e Lin, p. 1167, 2005).O uso de EBA e PEJU será benefício no
desenvolvimento de produtos novos com caraterísticas sustentáveis.
Figura 1. Eletromicrografia de polissacarídeo de Caju Arbóreo do Cerra

Tabelas 1 e 2.
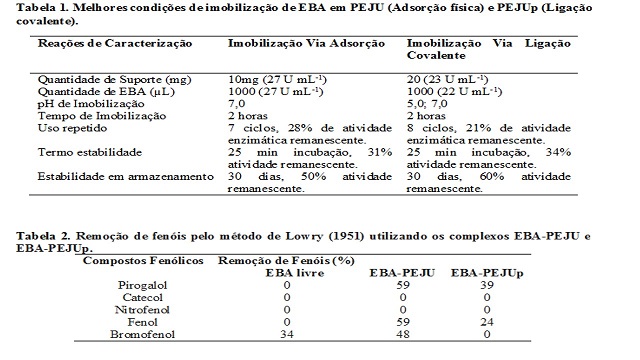
Tabela 1. Condições de imobilização de EBA em
PEJU (Adsorção física) e PEJUp (Ligação
covalente).
Tabela 2. Remoção de fenóis pelo método de
Lowry.
CONCLUSÕES: A Abobrinha Verde (Cucurbita pepo L.) apresentou atividade da
peroxidase, o que a torna fonte alternativa para aplicação em tecnologia
enzimática; além disso, o polissacarídeo de Caju arbóreo do Cerrado mostra-se
um material para imobilização de enzimas por adsorção física e ligação
covalente em diferentes condições de pH, baixo custo, biodegradável, não-
tóxico e extraído de forma sustentável. A redução de compostos fenólicos
através do sistema de enzima imobilizada apresentou alta eficiência para os
dois métodos propostos, desempenhando um papel significativo como
bioremediador.
AGRADECIMENTOS: A Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES) pela
bolsa de doutorado concedida a Thâmara Machado e Silva.
REFERÊNCIAS BIBLIOGRÁFICA: AKHTAR, M.; RUI, D.; Covalently cross-linked proteins & polysaccharides: Formation, characterisation and potential applications, Current Opinion in Colloid & Interface Science, 2017 <doi:10.1016/j.cocis.2017.01.002>
AZEVEDO, V. V. C., CHAVES, S. A., BEZERRA, D. C.; FOOK, M. V., COSTA, A. C. F. M., Quitina e Quitosana: aplicações como biomateriais, Revista Eletrônica de Materiais e Processos, v.2.3, 27-34, 2007.
BUCKERIDGE, M.S.; DIETRICH, S.M.C.; LIMA, D.U. Galactomannans as the reserve carbohydrate in legume seeds. Carbohydrate Reserves in Plants – Synthesis and Regulation. v 26, p. 283-315, 2000.
BRADFORD, M. A rapid and sensitive method for the quantitaion of microgram quantities of protein utilizing the principle of protein-dye binding; Anal Biochem., 72: 248-254, 1976
VIEIRA, IOLANDA CRUZ; LUPETTI, KARINA OMURO; FATIBELLO-FILHO, ORLANDO. Determination of paracetamol in pharmaceutical products using a carbon paste biosensor modified with crude extract of zucchini (Cucurbita pepo). Química Nova [online], Vol.26, n.1, pp.39-43, 2003.
GÓMEZ, J.L.; BÓDALO, A.; GÓMEZ, E.; BASTIDA, J.; HIDALGO, A.M.; GÓMEZ, M.; Immobilization of peroxidases on glass beads: An improved alternative for phenol removal; Enzyme and Microbial Technology 39, 1016–1022, 2006.
HALPIN, B.E.; LEE, C.Y. Effect of blanching on enzyme activity and quality changes in green peas. Journal of Food Science, v. 52, n 4, p. 1002-1005, 1987.
LAI YC, LIN SC. Application of immobilized horseradish peroxidase for the removal of p-chlorophenol from aqueous solution; Process Biochem 40, 1167–74, 2005.
LIU JZ, SONG HY, WENG LP, JI LN. Increased thermostability and phenol removal efficiency by chemical modified horseradish peroxidase. J Mol Catal B Enzym 18:225–32., 2002.
LOWRY, O. H.; ROSEBROUGH, N. J.; FARR, A. L; RANDALL, R. J. Protein measurement with the Folin-Phenol reagent. The Journal of Biological Chemestry, v. 193, p; 265-276, 1951.
OLIVEIRA, I. R. W. Z.; VIEIRA, I. C. Construção e aplicação de biossensores usando diferentes procedimentos de imobilização da peroxidase de vegetal em matriz de quitosana. Química Nova, v. 29, n. 5, p. 932-939, 2006.
RAMALHO, R.P.R.S.; SCALIZE, P.S.; CARAMORI, S.S. Peroxidase of Brazilian Cerrado grass as an alternative for agro industrial waste treatment, Revista Ambiente e Água, Vol. 11 Jan. / Mar. n. 1, 50-59, 2016.
RAMALHO, I. M.M.; Biopolímero da Goma de Cajueiro (Anacardium occidentale) como potencial excipiente farmacêutico. Trabalho de Conclusão de Curso, 28p. Universidade Estadual da Paraíba, 2014.
RINAUDO, M.; MILAS, M.; Polieletrólitos. In: GROOTE, R. A. M. C.; CURVELO, A. A. S. (ed.). São Carlos: Editora da USP, 1991.
SILVA, D. B. Frutas do Cerrado. Brasília: Embrapa Informação Tecnológica, p. 46-78, 2001.
SINGH N, SINGH J. Um método enzimático para remoção de fenol de efluentes industriais. Prep Biochem Biotechnol 32, 127-33, 2002.
