Realizado em Goiânia/GO, de 19 a 21 de Setembro de 2016.
ISBN: 978-85-85905-20-0
TÍTULO: APLICAÇÃO DE LÍQUIDOS IÔNICOS PRÓTICOS COMO AGENTES CATALÍTICOS PARA SÍNTESE DE TRIACETINA
AUTORES: Costa, K. (UFBA) ; Castro, T. (UFBA) ; Queiróz, L. (UFBA) ; Serra, J. (UFBA) ; Iglesias, M. (UFBA)
RESUMO: A triacetina é um composto químico artificial derivado da glicerina que na
indústria tem sido produzida, normalmente, na presença de catalisadores
ácidos, apresentando uma série de desvantagens. Neste trabalho, um conjunto
de líquidos iônicos próticos (LIPs) foi sintetizado e caracterizado, sendo
eles: citrato de monoetanolamina (2-HEACi), citrato de dietanolamina (2-
HDEACi), butirato de monoetanolamina (2-HEABu), butirato de dietanolamina
(2-HDEABu), formiato de monoetanolamina (2-HEAF), ftalato de monoetanolamina
(2-HEAFt) e propionato de monoetanolamina (2-HEAPr). O uso desses líquidos
como catalisadores contribui para o desenvolvimento de uma estratégia
sustentável na geração de produtos de valor agregado a partir da glicerina,
apresentando uma excelente atividade catalítica.
PALAVRAS CHAVES: Triacetina; Líquidos Iônicos Próticos; Catálise
INTRODUÇÃO: Os líquidos iônicos próticos, os“solventes verdes”, apresentam nos últimos
anos, progressos quanto à sua aplicação á temperatura ambiente, atraindo o
interesse da comunidade científica devido as suas características as quais
os permitem ser uma alternativa sustentável a solventes orgânicos
convencionais (PLECHKOVA e SEDDON, 2008). Os LIPs também apresentam uma
variedade de propriedades que lhes conferem utilidades em diversos setores
da indústria química, propriedades estas que não são apresentadas pelos
solventes orgânicos convencionais. Até agora, os líquidos iônicos consistem,
normalmente, de pequenos ânions e cátions volumosos (imidazólio, piridinio,
amônia quaternária, e fosfônio). Contra a forte atração eletrostática entre
os íons, o efeito estérico do grande tamanho do cátion evita que os líquidos
iônicos se solidifiquem a temperatura ambiente, como ocorre com outros sais.
A interação de Coulomb e os efeitos estéricos entre os íons são muito fortes
em comparação com a interação intermolecular entre moléculas polares, que o
comportamento dos líquidos iônicos é bem diferente daquele dos líquidos
polares convencionais.
A triacetina possui maior valor agregado quando comparada à glicerina. Na
sua síntese são utilizados catalisadores homogêneos ácidos (ácido sulfúrico)
que apresentam graves problemas técnicos: alta corrosão nas instalações e
difícil remoção do catalisador do produto. Além disso, a separação dos
contaminantes exige o uso de mais equipamentos, mais reagentes químicos e
mais operações unitárias, aumentando o consumo energético da unidade
produtiva. Este projeto aponta para uma mudança integral no processo
catalítico da triacetina a partir da substituição dos catalisadores
tradicionais homogêneos por uma catálise suportada usando LIPs como agentes
ativos.
MATERIAL E MÉTODOS: Para a síntese de Lips, foi utilizada a metodologia apresentada por Alvarez
et al. (2010). A amina foi colocada num balão de três tubuladuras, equipado
com um condensador de refluxo e um sensor de temperatura PT-100. O balão foi
montado em um banho térmico a fim de evitar o sobreaquecimento e a
degradação parcial dos produtos de síntese. O ácido orgânico foi adicionado
gota a gota, ao balão, sob agitação constante com uma barra magnética. A
agitação foi continuada durante 24 h à temperatura ambiente, a fim de se
obter um líquido viscoso no final da síntese.
Para o procedimento de purificação o produto de reação foi mantido sob uma
placa de aquecimento a 50 ºC por mais 48 horas, com agitação magnética
constante. Para o presente trabalho, foram selecionados os líquidos iônicos,
variando o tamanho dos cátions e ânions, para assim comparar a influência de
sua natureza na atividade catalítica.
Após serem sintetizados os líquidos foram enviados para análises de
ressonância magnética nuclear (RMN) e espectroscopia no infravermelho por
transformada de Fourier (FTIR) com o objetivo de ser usada para identificar
os compostos sintetizados (LIP).
Para síntese de triacetina os reagentes (glicerina, ácido acético e
catalisador) foram colocados em proporção estequiométrica no balão, equipado
com o condensador e um sensor de temperatura PT-100. O banho térmico foi
mantido a 60, 80 ou 100 °C e a mistura reacional sob agitação constante,
para garantir a homogeneidade da reação durante 4h de processo. Foram
recolhidas amostras em intervalos de tempos fixos que foram imediatamente
submetidas a um banho de gelo para cessar a reação.
Para quantificar a quantidade de triacetina formada durante a reação
utiliza-se a volumetria de neutralização ácido-base.
RESULTADOS E DISCUSSÃO: Ao reagir LIP´s ácidos com o mesmo número de moles: 2-HEABu e o 2-HDEABu de pH 5,34 e 5,65 respectivamente,
verificou-se que ambos apresentaram atividades catalíticas e que a atividade catalítica tem um melhor desempenho
com a diminuição do pH (Meirelles et al., 2013).
Para efeito de comparação entre o catalisador industrial convencional H2SO4, de pH 1,5, observa-se que o ácido
sulfúrico apresentou maior desempenho (92,94%) quando comparado ao LIP de maior conversão, 2-HEABu (81,8 % ) pois
este apresenta pH muito mais ácido (Meirelles et al., 2013).
Dentre os básicos, os LIP´s, 2-HEACi e 2-HDEACi, com pH 9,30 e 8,38 respectivamente e 3 sítios ativos
apresentaram melhor desempenho catalítico em relação aos demais (94,16 e 81,62% respectivamente). Esse maior
desempenho está associado a um maior número de sítios ativos que a estrutura dos líquidos possui alinhados a um
maior pH. Ainda não pode-se estabelecer uma relação diretamente proporcional entre o pH e o desempenho catalítico
entre os LIP´s básicos.
Existe um aumento de conversão proporcional a um aumento de temperatura,fato que foi comprovado pelo autor
Meirelles et al., (2013). Sendo assim, a reação que apresentou melhor desempenho foi aquela realizada a 100ºC.
Observou-se que a reação sem catalisador realizada a 100ºC consegue ter um desempenho melhor do que a reação
catalisada pelo LIP á 60ºC. Nesse caso, a alta temperatura prevaleceu sobre a influência do catalisador LIP para a
reação realizada à 60ºC.
Dos resultados obtidos para o 2-HDEACi a reação mesmo realizada a baixas temperaturas (60ºC), conseguiu superar a
reação Branco na temperatura de 100ºC. Ou seja, a estrutura funcional do LIP fez as reações apresentarem melhor
desempenho mesmo em baixas temperaturas.
Comparação dos LIP´s ácidos com o H2SO4
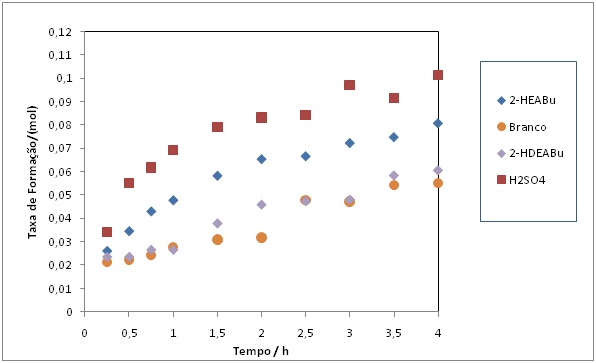
Ambos os líquidos iônicos apresentaram atividades
catalíticas. Observa-se que a atividade catalítica
tem um melhor desempenho com a diminuição do pH.
Desempenho catalítico dos LIP’s básicos
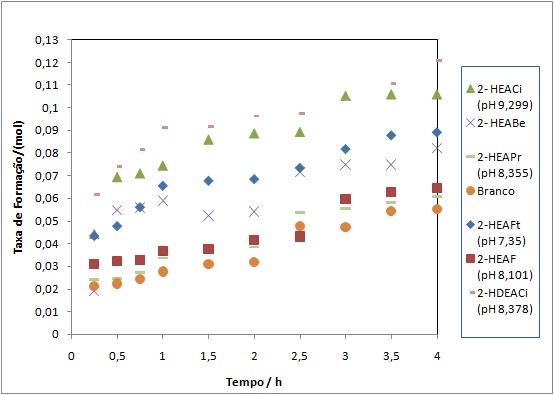
Observa-se pelo gráfico que os líquidos que
possuem pH´s variando entre 7,35 ≤ pH≤ 8,36
possuem atividades catalíticas entre baixa e
intermediária.
CONCLUSÕES: Utilizando-se líquidos iônicos próticos como catalisadores, foi obtida uma
taxa de conversão satisfatória, aproximando-se da taxa do catalisador
convencional (ácido sulfúrico). A utilização desses líquidos não possuem as
desvantagens ambientais e técnicas que o ácido sulfúrico proporciona em nível
industrial para obtenção de triacetina quando comparado ao uso do catalisador
convencional.
A continuidade das pesquisas ajudará a definir os cátions e os ânions
que devem compor a estrutura de novos líquidos iônicos próticos a serem
sintetizados.
AGRADECIMENTOS: Ao PIBIC e à CAPES pela bolsa de iniciação científica de Karolyne S. Costa. Ao
professor Miguel Iglesias pela orientação e suporte.
REFERÊNCIAS BIBLIOGRÁFICA: [1] PLECHKOVA, N.V.; SEDDON, K.R. Applications of ionic liquids in the chemical industry. Chemical Society Reviews, v. 37, p. 123-150. 2007.
[2] ALVAREZ, V.H.; MATTEDI, S.; MARTIN, P.M.; AZMAR, M.; IGLESIAS, M. Thermophysical properties of binary mixtures of {ionic liquid 2-hydroxy ethylammonium acetate + (water, methanol, or ethanol). Journal of Chemical Thermodynamics, v. 43, n. 7, p. 997-1010. 2011.
[3] BRENNECKE, J.F.; MAGINN, E.J. Ionic liquids: Innovative fluids for chemical processing. AIChe Journal, v.47, n.11, p. 2384-2389. 2011.
[4] IGLESIAS, M.; TORRES, A.; GONZALEZ-OLMOS, R.; SALVATIERRA, D. Effect of temperature on mixing thermodynamics of a new ionic liquid: {2-Hydroxy ethylammonium formate (2-HEAF) + short hydroxylic solvents}. Journal of Chemical Thermodynamics, v.40, n.1, p. 119-133. 2008.
[5] MATTEDI, S.; CARVALHO, P.J.; COUTINHO, J.A.P.; ALVAREZ, V.H.; IGLESIAS, M. High pressure CO2 solubility in N-methyl-2-hydroxyethylammonium protic ionic liquids. Journal Supercritical Fluids, v. 56, n. 3, p. 224-230. 2011.
[6] ZHAO, D.; WU, M.; KOU, Y.; MIN, E. Ionic liquids: Applications in catalysis. Catalysis Today, v.74, n. 1-2, p.157-189. 2002.
[7] PERIC, B.; MARTÍ, E; SIERRA, J.; CRUAÑAS, R.; IGLESIAS, M.; GARAU, M.A. Terrestrial ecotoxicity of short aliphatic protic ionic liquids. Environmental Toxicology and Chemistry, v. 30, n. 2, p. 2802-2809. 2011.
[8] MEIRELES, Bruno A.; PEREIRA, Vera Lúcia P. Synthesis of bio-additives: transesterification of ethyl acetate with glycerol using homogeneous or heterogeneous acid catalysts. Journal of the Brazilian Chemical Society, v. 24, n. 1, p. 17-57, 2013.
