Realizado em Maceió/AL, de 28 a 30 de Agosto de 2013.
ISBN: 978-85-85905-04-0
TÍTULO: Controle de qualidade em paracetamol, cápsulas manipuladas
AUTORES: Rodrigues, A.P. (UNIVERSIDADE DE PASSO FUNDO) ; Ortiz, J.C. (UNIVERSIDADE DE PASSO FUNDO) ; Bertol, C.D. (UNIVERSIDADE DE PASSO FUNDO) ; Boff, P. (UNIVERSIDADE DE PASSO FUNDO)
RESUMO: A crescente demanda de medicamentos proporcionada pela indústria farmacêutica nos últimos anos, fez com que, a preocupação com um controle de qualidade mais efetivo acerca dos medicamentos aumentasse. Para que um fármaco seja de fato eficaz no tratamento e prevenção de doenças, deve passar por testes específicos de acordo com os Compêndios Oficiais. Assim, este projeto de pesquisa realizou o controle de qualidade em cápsulas de paracetamol manipulado de duas farmácias distintas. Os ensaios de controle de qualidade foram realizados e comparados com os parâmetros apontados na Farmacopéia Brasileira, Volume 2, 5ª edição de 2010. Após a realização dos testes, verificou-se que algumas cápsulas apresentaram não conformidades, indicando que estas não poderiam ser comercializadas para a população.
PALAVRAS CHAVES: paracetamol; qualidade; manipulação
INTRODUÇÃO: O desenvolvimento mundial provocou mudanças na vida do ser humano. O trabalho, a rotina e a correria do dia-a-dia, trouxeram, também, o estresse e a pré-disposição às doenças. Essas doenças foram amenizadas ou até mesmo curadas devido aos medicamentos desenvolvidos, que usados de forma racional, propiciam a melhora da qualidade de vida da população (SHIVHARE, et al., 2010).
A indústria farmacêutica está se aprimorando cada vez mais ao investir em novas pesquisas e tecnologias para melhor atender a sociedade. Mas, para que o fármaco realmente auxilie no tratamento das enfermidades, é necessário, além do paciente seguir as prescrições médicas, que este cumpra com as especificações descritas nos compêndios oficiais como, por exemplo, a Farmacopéia Brasileira.
Nos últimos anos, houve um aumento na venda de produtos manipulados, pois estes podem ser formulados de maneira diferenciada, de forma a sanar as necessidades individuais de cada paciente. No entanto, a manipulação de medicamentos pode apresentar desvantagens pois, a qualidade deste depende de fatores como a habilidade do farmacêutico, manipuladores, adequação dos equipamentos, e utilização de insumos que atendam aos critérios de qualidade estabelecidos pela legislação vigente (BRASIL, 2012).
Dessa forma, este estudo teve por objetivo realizar ensaios de controle de qualidade em cápsulas manipuladas de paracetamol, analgésico-antipirético mais utilizado no país, para verificar se esse princípio ativo está em conformidade com os parâmetros estabelecidos na Farmacopéia Brasileira 5ª edição, e também, analisar o medicamento manipulado que é fornecido aos consumidores com o intuito de comprovar a qualidade deste, e consequentemente, cumprir com a função na melhora/cura do paciente que o consome.
MATERIAL E MÉTODOS: As cápsulas de paracetamol (375 mg) foram adquiridas em duas farmácias de manipulação distintas, denominadas neste trabalho como farmácia A e farmácia B. Para o teste de determinação de peso médio, mediu-se a massa de 20 unidades da amostra, removeu-se o conteúdo de cada uma, e mediu-se a massa novamente. Calculou-se o peso médio através dos valores obtidos. No teste de desintegração, as cápsulas foram submetidas ao desintegrador para verificar quanto tempo levavam até desintegrar-se totalmente. Já, para o teste de doseamento, mediu-se a massa de 5 cápsulas de paracetamol e transferiu-se quantidade do pó equivalente a 0,075 g para balão volumétrico de 100 mL, adicionou-se 25 mL de NaOH 0,1 mol/L, 50 mL de água purificada, homogeneizou-se e completou-se o menisco. Após homogeneizar e filtrar retirou-se uma alíquota de 5 mL e transferiu-se para balão volumétrico de 50 mL, completado com água. Dessa solução, retirou-se outra alíquota de 5 mL transferiu-se para balão de 50 mL adicionou-se 5 mL de NaOH 0,1 mol/L e completou-se o volume com água.
Para o preparo da solução padrão de paracetamol, mediu-se uma massa equivalente à 0,0250 g de substância química de referência, que foi diluída com NaOH 0,01 mol/L em balão volumétrico de 100 mL. Dessa solução, retirou-se três alíquotas de 3 mL, e transferiu-se cada alíquota para balão de 100 mL que foi completado até o menisco com NaOH 0,01 mol/L.
Mediram-se as absorbâncias das amostras e da solução padrão em espectrofotômetro em comprimento de onda de 257 ηm ajustando o zero com NaOH 0,01 mol/L. Para o teste de identificação, através da temperatura de fusão, transferiu-se uma massa equivalente 0,5 g de paracetamol, diluiu-se em 20 mL de acetona. Filtrou-se. Evaporou-se o filtrado em estufa e realizou-se as leituras no DSC.
RESULTADOS E DISCUSSÃO: A determinação de peso médio é um teste essencial para avaliar a qualidade de um lote de medicamentos. Segundo a monografia da Farmacopéia Brasileira, pode-se ter um limite de variação de ± 7,5%, onde duas unidades podem ser toleradas fora deste limite. Assim, as amostras analisadas da farmácia A, não cumpriram o teste, uma vez que 8 unidades apresentaram-se fora dos limites estipulados. O peso médio encontrado para as cápsulas da farmácia A foi de 0,34953 g. Já, as cápsulas da farmácia B, foram aprovadas no teste, uma vez que apresentaram todas as unidades dentro dos limites superior e inferior. O peso médio obtido para as cápsulas foi de 0,36577 g.
O teste de desintegração possibilita a avaliação do tempo em que determinado medicamento demora até desintegrar-se totalmente. Segundo a monografia da Farmacopéia Brasileira, as cápsulas devem estar completamente desintegradas em um tempo de até 45 minutos. As cápsulas da farmácia A desintegraram-se num tempo de 3 minutos e 18 segundos, e as da farmácia B, desintegraram-se em 3 minutos e 2 segundos, o que permite afirmar que ambas foram aprovadas no teste.
Doseamento é o teste utilizado para quantificar o teor de princípio ativo presente em determinado medicamento. A Farmacopéia Brasileira estabelece que o medicamento deve conter no mínimo 95% e no máximo 105% da quantidade declarada do princípio ativo. Assim, as cápsulas analisadas da farmácia A não cumpriram o teste, pois atingiram uma média de 87,2% de paracetamol, segundo o que apresenta a Tabela 1.
No entanto, as amostras da farmácia B cumpriram o teste pois, a média obtida para o percentual de paracetamol foi de 98,1%, segundo os dados da Tabela 2. Por fim, no teste de identificação ambas as cápsulas foram aprovadas obtendo temperatura de fusão de 171,2ºC.
Tabela 1
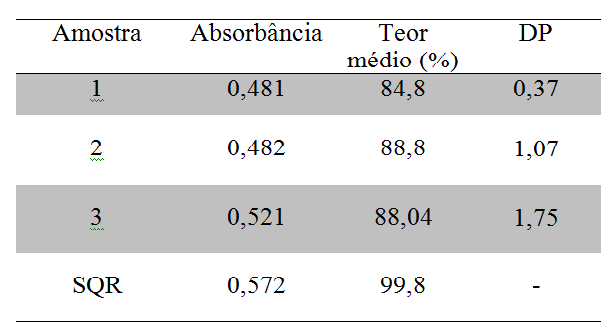
Tabela 1: Valores obtidos para as cápsulas da farmácia A
Tabela 2

Tabela 2: Valores obtidos para as cápsulas da farmácia B
CONCLUSÕES: Os dados obtidos neste estudo permitiram concluir que nem sempre adquire-se um produto com eficácia e qualidade comprovada. Através dos testes realizados, pôde-se verificar que os medicamentos e produtos manipulados variaram de uma farmácia para outra e a qualidade depende de muitos fatores, tais como habilidade do manipulador, qualidade da matéria prima, entre outros. Ainda, observou-se que as cápsulas da farmácia A, apresentaram algumas não conformidades em cumprimento aos parâmetros estabelecidos na monografia da Farmacopéia Brasileira.
AGRADECIMENTOS:
REFERÊNCIAS BIBLIOGRÁFICA: BRASIL, Agência Nacional de Vigilância Sanitária, 2012. Disponível em < http://portal.anvisa.gov.br/wps/content/Anvisa+Portal/Anvisa/Inicio/Medicamentos/Assunto+de+Interesse/Glossario/Medicamento+de+referencia > Acessado em 10 de maio de 2012.
SHIVHARE, S. C.; KUNJWANI, H. K.; MANIKRAO, A. M.; BONDRE, A. V. Drugs Hazards and Rational Use of Drugs: A Review. Journal of Chemical and Pharma ceutical Research., vol.2, no.1, 2010. Disponível em <http://jocpr.com/second-issue/J.%20Chem.%20Pharm.%20Res.,2010,%202(1)%20106-112.pdf>. Acessado em 16 de maio de 2012.
