APOIO




Catálise
Porciuncula Ramos dos Anjos, R. (UFF) ; de Oliveira dos Santos, A. (UFF) ; Molina Antoniassi, R. (USP) ; Cambraia Alves, O. (UFF) ; Martins da Silva, J.C. (UFF)
Catalisadores contendo nanopartículas cúbicas de Pt com orientação preferencial Pt(100) foram sintetizados a partir do método de redução por álcool utilizando KBr como agente direcionador de formato, além de catalisadores sem orientação preferencial, a fim de serem usados para reação de oxidação do metanol (ROM) em meio básico. Difração de raios-x comprovou a estrutura cúbica de face centrada para a Pt e micrografias de transmissâo eletrônica confirmaram a presença de formas cúbicas para os materiais (100) e esféricas para os demais materiais sintetizados. Nas voltametrias cíclicas e cronamperometrias, foi possível avaliar a atividade catalítica dos mesmos frente a ROM, com Pt/C (100) apresentando melhor desempenho. A densidade de corrente da Pt(100) foi 2,35 vezes maior que a de Pt/C.
reação oxidação metanol; Pt cúbica; PtSnO2 cúbica
Células a combustível (CaC) a metanol direto têm ganhado destaque no contexto de geração de energias renováveis e sustentáveis pela sua alta eficiência de conversão em energia elétrica, baixa emissão de poluentes e funcionamento simples (WANG, 2017). Elas apresentam a vantagem de menor custo e de alimentação do sistema sobre as CaCs alimentadas por hidrogênio (LIU, et al, 2006). Os dois pontos-chave no funcionamento de uma CaC são a membrana trocadora de íons e o eletrocatalisador (LIU, et al, 2012). A membrana trocadora de íons pode ser de prótons ou de ânions, todavia, o uso de meio alcalino favorece a cinética da reação de oxidação do metanol (ROM), diminui efeitos de contaminação por CO e de crossover do metanol, além de deixar o meio menos corrosivo frente ao meio ácido (HIGA, et al, 2020). O eletrocatalisador pode ser constituído por metais nobres, como platina, que tem alta atividade catalítica para a ROM (MANSOR, et al, 2019). Também pode ser constituído composto de materiais bimetálicos, com a possibilidade de um deles ser não nobre, já que o meio alcalino favorece o uso desses materiais (ANTOLINI, et al, 2010). Nesse trabalho, foram sintetizados nanopartículas a base de platina (PtNPs) e platina-estanho suportadas em carbono Vulcan por meio do método de redução por álcool com morfologia controlada, utilizando KBr como agente direcionador de morfologia (ANTONIASSI, et al, 2016; ANTONIASSI, et al, 2017) e sem morfologia controlada, na ausência de KBr. Os materiais foram caracterizados pelo método de difração de raios-x (DRX) e microscopia eletrônica de transmissão (TEM). A atividade dos eletrocatalisadores frente a reação de oxidação do metanol (ROM) em meio alcalino foi avaliada por experimentos de voltametria cíclica (CV) e cronoamperometria (CA).
Pt/C (100) foi sintetizado utilizando uma solução de etilenoglicol e água Milli-Q® na proporção de 3:1 (v/v) e carbono Vulcan, aquecidos até 150 °C com agitação magnética. Em seguida, foi adicionado 30% da quantidade de H2PtCl6.6H2O e deixado em refluxo por 20 min. KBr foi adicionado (na proporção molar Br:Pt = 300:1) e deixado em refluxo por mais 20 min. Os outros 70% do precursor de Pt foram adicionados e mantidos sob refluxo por 3 h em refluxo. A suspensão foi filtrada, lavada com água destilada e secada por 2h a 70°C. A síntese de PtSnO2/C (100) foi feita utilizando a mesma metodologia, apenas adicionando o cloreto de estanho (II) hidratado 10 min antes do final da síntese. Pt/C e PtSnO2/C sem orientação preferencial também foram sintetizados pelo método de redução de álcool, sem adição de KBr e a fonte de metal foi adicionada em uma etapa. As análises de DRX foram feitas no aparelho X’Pert Pro PW3042/10, na faixa entre 20°<2θ>90° (ΚαCu= 1,54 Å, escaneamento 0.025°s-1). Imagens de TEM foram obtidas pelo modelo JEOL JEM-2100 a 200 kV. Medidas eletroquímicas foram conduzidas no equipamento bipotenciostato μStat400 Metrohm DropSens e numa célula contendo contraeletrodo de platina, eletrodo de referência Hg/HgO e um eletrodo de carbono vítreo como eletrodo de trabalho (ET). Uma suspensão catalítica feita do catalisador, água, 2-propanol e Nafion® foi depositada sobre o ET e secada a 60°C por 10 min. Experimentos de CV foram feitos após borbulhamento de N2 por 10 min em 1 mol L−1 KOH (eletrólito). Os brancos foram coletados em potenciais de −0.85 a 0.1 V a 50 mVs−1 por 10 ciclos. A atividade catalítica frente a ROM foi avaliada utilizando 1 mol L−1 CH3OH no eletrólito por 5 ciclos no mesmo potencial. Os testes de CA foram feitos durante 900 s no potencial de −0.3 V.
O difratograma para as PtNPs mostram picos em 39.8°, 46.2°, 67.5° e 81.3°, atribuídos aos planos cristalinos Pt(111), Pt(200), Pt(220) and Pt(311), nessa ordem, para a estrutura cúbica de face centrada da Pt (ANTONIASSI, et al, 2017). As micrografias TEM dos eletrocatalisadores de PtNPs mostram que todos os materiais estão dispersos adequadamente na suspensão. PtSnO2/C (100) e Pt/C (100) tem estruturas cúbicas, com tamanho aproximado de 9,4 e 9,0 nm. Os materiais policristalinos de PtSnO2/C e Pt/C tem forma majoritariamente esférica, com tamanho aproximado de 3,7 e 4,4 nm. Nos brancos de CV, (Fig. 1) o pico de dessorção de hidrogênio em -0,64 V é associado aos sítio de Pt(110) e o pico -0,53 V, a contribuição de Pt(100). O aumento dessa proporção nos materiais preferencialmente orientados, Pt/C (100) e PtSnO2/C (100), evidencia o alto número de sítios de Pt(100) e de morfologia cúbica nesses materiais (ANTONIASSI, et al, 2017; BARBOSA, et al, 2020). O pico da CV em metanol (Fig. 1) no sentido positivo é atribuído a ROM e o pico no sentido negativo é relacionado a intermediários reativos da reação. A ROM ocorre a menores potenciais para os materiais Pt/C (100) e PtSnO2/C (100), o que indica melhor atividade catalítica para os materiais cúbicos do que os policristalinos. Além disso, o pico de densidade de corrente obtida para o Pt/C (100) foi 2,35 vezes maior que o de Pt/C. A cronoamperometria (Fig. 2) mostra que todos os materiais tiveram decrécimo em sua atividade ao longo do tempo, sendo o maior para o Pt/C (100), contudo, esse material apresentou maior densidade de corrente ao longo de todo o experimento, tendo melhor desempenho geral.
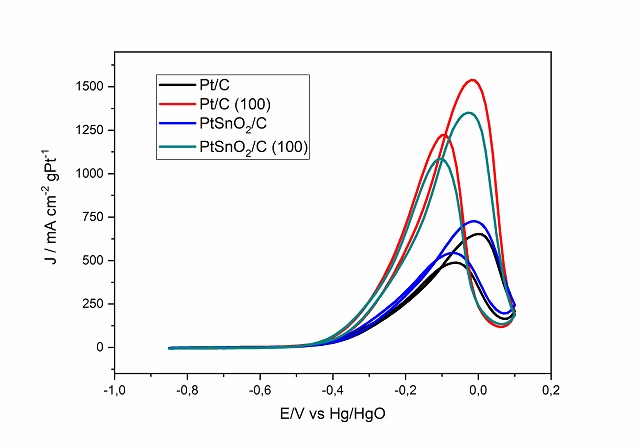
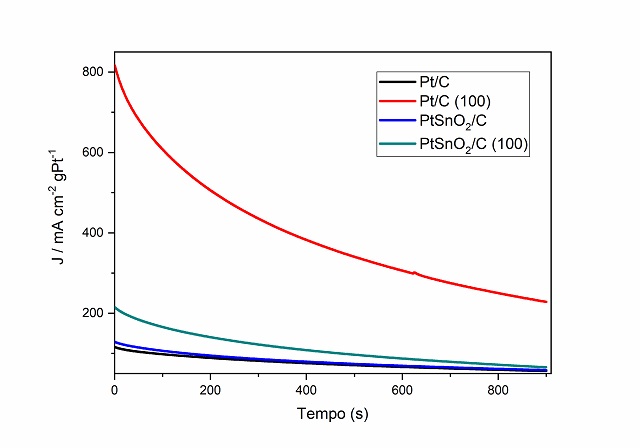
Nesse trabalho, a influência da morfologia e composição de catalisadores a base de Pt foram estudados. PtNPs com morfologia cúbica preferencial utilizando KBr como direcionador foram sintetizadas, confirmadas TEM e pela razão entre os dois picos de dessorção de hidrogênio obtidos nos brancos de CV. Nos experimentos de CV com metanol, a maior corrente obtida foi pelo Pt/C (100), seguido pelo PtSnO2/C (100), PtSnO2/C e Pt/C, sendo 2,35 vezes a corrente do primeiro em relação ao último. Nas análises de CA o Pt/C (100) apresentou melhor desempenho também frente a ROM.
Os autores agradecem ao CBPF, CAPES, LNNANO, CNPQ, FAPERJ (processo n. E-26/211.371/2019 (250734)), CNPEM
ANTOLINI, E.; GONZALEZ, E. R. Alkaline direct alcohol fuel cells. Journal of Power Sources, 195, n. 11, p. 3431-3450, 2010.
ANTONIASSI, R. M.; OTUBO, L.; VAZ, J. M.; OLIVEIRA NETO, A. et al. Synthesis of Pt nanoparticles with preferential (100) orientation directly on the carbon support for Direct Ethanol Fuel Cell. Journal of Catalysis, 342, p. 67-74, 2016.
ANTONIASSI, R. M.; SILVA, J. C. M.; LOPES, T.; OLIVEIRA NETO, A. et al. Carbon-supported Pt nanoparticles with (100) preferential orientation with enhanced electrocatalytic properties for carbon monoxide, methanol and ethanol oxidation in acidic medium. International Journal of Hydrogen Energy, 42, n. 48, p. 28786-28796, 2017.
ANTONIASSI, R. M.; SILVA, J. C. M.; OLIVEIRA NETO, A.; SPINACÉ, E. V. Synthesis of Pt+SnO2/C electrocatalysts containing Pt nanoparticles with preferential (100) orientation for direct ethanol fuel cell. Applied Catalysis B: Environmental, 218, p. 91-100, 2017.
BARBOSA, J. R.; LEON, M. N.; FERNANDES, C. M.; ANTONIASSI, R. M. et al. PtSnO2/C and Pt/C with preferential (100) orientation: High active electrocatalysts for ammonia electro-oxidation reaction. Applied Catalysis B: Environmental, 264, p. 118458, 2020.
HIGA, M.; MEHDIZADEH, S.; FENG, S.; ENDO, N. et al. Cell performance of direct methanol alkaline fuel cell (DMAFC) using anion exchange membranes prepared from PVA-Based block copolymer. Journal of Membrane Science, 597, p. 117618, 2020.
LIU, G.; SHANG, Y.; XIE, X.; WANG, S. et al. Synthesis and characterization of anion exchange membranes for alkaline direct methanol fuel cells. International Journal of Hydrogen Energy, 37, n. 1, p. 848-853, 2012.
LIU, H.; SONG, C.; ZHANG, L.; ZHANG, J. et al. A review of anode catalysis in the direct methanol fuel cell. Journal of Power Sources, 155, n. 2, p. 95-110, 2006.
MANSOR, M.; TIMMIATI, S. N.; LIM, K. L.; WONG, W. Y. et al. Recent progress of anode catalysts and their support materials for methanol electrooxidation reaction. International Journal of Hydrogen Energy, 44, n. 29, p. 14744-14769, 2019.
WANG, Y. Methanol Electrooxidation Reaction in Alkaline Medium on Glassy Carbon Electrode Modified with Ordered Mesoporous Ni/Al2O3. International Journal of Electrochemical Science, 12, p. 2194-2206, 2017.