ÁREA
Química Ambiental
Autores
Cardoso, W.S. (UFRJ) ; Yokoyama, L. (UFRJ) ; Santos, F.S. (UFRJ) ; Orlanda, J.F.F. (UEMASUL)
RESUMO
O glifosato é o herbicida sistêmico de amplo espectro e não seletivo mais utilizado no mundo. O seu crescente e excessivo uso em muitos países nos últimos anos, tem gerado preocupações ambientais. Dessa maneira, o objetivo deste estudo foi avaliar a degradação do glifosato por meio de um agente oxidante (PMS) gerador de radicais SO4•-, com o auxílio de micropartículas de ferro zero valente como catalisador. Foi aplicado um planejamento fatorial 23 utilizando as variáveis: concentração do agente oxidante, pH e tempo de contato. A avaliação da eficiência da degradação do glifosato, se deu por meio do decaimento da absorbância (medida em λ 570 nm) pelo tempo de reação, o qual os resultados mostraram uma redução de 70% em 20 min.
Palavras Chaves
Glifosato; Degradação; Radical Sulfato
Introdução
O crescimento populacional mundial impulsionou o consumo global de alimentos, demandando um aumento na produção agrícola para atender essa necessidade. A agricultura desempenha um papel fundamental nesse contexto, sendo responsável por suprir essa demanda crescente (JYOTHI et al., 2022; SPRINGMANN et al., 2018). O setor agrícola enfrenta o desafio de expandir sua produção, o que envolve explorar novas áreas e adotar sistemas de cultivo alternativos, como rotação de culturas e agroflorestas. No Brasil, a área cultivável deverá aumentar consideravelmente, tornando o país um dos principais produtores mundiais de grãos (BRASIL, 2022; BRASIL, 2021). No entanto, o crescimento das áreas cultivadas aumenta a exposição a pragas e plantas daninhas, levando ao desenvolvimento de técnicas de controle agrícola (HASANUZZAMAN et al., 2020; LIMA, 2019). O manejo de plantas daninhas é particularmente complexo, influenciado pela diversidade de espécies, tipos de culturas e condições climáticas (WONG et al., 2022). Essas plantas competem por recursos, prejudicando o crescimento das culturas e a produtividade agrícola, o que exige abordagens como o uso de herbicidas (HASANUZZAMAN et al., 2020; CHAUHAN, 2020; SALOMÃO et al., 2020). Dentre os herbicidas, destaca-se o glifosato, com característica sistêmica, utilizado em plantas daninhas pós-emergentes em várias culturas, como café, cana-de-açúcar, soja, entre outras (SYNGENTA, 2022; NORTOX, 2021). Porém, o emprego de agroquímicos nas lavouras causa preocupações ambientais devido à possibilidade de contaminação de águas superficiais e subterrâneas, solo e ar, resultando também em problemas relacionadas à saúde pública, (JYOTHI et al., 2022; HAZARAIMI et al., 2022; VILLETTE et al., 2022; RAWTANI et al., 2018). Dessa maneira, os Processos Oxidativos Avançados (POA) emergem como uma tecnologia capaz de criar radicais com potencial redutor, impulsionando a oxidação de diferentes poluentes, com destaque para o radical sulfato (SO4•−), que é gerado a partir do persulfato (PS, S2028−) e peroximonosulfato (PMS, HSO5−) (WANG; WANG, 2018). O PMS é um reagente químico com potencial redox de 1,82 V, usado na degradação de poluentes via POA. Sua estabilidade e alto potencial de oxidação são resultado de ativações por calor, radiação UV, metais de transição, catalisadores de carbono, pH alcalino, eletrólise, entre outros. Isso lhe permite gerar radicais sulfato com potencial redox elevado (2,5-3,1 V) (YANG et al., 2022; WANG; WANG, 2018). Entre as ativações do PMS, os metais de transição e óxidos metálicos, especialmente o ferro zero valente (Fe0), têm sido amplamente estudados para degradar compostos orgânicos. O ferro elementar e seus óxidos são destacados devido à sua abundância, baixa toxicidade e viabilidade econômica em comparação com outros metais de transição (DUAN et al., 2021; WANG; WANG, 2018; RASTOGI et al., 2009). Diante do exposto, este trabalho está voltado para avaliar a degradação do glifosato por meio de um agente oxidante (PMS) gerador de radicais SO4•-, com o auxílio de micropartículas de ferro zero valente como catalisador.
Material e métodos
Padrões e reagentes Foram utilizados padrões analíticos com grau de pureza elevada sem purificação prévia. Os reagentes utilizados foram: glifosato padrão analítico (pureza <= 100%) adquiridos da Merk e glifosato comercial (TOUCHDOWN, 62% m/v) adquirido da Syngenta Proteção de Cultivos LTDA, peroximonosulfato (PMS, HSO5−), ferro zero valente (Fe0), ninidrina (Química Moderna, P.A.), molibdato de sódio dihidratado (Êxodo Científica), hidróxido de sódio (Êxodo Científica) e ácido acético glacial (2%, Dinâmica). Utilizou-se também água ultra pura (MiliQ) em todos os experimentos. Preparo das soluções Uma solução estoque de glifosato comercial (1000 mgL-1) foi preparada em água ultra pura e armazenada em frasco âmbar para ser utilizada nos experimentos. Soluções de hidróxido de sódio a 0,1 mM e ácido acético a 0,1mM foram preparadas para a correção do pH da solução. A solução cromogênica foi preparada utilizando ninidrina e molibdato de sódio, ambas em concentração de (5%, m/v). Planejamento experimental Para realizar o experimento de planejamento fatorial completo 2³, foram conduzidos 8 experimentos e 3 corridas em ponto central, totalizando 11 experimentos. Os fatores independentes (ou parâmetros) examinados foram a concentração inicial de PMS, o pH inicial e o tempo de contato. Como fator dependente (ou resposta) teve-se o decaimento da absorbância. As condições experimentais, bem como as variáveis e seus respectivos níveis (-1, 0, +1), estão detalhados na Tabela 1. Utilizou-se o software Statistica 10.0 para o processamento dos dados estatísticos, visando a análise dos gráficos gerados pelo software. Ensaios de degradação do glifosato Uma solução de 100 mL de glifosato (25 mgL-1) foi adicionada a um Erlenmeyer de 250 mL contendo Fe0, ficando sob agitação turbulenta constante (1350 rpm) por 10 min, seguida por mais 30-60 min de agitação (250 rpm) para atingir as condições de equilíbrio de adsorção e dessorção. Em seguida, uma solução de 10 mL de PMS (50-150 mgL-1) foi adicionada ao Erlenmeyer para iniciar a reação, mantendo-se a agitação em 250 rpm por 30 min. Foram retiradas alíquotas (3 mL) em tempos predeterminados e levadas para centrifugação a 4000 rpm por 15 min, afim de precipitar as partículas coloidais de ferro. Após a centrifugação, 2 mL do sobrenadante foram adicionados na solução cromófora (ninidrina e molibdato de sódio a 5%), conforme metodologia proposta por Nagaraja e Bhaskara, (2006). Por fim, procedeu-se com a leitura da absorbância no espectrofotômetro Femto 800XI, no comprimento de onda máximo, em 570 nm. Todos os ensaios foram realizados em triplicata.
Resultado e discussão
Inicialmente, foram realizados testes preliminares para avaliar a degradação do
glifosato apenas utilizando o catalisador (Fe0) e o agente oxidante (PMS). Os
resultados obtidos não foram satisfatórios, levando a um incremento na
absorbância, ao invés de um decaimento, o que pode estar relacionado a não
distinção entre o composto principal do seu subproduto por análise
espectrofotométrica (HERINGER, 2019).
Outros autores, também reportaram resultados similares, onde o PMS sozinho ou o
catalizador sozinho não foi capaz de degradar o glifosato (LI et al., 2023),
apresentou baixa degradação (DUNG et al., 2023; DUNG et al., 2021). Para
corrigir este erro, foi realizado a centrifugação das alíquotas após a reação, a
fim de precipitar as partículas coloidais de ferro remanescentes na solução, o
qual pode interferir na leitura da absorbância (NAGARAJA; BHASKARA, 2006).
Após tal correção, foi possível obter até 77% de redução da absorbância para as
seguintes condições experimentais: pH inicial (4); concentração de PMS (100 mgL-
1); Fe0 (50 mgL-1); e concentração de glifosato (25 mgL-1). A partir deste
resultado, foi traçado e executado o planejamento experimental.
O planejamento experimental permitiu avaliar a interação entre as variáveis
estudadas, afim de otimizar o sistema de tratamento proposto. Utilizando o
software Statistica 10.0, com nível de confiança de 95%, foram gerados os
gráficos a partir dos resultados obtidos do planejamento fatorial 2³. Como pode
ser observado na Figura 1 (a), todas as variáveis apresentaram significância no
planejamento (p>0,05), com destaque para o PMS e sua interação com o pH. Além
disso, a curvatura demonstrou-se ser altamente significativa (R2 0,971 e Ajuste
0,963) para o modelo proposto, considerando que, o modelo linear (R2 ,0585 e
Ajuste ,0490), apresentou baixa explicabilidade, logo, o ajuste quadrático é
mais apropriado para representar modelo deste experimento por ser bastante
preditivo. Na Figura 1 (b), o tempo de contato foi fixado em seu nível de maior
significância (60 min), sendo em seguida, gerado o gráfico da superfície de
resposta para o experimento, onde as variáveis que apresentaram maior influência
no decaimento da absorbância foi o pH (4), associado a uma concentração de PMS
elevada (150 mgL-1), resultando em aproximadamente 70% de degradação do
glifosato. A Figura 1 (c), ilustra as maiores eficiências de degradação do
glifosato pelo sistema de tratamento proposto nas condições dos ensaios III e
IV. É possível notar que ocorre uma rápida degradação no primeiro minuto de
reação, aumentando nos minutos seguintes, porém, a uma velocidade mais lenta,
até atingir o equilíbrio por volta de 20 min. Dessa maneira, o catalisador (Fe0)
levou a uma rápida ativação do PMS, liberando mais espécies reativas de oxigênio
(SO4•- e •OH) no meio reacional, de modo a degradar o glifosato logo nos minutos
iniciais de reação, similarmente ao reportado por (DUNG et al., 2023; DUNG et
al., 2021; LI et al., 2023). O pH inicial da reação (4) favoreceu a redução do
catalisador (Fe0 a Fe2+), sendo liberado no meio para ativar o PMS sob condições
ácidas e assim, degradar o glifosato (XIAO et al., 2021). Por outro lado, o pH
alcalino inibe a formação do íon Fe2+, impedindo assim, a ativação do PMS e a
consequente degradação do glifosato. A Figura 1 (d) reporta o ensaio III, cujo o
decaimento da absorbância pode ser notado visivelmente, devido a solução
cromogênica utilizada para dar cor a reação.

Condições para realização do planejamento \r\nexperimental
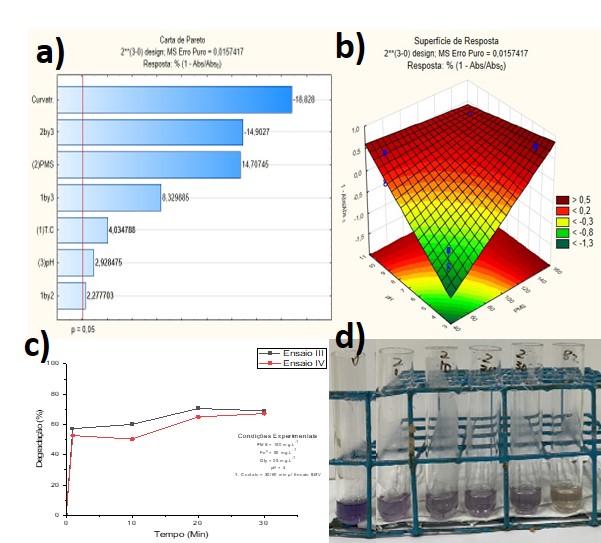
a) Carta de Pareto; b) Superfície de resposta; c); e \r\nd) Eficiência de degradação no Ensaio III e IV, e; \r\nd) Decaimento da absorbância pelo tempo.
Conclusões
Com base nos experimentos realizados, pode-se concluir que após os ajustes experimentais, o sistema de tratamento demonstrou eficácia na degradação do glifosato, indicando a influência significativa do PMS e interação com o pH no planejamento fatorial. Além disso, o catalisador (Fe0) e o agente oxidante PMS atuando em sinergia, tendo também, o pH ácido como um fator chave para a otimização do processo, proporcionou um alcance de 70% de degradação do herbicida glifosato. Os resultados respaldam a aplicação desse sistema como um método promissor para a remoção do herbicida em questão.
Agradecimentos
“O presente trabalho foi realizado com apoio da Coordenação de Aperfeiçoamento de Pessoal de Nível Superior – Brasil (CAPES) – Código de Financiamento 001”. À FAPERJ.
Referências
BRASIL. Projeções do Agronegócio: Brasil 2020/21 a 2030/31: projeções de longo prazo. Ministério da Agricultura, Pecuária e Abastecimento - MAPA, Brasília, DF, 2021.
BRASIL. Agropecuária Brasileira em Números. Ministério da Agricultura, Pecuária e Abastecimento - MAPA, Brasília, DF, 2022.
CHAUHAN, Bhagirath Singh. Grand challenges in weed management. Frontiers in Agronomy, [s. l.], v. 1, 2020. ISSN: 2673-3218.
DUAN, P., PAN, J., DU, W., et al. Activation of peroxymonosulfate via medi- ated electron transfer mechanism on single-atom Fe catalyst for effective organic pollutants removal. Applied Catalysis B: Environmental, [s. l.], v. 299, pp. 120714, 2021. ISSN: 0926-3373.
DUNG, N. T., HANH, P. T. H., THAO, V. D., et al. Decomposition and mineraliza-
tion of glyphosate herbicide in water by radical and non-radical pathways
through peroxymonosulfate activation using Co3O4/g-C3N4: a comprehen-
sive study. Environ. Sci.: Water Res. Technol., [s. l.], v. 9, pp. 221–234, 2023.
DUNG, N. T., THAO, V. D., HUY, N. N. Decomposition of glyphosate in water by peroxymonosulfate activated with CuCoFe-LDH material. Vietnam Journal of Chemistry, [s. l.], v. 59, n. 6, pp. 813–822, 2021.
GUPTA, P. K. Chapter 37 - Herbicides and Fungicides. In: Gupta, R. C. (Ed.), reproductive and Developmental Toxicology (Second Edition), second edition ed., Academic Press, [s. l.], pp. 657–679, 2017. ISBN:978-0-12-804239-7.
HASANUZZAMAN, M., MOHSIN, S. M., BHUYAN, M. B., et al. Chapter 3 - Phytotoxicity, environmental and health hazards of herbicides: challenges 12 and ways forward. In: Prasad, M. N. V. (Ed.), Agrochemicals Detection, Treatment and Remediation, Butterworth-Heinemann, [s. l.], pp. 55–99, 2020. ISBN: 978-0-08-103017-2.
HAZARAIMI, M., GOH, P., LAU, W., et al. The state-of-the-art development of photocatalysts for the degradation of persistent herbicides in wastewater. Science of The Total Environment, [s. l.], v. 843, pp. 156975, 2022. ISSN: 0048-9697.
HERINGER, Andreia Azevedo. Degradação do Herbicida Glifosato por Processo Oxidativo Avançado H₂O₂/UV. Dissertação (Mestrado em Engenharia de Processos Químicos e Bioquímicos) – Escola de Química, Universidade Federal do Rio de Janeiro, Rio de Janeiro, 2019.
JYOTHI, M., NAGARAJAN, V., CHANDIRAMOULI, R. Chemisorption of atrazine and diuron molecules on -arsenene nanosheet - a first- principles study. Chemical Physics Letters, [s. l.], v. 794, pp. 139484, 2022. ISSN: 0009-2614.
LI, J., NI, Z., GAO, Q., et al. Core-shell structured cobalt–nickel bimetallic sulfide with dual redox cycles to activate peroxymonosulfate for glyphosate removal. Chemical Engineering Journal, [s. l.], v. 453, pp. 139972, 2023. ISSN: 1385-8947.
LIMA, T. CAPÍTULO 2–ODS 2 Acabar com a fome, alcançar a segurança alimentar e melhoria da nutrição e promover a agricultura sustentável. Os objetivos de desenvolvimento sustentável e as relações internacionais, [s. l.], p. 43, 2019.
NAGARAJA, P.; BHASKARA, B. L. Sensitive spectrophotometric assessment of carbofuran using dapsone as a new chromogenic reagent in formulations and environmental samples. Ecletica Quimica, [s. l.], v. 31, n. 4, p. 43–48, 2006.
NORTOX. GLIFOSATO NORTOX SL. Arapongas - PR: Nortox S/A, Brasil, 2021.
RASTOGI, A., AL-ABED, S. R., DIONYSIOU, D. D. Sulfate radical-based fer-rous–peroxymonosulfate oxidative system for PCBs degradation in aqueous and sediment systems. Applied Catalysis B: Environmental, [s. l.], v. 85, n. 3, pp. 171–179, 2009. ISSN: 0926-3373.
RAWTANI, D., KHATRI, N., TYAGI, S., et al. Nanotechnology-based recent approaches for sensing and remediation of pesticides. Journal of Environmental Management, [s. l.], v. 206, pp. 749–762, 2018. ISSN: 0301-4797.
SALOMÃO, P. E. A., FERRO, A. M. S., RUAS, W. F. Herbicidas no Brasil: uma breve revisão. Research, Society and Development, [s. l.], v. 9, n. 2, pp. e32921990–e32921990, 2020.
SPRINGMANN, M., CLARK, M., MASON-D’CROZ, D., et al. Options for
keeping the food system within environmental limits. Nature, [s. l.], v. 562, n.
7728, pp. 519 – 525, 2018.
SYNGENTA. TOUCHDOWN. São Paulo - SP, Brasil, 2022.
VILLETTE, S., MAILLOT, T., GUILLEMIN, J.-P., et al. Assessment of nozzle control strategies in weed spot spraying to reduce herbicide use and avoid under- or over-application. Biosystems Engineering, [s. l.], v. 219, pp. 68–84, 2022. ISSN: 1537-5110.
WANG, J., WANG, S. Activation of persulfate (PS) and peroxymonosulfate (PMS) and application for the degradation of emerging contaminants. Chemical Engineering Journal, [s. l.], v. 334, pp. 1502–1517,
2018. ISSN: 1385-8947.
WONG, A. C. S., MASSEL, K., LAM, Y., et al. Biotechnological Road Map for Innovative Weed Management. Frontiers in Plant Science, [s. l.], v. 13, 2022. ISSN: 1664-462X.
XIAO, Y., LIU, X., HUANG, Y., et al. Roles of hydroxyl and carbonate radicals in bisphenol a degradation via a nanoscale zero-valent iron/percarbonate system: influencing factors and mechanisms. RSC Adv., [s. l.], v. 11, pp. 3636–3644, 2021.
YANG, L., XIONG, Z., LI, J., et al. Iron active sites encapsulated in N-doped grafite for efficiently selective degradation of emerging contaminants via peroxy-monosulfate (PMS) activation: Inherent roles of adsorption and electron-transfer dominated nonradical mechanisms. Chemical Engineering Journal, [s. l.], v. 444, pp. 136623, 2022. ISSN: 1385-8947.