ÁREA
Química Analítica
Autores
dos Santos, E. (NUPAM UFBA) ; Santos, M.P. (NUPAM UFBA) ; Santos, S. (NUPAM UFBA) ; Cazedey, E.C. (NUPAM UFBA) ; Wingert, N. (NUPAM UFBA)
RESUMO
Os antirretrovirais fumarato de tenofovir desoproxila (TDF) e entricitabina (FTC) fazem parte do esquema de prevenção da soroconversão para o HIV. Como ferramenta para controle de qualidade, a espectrofotometria UV derivada (ED), permite analisar medicamentos multicomponentes, através da derivação matemática dos valores de absorvância na região do UV. O objetivo do trabalho foi desenvolver e validar um método por ED para análise simultânea de TDF e FTC em comprimidos, visando o controle de qualidade farmacêutico. Foram usados de solventes de menor toxicidade: água e etanol). Foi obtido o ponto de anulação (zero crossing) para o TDF em 2ª derivada e para o FTC em 1ª derivada. O método apresentou linearidade, seletividade, precisão, exatidão e robustez para ambos os fármacos analisados.
Palavras Chaves
PrEP; Espectrofotometria deriva; Química verde
Introdução
A associação dos fármacos fumarato de tenofovir desoproxila (TDF) e entricitabina (FTC) é utilizado tanto no tratamento quanto na prevenção da soroconversão para o HIV, distribuído em território nacional pelo SUS no protocolo de profilaxia pré-exposição ao HIV (PrEP). Essas moléculas possuem atuam inibindo a enzima transcriptase reversa do HIV-1. Para garantir a qualidade deste medicamento, é necessária a realização de ensaios qualitativos e quantitativos para avalição das características físico-químicas, como dureza, dissolução, pureza, teor. A técnica de espectrofotometria no ultravioleta (UV) tem ampla aplicação na indústria farmacêutica para identificação e quantificação, devido à capacidade de muitos fármacos absorverem luz entre 200 – 400 nm, além de ser uma técnica simples, sensível, confiável e com baixo consumo de solventes. Para formulações multicomponentes, com fármacos em associação, a análises por espectrofotometria-UV torna-se desafiadora, devido a sua falta de seletividade. A aplicação da derivação matemática é especialmente útil para detectar compostos sobrepostos de bandas espectrais, como FTC e TDF. Alinhado aos princípios da química verde e da busca por inovação na indústria de controle de qualidade farmacêutico, o presente trabalho desenvolveu um método para análise simultânea de TDF e FTC por espectrofotometria derivada, sendo validado de acordo com as normativas da Anvisa e do Inmetro.
Material e métodos
O desenvolvimento e a validação do método foram executados no laboratório Núcleo de Pesquisa e Análises de Medicamentos (NuPAM), na Universidade Federal da Bahia. As substâncias químicas de referência (SQR) de TDF e FTC foram produzidas pela Nortec Química (RJ, Brasil), com teores equivalentes a 98,5% e 101,0%, respectivamente. Os comprimidos de TDF 300 mg + FTC 200 mg foram gentilmente doados pelo setor de Farmácia do Hospital Universitário Prof. Edgard Santos, com fabricação pela Blanver Farmacêutica e distribuição para o SUS pela fundação Oswaldo Cruz. Todos os solventes utilizados foram de grau analítico, e a água purificada por sistema de osmose reversa Permution (PR, Brasil). No preparo das amostras foram utilizadas balança analítica da Bioprecisa (PR, Brasil), banho ultrassônico Solidsteel (SP, Brasil) e micropipetas automáticas da marca Eppendorf® (Alemanha). As análises foram realizadas no Espectrofotômetro Spercord 200 – plus da marca Analytik Jena (Jena, Alemanha), com cubetas de quartzo de 1 cm. As soluções estoque de SQR e comprimidos foram preparadas em etanol, na concentração de 500 μg/mL, com posterior diluição até a concentração de trabalho com água purificada. O método foi validado seguindo a RDC 166 (2017) e o Inmetro (2020).
Resultado e discussão
Os trabalhos publicados para quantificação de TDF/FTC utilizam ACN
como principal solvente. Para aplicação da química verde, foram testados
solventes menos tóxicos: água purificada, etanol e metanol. Ambos os fármacos
são hidrossolúveis, assim como alguns excipientes, levando a interferências
adicionais na análise. Dessa forma, o etanol foi selecionado como solvente
inicial da forma farmacêutica, seguido por água purificada como diluente. As
moléculas apresentam variações nas taxas de absorção em diferentes comprimentos
de onda, fornecendo informações cruciais para a diferenciação e quantificação
dos fármacos e obtenção dos pontos de anulação. A partir de diferentes
velocidades de varredura e aplicação de derivações com incremento de delta
lambda (Δλ) e suavizações, foi possível encontrar pontos de anulação para a
absorbância de ambos os fármacos. As quantificações foram feitas na velocidade
de varredura 100 nm/s e Δλ=10, aplicando 2ª derivada e suavização (TDF) e 1ª
derivada sem suavização (FTC), conforme espectros das figuras 1 e 2. Respeitando
a lei de Beer-Lambert, as concentrações de trabalho foram TDF 40 µg/mL e FTC
26,67 µg/mL, seguindo a proporção do produto acabado (TDF 300 mg e FTC 200 mg).
O intervalo de linearidade foi estabelecido entre 80% - 120% das concentrações
de trabalho. O método apresentou regressão linear significativa (r>0,99), sem
desvio da linearidade e com valores homocedásticos (teste de Cochran). O desvio
padrão relativo foi <5% para precisão intermediária, e a recuperação dentro da
faixa de 80 – 110%. A robustez do método foi verificada frente a variações nos
solventes. Dessa forma, pode ser afirmado que o método desenvolvido é linear,
seletivo, preciso, exato e robusto para determinação simultânea de TDF e FTC em
comprimidos.
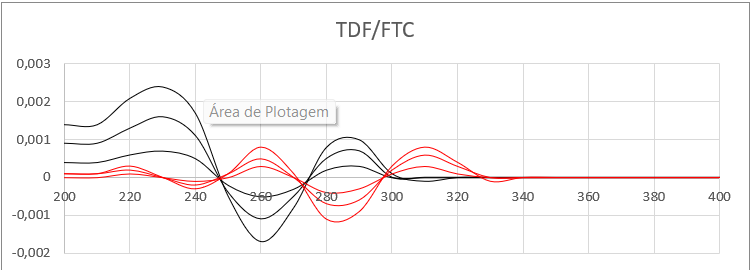
Espectro do TDF/FTC em 2ª derivada, para \r\nquantificação do TDF.
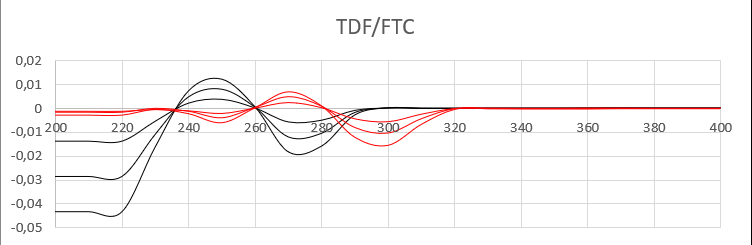
Espectro de TDF/FTC em 1ª derivada, para \r\nquantificação de FTC.
Conclusões
Apresentou-se o desenvolvimento e validação de um método inovador, capaz de quantificar TDF e FTC em associação, e aplicável à rotina de controle da qualidade de comprimidos do antirretrovirais. A técnica de espectrofotometria derivada e os solventes etanol e água foram utilizados, mostrando assim alinhamento com as práticas da química verde. Essa abordagem de controle de qualidade de medicamentos eleva a segurança dos medicamentos para os pacientes e a população em geral e reforça a responsabilidade ambiental da indústria farmacêutica.
Agradecimentos
Ao NuPAM da UFBA pela estrutura de laboratório. Ao CNPq pela bolsa de iniciação científica. À FAPESB pelos recursos para a execução do projeto (TO SUS0012/2021).
Referências
AOAC international., official methods of analysis of AOAC international, in guidelines for Standard Method Performance Requirements (Appendix F), 2012.
BRASIL. Agência Nacional de Vigilância Sanitária – RDC n° 166, de 2017.
BRASIL. Farmacopeia Brasileira, vol.1. 6ª ed, 2019.
DONATO, Eliane Maria et al. Espectrofotometria derivada: uma contribuição prática para o desenvolvimento de métodos. Revista de ciências farmacêuticas: básicas e aplicadas. v. 31, p. 125-130, 2010.
INMETRO: Orientações sobre validação de métodos analíticos. Inmetro. Rio de Janeiro, agosto 2016.