ÁREA
Química Analítica
Autores
Moraes, M. (INT/IFRJ) ; Rodrígues, P. (INT) ; Costa, L. (INT) ; Oliveira, P. (INT) ; Gaspar, A. (INT) ; Rodrigues, C. (INT) ; Oliveira, F. (INT/IME) ; Francisco, T. (INT/UFRJ)
RESUMO
Neste estudo foi realizada a síntese e a avaliação da quantidade de etilenodiamina (EDA) durante a funcionalização do óxido de grafeno (GO) visando a captura de CO2. A síntese do GO foi realizada pelo método de Hummers modificado e depois foi funcionalizado com EDA. A análise dos difratogramas de raios X indicaram aumento da distância interplanar devido a entrada de moléculas de EDA. A análise dos espectros na região do infravermelho mostrou bandas nitrogenadas, o que sugere a presença de EDA na estrutura do GO. No entanto, somente a amostra GOEDA0,5 apresentou bandas em aproximadamente 2.920 e 2.860 cm-1, características de CH2 que está presente na estrutura do EDA, e maior aumento da distância entre camadas, sendo considerada a melhor condição de funcionalização.
Palavras Chaves
Óxido de grafeno ; CO2; Etilenodiamina
Introdução
A emissão de CO2 nos últimos anos tem aumentado exponencialmente, chegando em torno de 37 bilhões de toneladas em 2021, sendo considerada uma das causas das mudanças climáticas (FRIEDLINGSTEIN et al., 2022). As principais fontes de emissão de CO2 são atividades antropogênicas como: geração de energia pela queima de combustíveis fosseis (carvão e gás natural), transporte, construção (produção de cimento) e agricultura (RITCHIE et al., 2020). De acordo com o IPCC de 2005, uma das formas de reduzir a emissão de CO2 de fonte pontual, à médio prazo, é por meio da tecnologia de captura e armazenamento, que consiste em capturar o CO2 emitido e armazenar em reservatório geológico. O processo de captura envolve a etapa de separação do CO2 da mistura gasosa, sendo a técnica de absorção líquida usada comercialmente por ser simples, apresentar alta seletividade e eficiência de captura. No entanto, seu alto custo de regeneração do solvente contribui para a busca de novas tecnologias como a utilização de adsorvente sólidos mais eficientes (METZ et al., 2005). Entre as vantagens de utilizar um adsorvente sólido podem ser citadas a formação de interações físicas fracas com CO2 e a facilidade de regeneração seja por alteração na pressão de operação ou na temperatura. Para selecionar bons adsorventes, os sólidos devem apresentar as seguintes características: alta área superficial, larga estrutura de poros e alta seletividade. Recentemente, o grafeno vem se destacando como material adsorvente devido as suas propriedades. Ele é um material bidimensional que consiste em monocamada de átomos de carbono organizados em uma rede hexagonal, no qual todos os carbonos contêm dupla ligação. Esta característica proporciona propriedades interessantes para o grafeno como alta condutividade térmica a 25°C (5.000 W m-1 K-1) e elétrica (2. 104 S cm-1), mobilidade eletrônica (2. 105 cm2 V-1 s-1), alta área superficial específica teórica (2.600 m2 g-1) e boa resistência mecânica com resistência a tração de 130 GPa e módulo de Young de 1TPa (BALASUBRAMANIAN et al., 2015; VIEIRA SEGUNDO; VILAR, 2016). O óxido de grafeno é a forma oxidada do grafeno. Este composto apresenta estrutura carbônica hexagonal similar ao grafeno, se diferenciando deste por possuir grupos funcionais como hidroxila (-OH), epóxi (-O-) e carboxila (-COOH), o que lhe confere propriedade hidrofílica e possibilidade de funcionalização da superfície. Esses grupos funcionais são descritos como sítios ativos uma vez que em água sofrem ionização, ficando com carga superficial negativa. Isso possibilita a sua interação eletrostática com moléculas catiônicas, como também, podem interagir por meio de interação dipolo-dipolo e dipolo momentâneo. (PENG et al., 2017; DESHWAL et al., 2023). Estudos recentes mostram que óxido de grafeno funcionalizado com aminas tem potencial para aplicação na adsorção de CO2 (PRUNA et al., 2019; ZHOU et al., 2019). No entanto, as pesquisas foram feitas em baixa escala, com baixo rendimento de reação de aprox. 20%, sendo necessário o aumento de escala do processo (COELHO, 2016, XUE et al., 2015). Com base no que foi exposto, este trabalho tem como objetivo: (i) a síntese do óxido de grafeno e (ii) o estudo da quantidade de etilenodiamina para a funcionalização do óxido de grafeno em maior escala, visando sua aplicação na captura de CO2
Material e métodos
Reagentes Grafite (Grafine 996100, fornecido pela Nacional de Grafite), ácido sulfúrico (H2SO499%), permanganato de potássio (KMnO499%, sigma aldrich), peróxido de hidrogênio (H2O235%, sigma aldrich), etilenodiamina (EDA 99%, sigma aldrich). Síntese óxido de grafeno O óxido de grafeno foi sintetizado pelo Método de Hummers modificado (BENEVIDES et al., 2020). Em um balão de fundo redondo foi adicionado 0,5 g de grafite, 28,75 mL de H2SO4 concentrado em pequenas porções e 3,75 g KMnO4 em pequenas porções sob agitação magnética e temperatura em torno de 10 °C. Em seguida, aumentou a temperatura para 35 ºC por 3 h. Após esse tempo, foi feita a adição de 200 mL de água destilada gelada em pequenas porções e controlando a temperatura para não ultrapassar 100 °C. Posteriormente, a reação foi submetida a temperatura de 90 ºC por 15 minutos. Após esse tempo, suspendeu o aquecimento e resfriou a reação para 20 °C, em seguida, foi adicionado 150 mL de H2O210% e deixou em agitação magnética por 30 minutos. No dia seguinte, foi realizada três lavagens, com 100 mL de solução de H2O210% e H2SO45% (1:1), em centrifuga a 3.000 rpm por 10 minutos. Posteriormente, foi feita lavagem com água destilada até alcançar pH ≈ 5. Após lavagem, a amostra foi seca em estufa a 50 °C. Funcionalização óxido de grafeno Foi feita funcionalização do GO com etilenodiamina(EDA) sob refluxo em banho de óleo de silicone a temperatura de 33°C (COELHO, 2016 e XUE et al., 2015). Para isso, foi adicionado em um balão de fundo redondo 400 mg de GO e 200 mL de água destilada, previamente disperso em ultrassom por 30 minutos, o volume de EDA foi adicionado gota a gota, e mantido sob agitação magnética por 4 horas. Posteriormente, o sólido foi lavado em centrifuga (5.000 rpm, 10 minutos) com água destilada até pH = 5 e seco em estufa a 50 °C. A funcionalização foi realizada com 0,1; 0,25 e 0,5 mL de EDA, sendo as amostras denominadas GOEDA0,1, GOEDA0,25 e GOEDA0,5, respectivamente. Caracterização das amostras As amostras foram caracterizadas utilizando as técnicas a seguir. Difração de raios X (DRX), usando um difratômetro da marca Bruker D8 Advance, radiação Cu- Kα, (λCu: 0,154 nm) com voltagem de 30 kV e corrente de 30 A. A análise foi realizada no intervalo de ângulo de Bragg (2θ) entre 5º e 50º, com passo de 0,05º e tempo de 2s. Espectroscopia na região do infravermelho com transformada de Fourier (FTIR), utilizando um espectrômetro PerkinElmer FT-IR/FIR Frontier, por reflectância sobre o cristal de diamante, na faixa de 4.000 a 600 cm 1 e com resolução de 4 cm min-1. Microscopia eletrônica de varredura (MEV) em um equipamento de modelo FEI Quanta FEG 450. As amostras foram dispersas em etanol e depositadas com auxílio de pipeta na placa de silício e metalizadas com platina utilizando o equipamento K550X Sputter com corrente de 20 mA e tempo de recobrimento de 2 min. Detalhes sobre as condições de operação para a aquisição das imagens, tais como tamanho de spot, distância de trabalho, bem como sobre as ampliações das regiões observadas estão disponíveis na barra de escala das micrografias apresentadas.
Resultado e discussão
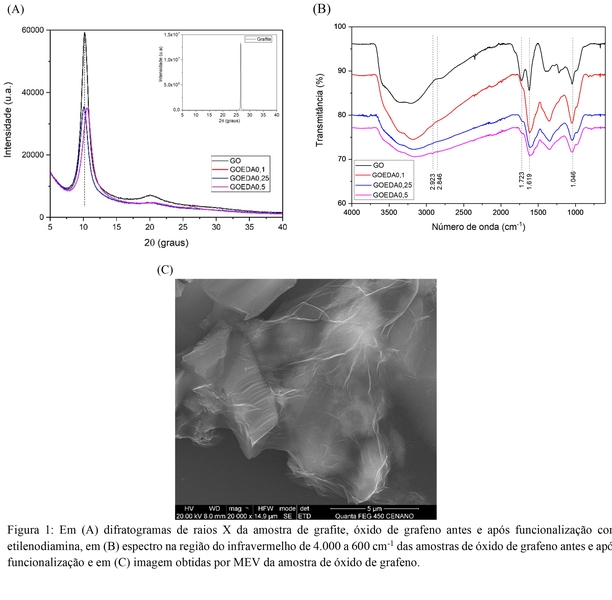
A técnica difração de raios X foi utilizada para obter informações sobre a
estrutura cristalina do grafite e do óxido de grafeno. Pode-se notar que o
grafite apresenta pico em 26,6° (2θ) referente ao plano 002 e, após a realização
do método de Hummers, nota-se no difratograma da amostra de GO um deslocamento
do pico para o ângulo 10,2° (Figura 1(A)), indicando a formação de grupos
oxigenados ao longo da rede do grafite, que de acordo com o a Lei de Bragg
(Equação 1)aumenta a sua distância interplanar, confirmando assim que houve a
esfoliação e oxigenação do grafite (REN et al., 2023; YU et al., 2015).
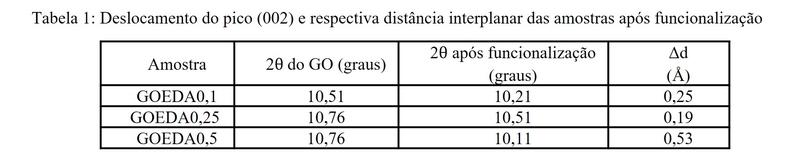
Após a funcionalização com EDA nota-se para todas as amostras o deslocamento do
pico para a ângulos menores, o que representou um aumento da distância
interplanar de 0,25 (GOEDA0,1); 0,19 (GOEDA0,25) e 0,53 (GOEDA0,5) Å (Tabela 1).
Isso ocorre pela entrada de moléculas de EDA no espaço interlamelar do GO,
contribuindo para o afastamento das camadas de carbono e aumentando o
espaçamento entre elas. (XUE et al., 2015).
nλ= 2dsenθ Equação 1
Onde:
n: número natural (n =1)
d:distância interplanar
λ: comprimento de onda da radiação (λCu: 0,154 nm)
θ:ângulo de incidência
A partir dos resultados obtidos por espectroscopia na região do infravermelho
com transformada de Fourier foi possível observar os seguintes aspectos: (i) se
as bandas características dos grupos funcionais oxigenados estavam presentes no
GO sintetizado e (ii) se após a funcionalização do GO ocorreu o aparecimento de
bandas próprias dos grupos funcionais nitrogenados de amina.
Na Figura 1(B) é apresentado o espectro da amostra de GO, na qual pode-se
observar a presença das bandas com deslocamentos de 3.590, 3.370, 3.200 e 2.800
cm-1 características de estiramento vibracional do grupo hidroxila (-OH) e de
água interlamelar (JOSHI et al., 2023 e YAN et al., 2012). Bandas com
deslocamentos em 1.728, 1.622 e 1.048 cm-1 são atribuídas a estiramento
vibracional de ligação C=O em grupos carbonila ou carboxila (15), C=C (JOSHI et
al., 2023 e YAN et al., 2012) e C-O (YU et al., 2023), respectivamente. As
bandas com deslocamento em 1.222 e 1.048 cm-1 são características de estiramento
vibracional C-O-C de grupo epóxi e C-O, respectivamente (Figura 1(B)) (YU et
al., 2023; USCA et al.,2019; PRUNA et al., 2020). O aparecimento dessas bandas
de grupos funcionais oxigenados, hidroxila, carbonila e de grupo etóxi,
confirmam o sucesso da síntese do óxido de grafeno.
Após a funcionalização do GO, notamos no espectro de FTIR da Figura 1(B) o
aparecimento da banda com deslocamento em 1.631 cm-1 devido a sobreposição das
bandas C-N e C=C, e que está de acordo com o que foi observado nos estudos de
Zhang e col. (2018).
Nos espectros da amostra GOEDA0,5 apareceram as bandas com deslocamento em 2.920
e 2.860 cm-1 características de deformação axial simétrica e assimétrica de
carbono secundário, respectivamente, presente na estrutura do EDA (SILVERTEIN et
al., 1979). Após a funcionalização houve a diminuição das bandas referentes ao
grupo carbonila ou carboxila (1.029 cm-1) e o desaparecimento das bandas
características de grupo epóxi (1.154 e 870 cm-1) (ERSHADI et al., 2019). Esses
resultados corroboram com o DRX e confirma a presença de EDA na estrutura do GO.
A microscopia eletrônica de varredura foi realizada para avaliar a morfologia do
óxido de grafeno. Na Figura 1C mostra a imagem obtida da amostra de GO, na qual
é possível observar a presença de rugas que são atribuídas à interação dos
grupos oxigenados presentes nas suas folhas. Esse resultado está de acordo com o
DRX e FTIR e comprova que o GO foi formado com sucesso, uma vez que esta é a sua
morfologia característica (BENEVIDES et al., 2020; GONÇAVES et al., 2020).
Conclusões
Pelo estudo de funcionalização do óxido de grafeno com diferentes quantidades etilenodiamina, por meio de um método simples, foi possível aumentar a escala de produção, o que é promissor para aplicação na captura de CO2. O óxido de grafeno obtido pelo método de Hummers modificado foi caracterizado por difração de raios X, espectroscopia vibracional na região do infravermelho e microscopia eletrônica por varredura, que corroboraram com a presença de óxido de grafeno no produto. Após funcionalização, as técnicas de caracterização indicaram a presença de EDA no espaço interlamelar do GO e na estrutura, sendo a amostra GOEDA0,5 a que apresentou maior aumento da distância entre camadas e presença de bandas em 2.920 e 2.860 cm-1, logo foi a melhor condição de funcionalização.
Agradecimentos
Ao CNPq, a FAPERJ e ao FINEP pelo apoio financeiro. Ao CENANO pelas análises de MEV. A UERJ pela análise de FTIR.
Referências
1. A. P. BENEVIDES; A. R. CAMPOS; L. C. VIEIRA; C. dos R. PEREZ; D. V. CESAR, MaterialsResearch 2020, 1, 23, 1-9.
2. B. XUE; J. ZHU; N. LIU; Y. LI, Catalysis Communications 2015, 64, 105-109.
3. COELHO, Carolina Bispo de Sousa. Obtenção e caracterização de óxido de grafeno funcionalizado com aminas com potencial aplicação na captura de CO2. Niterói, RJ, Trabalho de Conclusão de Curso (Bacharelado em Química) – Universidade Federal Fluminense, 2016. 35f.
4. DESHWAL, Nidhi et al. A review on recent advancements on removal of harmful metal/metal ions using graphene oxide: Experimental and theoretical approaches. Science of The Total Environment, v. 858, p. 159672, 2023.
5. FRIEDLINGSTEIN, Pierre et al. Global carbon budget 2021. Earth System Science Data, v. 14, n. 4, p. 1917-2005, 2022.
6. GONÇALVES, Arthur HA et al. Synthesis of a magnetic Fe3O4/RGO composite for the rapid photo-Fenton discoloration of indigo carmine dye. Topics in Catalysis, v. 63, p. 1017-1029, 2020.
7. JOSHI, Rita et al. Green reduction of graphene oxide as a substitute of acidic reducing agents for supercapacitor applications. Materials Science and Engineering: B, v. 287, p. 116128, 2023.
8. METZ, Bert et al. IPCC special report on carbon dioxide capture and storage. Cambridge: Cambridge University Press, 2005.R. Balasubramanian; S. Chowdhury, Journal of Materials Chemistry A 2015, 4, 1-76.
9. MIN, Kyoungho et al. A facile route to fabricate stable reduced graphene oxide dispersions in various media and their transparent conductive thin films. Journal of colloid and interface science, v. 383, n. 1, p. 36-42, 2012.
10. PENG, Weijun et al. A review on heavy metal ions adsorption from water by graphene oxide and its composites. Journal of Molecular Liquids, v. 230, p. 496-504, 2017.
11. PRUNA, A. et al. Effect of synthesis conditions on CO2 capture of ethylenediamine-modified graphene aerogels. Applied Surface Science, v. 487, p. 228-235, 2019.
12. PRUNA, Alina I. et al. Effect of varying amine functionalities on CO2 capture of carboxylated graphene oxide-based cryogels. Nanomaterials, v. 10, n. 8, p. 1446, 2020.
13. REN, Zhijie et al. Green synthesis of reduced graphene oxide/chitosan/gold nanoparticles composites and their catalytic activity for reduction of 4-nitrophenol. International Journal of Biological Macromolecules, v. 229, p. 732-745, 2023.
14. RITCHIE, Hannah; ROSER, Max; ROSADO, Pablo. CO₂ and greenhouse gas emissions. Our world in data, 2020.
15. SEGUNDO, J. E. D. V.; VILAR, Eudésio Oliveira. Grafeno: Uma revisão sobre propriedades, mecanismos de produção e potenciais aplicações em sistemas energéticos. Revista Eletrônica de Materiais e Processos, v. 11, n. 2, p. 54-57, 2016.
16. USCA, G. et al. Preparation of graphene oxide as biomaterials for drug adsorption. In: AIP Conference Proceedings. American Institute of Physics, 2015. p. 79-86.
17. YAN, Jia-lin et al. Functionalized graphene oxide with ethylenediamine and 1, 6-hexanediamine. New Carbon Materials, v. 27, n. 5, p. 370-376, 2012.
18. YU, Jing et al. Ethylenediamine-oxidized sodium alginate hydrogel cross-linked graphene oxide nanofiltration membrane with self-healing property for efficient dye separation. Journal of Membrane Science, v. 670, p. 121366, 2023.
19. ZHOU, Fanglei et al. Ultrathin, ethylenediamine-functionalized graphene oxide membranes on hollow fibers for CO2 capture. Journal of Membrane Science, v. 573, p. 184-191, 2019.