ÁREA
Química Analítica
Autores
Valeriano, M.C. (UFABC) ; Mamián-lópez, M.B. (UFABC) ; Batista, A.C.F. (UFU)
RESUMO
Um dos parâmetros mais relevantes para manter o controle de qualidade do biodiesel é a estabilidade oxidativa. O controle do grau de oxidação no biodiesel é essencial, pois produtos indesejáveis, como sedimentos, polímeros ou ácidos graxos de cadeia curta, podem ser formados. Neste trabalho, uma metodologia utilizando a espectroscopia Raman aliada à regressão de Mínimos Quadrados Parciais (PLS) foi desenvolvida para avaliar a estabilidade oxidativa do biodiesel de soja através de seu tempo de indução. Com isso, foram alcançados valores de RMSEC e RMSEP de 0,26 e 0,30 h, respectivamente. Esses resultados foram significativamente menores do que os relatados para o método padrão, Rancimat (0,5 h), mostrando que a metodologia é promissora e pode ser facilmente adaptada para análises de rotina.
Palavras Chaves
Biodiesel; Espectroscopia Raman; Quimiometria
Introdução
Buscando formas de substituir os combustíveis fósseis por fontes de energia mais limpas, o biodiesel surge como uma alternativa eficiente. Com propriedades semelhantes ao diesel, o biodiesel é menos poluente, produz menos gases de efeito estufa, não contém enxofre, proporciona maior lubrificação do motor, e sua matéria prima é abundante (MAAWA et al., 2020; SUBRAMANIAM; MASRON; AZMAN, 2020). A legislação brasileira prevê até o ano 2026 o percentual 15% de biodiesel em amostras de diesel comerciais (MINISTÉRIO DE MINAS E ENERGIA, 2023). Comumente, o biodiesel é produzido através da transesterificação do óleo na presença de um álcool e um catalisador alcalino. Apesar de ter características semelhantes, o biodiesel tende a ser menos estável que o diesel (LÔBO; FERREIRA; CRUZ, 2009). Parâmetros como teor de água, índice de iodo e estabilidade oxidativa devem ser monitorados antes da entrega do produto ao consumidor final para manter a integridade do motor. A estabilidade oxidativa está relacionada à tendência do biodiesel de oxidar na presença de oxigênio à temperatura ambiente. Isso pode levar à formação de sedimentos, polímeros insolúveis, ácidos graxos de cadeia curta e outras substâncias (PULLEN; SAEED, 2012). O método EN 14112 (2020) define o método Rancimat como padrão para determinar a estabilidade oxidativa do biodiesel (CEN, 2020), e está baseado na oxidação acelerada das amostras por aumento da temperatura a um caudal constante e ar (110 °C e 10 L h-1, respetivamente, conforme definido pela EN 14112). O parâmetro que descreve quantitativamente a estabilidade oxidativa é o tempo de indução da amostra em horas, ou seja, quando há um aumento súbito da condutividade causado pela liberação de compostos voláteis gerados pelo processo de oxidação (PULLEN; SAEED, 2012). No entanto, uma análise Rancimat típica é um processo lento que pode levar várias horas para ser realizado, o que é desvantajoso para análises de rotina. Nesse sentido, métodos espectroscópicos como UV-vis (ZHOU et al., 2017; SOARES; ROCHA, 2020) e infravermelho (BAPTISTA et al., 2008b, 2008a; DE LIRA et al., 2010a, 2010b; BALABIN; SAFIEVA, 2011; ALVES; POPPI, 2013) têm se mostrado como alternativas para a determinação de parâmetros de qualidade do biodiesel, e estudar mudanças estruturais neste tipo de amostra. Dentre essas técnicas espectroscópicas, a espectroscopia Raman oferece vantagens muito atrativas, como a rápida aquisição de espectros, ausência de interferência devido à presença de água para uma ampla faixa espectral, grande quantidade de informações estruturais, entre outras. Esta técnica mede o espalhamento inelástico da radiação, quando interage com a matéria, trazendo informações estruturais de uma dada espécie química através de seus modos vibracionais (MIRANDA et al., 2014; LIU et al., 2019). No entanto, a interpretação e extração de informações quantitativas de um conjunto de dados de espectros Raman não é tão simples, especialmente em análise de rotina, onde decisões rápidas são necessárias, como por exemplo em rotinas de controle de qualidade ou em processos industriais, para citar alguns casos. As aplicações atuais se beneficiaram significativamente de métodos de aprendizado de máquina e mineração de dados aplicados a dados químicos, também conhecidos como quimiometria, como uma maneira mais rápida de processar dados de sinais complexos, como aqueles provenientes de medições espectroscópicas (KUMAR et al., 2014). Essas abordagens também permitem o desenvolvimento de aplicações mais simples e de baixo custo, bem como a identificação de amostras anômalas ou outliers. Pela natureza dos sinais Raman, mudanças estruturais em nível molecular também podem ser avaliadas (WOLD; ESBENSEN; GELADI, 1987). Modelos quantitativos também podem ser construídos onde os sinais são processados contra uma dada propriedade quantitativa (geralmente concentração), mesmo na presença de possíveis interferências, conhecidas ou desconhecidas. Isso é possível, por exemplo, usando a regressão de Mínimos Quadrados Parciais (PLS), um método que correlaciona as variáveis latentes, que são combinações lineares das variáveis independentes, com uma matriz ou vetor de referência. Além disso, o método PLS tem a vantagem de resolver problemas de multicolinearidade (HÖSKULDSSON, 1988; WOLD; SJÖSTRÖM; ERIKSSON, 2001), e pode prever uma propriedade quantitativa de um analito em uma matriz analítica multicomponente. Neste trabalho, combinamos os espectros Raman com a análise multivariada para desenvolver uma metodologia rápida e nova para avaliar quantitativamente o tempo de indução em biodiesel. Até onde mostram as pesquisas nas bases de dados, este trabalho apresenta pela primeira vez uma metodologia baseada em Raman para quantificar a estabilidade oxidativa, abrindo assim a possibilidade de realizar análises sustentáveis e muito rápidas em tempo real, mesmo em comparação com o método padrão.
Material e métodos
As amostras de biodiesel foram sintetizadas a partir de óleo de soja adquirido no mercado local. Resumidamente, 6,7 g de KOH foram dissolvidos em 110 mL de metanol sob agitação. Em seguida, 450 mL de óleo de soja foram transferidos para um Erlenmeyer sob agitação vigorosa e adicionados à solução de metanol/KOH. Após duas horas de reação, a mistura foi transferida para um funil separador e deixada repousar por 4 h. Em seguida, foi retirada a camada inferior contendo glicerina e excesso de álcool. A camada de éster foi lavada com água destilada para remoção dos resíduos dispersos de glicerina e alcoolato. A síntese foi monitorada por cromatografia em camada delgada usando uma mistura de hexano, acetato de etila e ácido acético glacial (95: 2,5: 2,5 v/v) como eluente. Em seguida, o biodiesel purificado foi seco com sílica Zeosil ZS1165mp e peneiras moleculares, mantido sob agitação por 24 horas. A oxidação do biodiesel foi realizada colocando-se 450 mL de biodiesel em um frasco de Erlenmeyer e mantidos a 110 ºC simulando uma análise de Rancimat. Em seguida, um fluxo de ar constante foi injetado na amostra para acelerar o processo de oxidação. Uma alíquota foi tomada a cada 10 minutos por 6 horas e 30 minutos. Após esse processo, 3g das alíquotas foram submetidas à análise de Rancimat de acordo com a norma EN 14112 (2020) a 110 °C e vazão de 10 Lh-1. Os espectros Raman foram adquiridos em um equipamento Raman Bruker FT com laser em λ0 = 1064 nm. Todos os espectros Raman foram adquiridos através de um vial de cromatografia, de vidro, com 600 mW de potência, resolução de 4 cm-1 e 64 acumulações cada. 57 amostras foram coletadas através do processo de oxidação, e cinco repetições de espectro foram medidas. Todos os espectros foram processados em ambiente MATLAB (Versão 2023a). As análises exploratórias multivariadas e PLS foram executadas no PLS Toolbox Versão 9.1 (2022). Os espectros foram dispostos em uma matriz de 285x569 e pré-processados com filtro Savitzky Golay de alisamento (ordem: 0, janela: 5 pt), correção de linha de base e correção de dispersão multiplicativa (MSC). Para a análise de PCA e PLS, foram também utilizadas correção da linha de base (Filtro Automático de Whittaker, assimetria = 1e-06 e lambda = 100), suavização do filtro Savitzky Golay (ordem: 0, janela: 5 pontos) e centragem na média.
Resultado e discussão
A degradação oxidativa produz um aumento na intensidade dos modos de flexão CH2
e CH3 (1500 – 1400 cm-1) e uma diminuição nos modos C=C (1656 cm-1). Uma visão
geral das mudanças estruturais que acompanham o processo de oxidação foi
primeiramente obtida através da análise de PCA, e os resultados estão
representados na Figura 1. O gráfico de escores mostra através da PC3 um padrão
claro que acompanha a variação de oxidação (marcadores rosa a azul). Com as
amostras menos oxidadas encontradas na região negativa do PC3, seus respectivos
pesos (loadings) (Figura 1b) mostram os modos vibracionais -C=C- como tendo
maior contribuição, juntamente com os modos -C-H (estiramento assimétrico -CH2).
Isso coincide totalmente com as amostras em estágios iniciais de oxidação, pois
a clivagem das ligações -C=C- baixa ou ausente é esperada.
Embora uma variação aparentemente pequena seja observada através do PC2, a
inclusão de amostras completamente oxidadas coloca em perspectiva a extensão da
oxidação e permite verificar a importância da modificação das ligações -C=C- ao
longo da oxidação. Nota-se que esses modos vibracionais têm a maior importância
e, ao mesmo tempo, um claro deslocamento para frequências mais altas de seu
valor original de número de onda (1672 cm-1), o que pode estar associado ao
processo de clivagem das ligações duplas formando novos compostos insaturados
(PULLEN; SAEED, 2012).
Para a calibração utilizando o PLS, seis variáveis latentes foram utilizadas,
capturando 99,85% e 90,07% da variância explicada nos espectros e na matriz de
concentrações, respectivamente. O modelo apresentou um valor de erro de
calibração (RMSEC) de 0,26 h para as amostras de calibração e, quando amostras
externas foram testadas nele, o erro de calibração (RMSEP) foi de 0,31 h. A
proximidade de ambos os valores indica um modelo com erros comparáveis para as
etapas de calibração e de previsão de amostras externas (não inclusas no modelo
de calibração). Além disso, o valor RMSEP é menor que o erro de Rancimat (0,50
h), mostrando que o modelo Raman- PLS apresentou uma melhora significativa na
previsão na do tempo de indução de amostras de biodiesel quando comparado com o
método Rancimat.
Com o objetivo de melhorar o desempenho do modelo, uma seleção de variáveis
através do método interval-PLS (iPLS) também foi executada, e um segundo modelo
de calibração foi construído. Essas regiões correspondem principalmente aos
modos vibracionais C-H e C=C, onde se espera encontrar uma maior variação de
intensidade à medida que o processo de oxidação ocorre. A comparação dos dois
modelos é mostrada na Tabela 1, mostrou que o desempenho foi comparável, com
discreta melhora na proximidade de RMSEC e RMSEP para o modelo iPLS. Além disso,
apesar desses dois parâmetros serem maiores que os valores obtidos para o modelo
PLS (0,28 e 0,31 horas), para uma aplicação prática não representaria uma
variação significativa no tempo (15,6 e 16,8 min para os métodos PLS e iPLS,
respectivamente). ou seja, essa diferença menor que 1 min não mudaria uma
decisão sobre uma amostra de biodiesel sob controle de qualidade para seu uso
como combustível.
Em relação a metodologias similares baseadas em técnicas espectroscópicas, vale
destacar o trabalho de Canha et al. (CANHA et al., 2012) onde foi desenvolvido
um método utilizando espectroscopia no infravermelho próximo para determinar a
estabilidade oxidativa do biodiesel. Os valores dos erros de calibração e
previsão alcançados neste caso foram 0.53 e 0.60 h, respectivamente, próximos ao
erro de Rancimat. Com os resultados aqui obtidos, mostramos que ambos os modelos
PLS- e iPLS- Raman permitem a previsão do tempo de indução do biodiesel de soja,
com uma melhora no erro relativo de ~ 47% em relação ao método padrão.
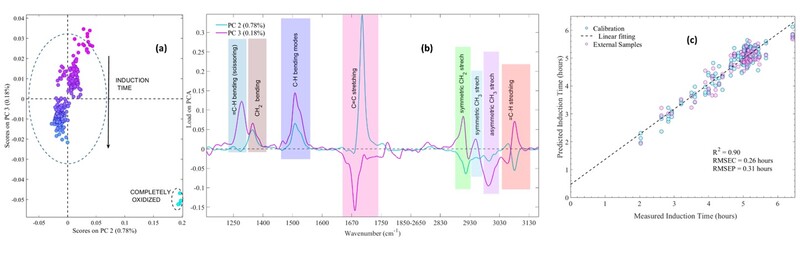
(a) Gráfico de escores de PC2 vs. PC3. (b) loadings \r\nPC2 (0,78%, azul) e PC2 (0,18%, rosa). (c) modelo \r\nPLS
Figuras de mérito para a previsão da estabilidade \r\noxidativa de amostras de biodiesel.
Conclusões
A união da quimiometria e da espectroscopia Raman possibilitou desenvolver uma metodologia capaz de prever a estabilidade oxidativa do biodiesel (medida através do tempo de indução em horas), seguindo um procedimento de análise muito rápido e sem o uso de reagentes adicionais ou condicionamento demorado da amostra. Quando comparados com trabalhos preliminares, os modelos PLS- e iPLS-Raman foram capazes de prever amostras externas com uma melhora significativa de aproximadamente 47% nos erros de previsão quando comparados ao erro relatado para métodos anteriormente desenvolvidos utilizando técnicas espectroscópicas. Ainda assim, essa vantagem se mantém quando comparada aos resultados relatados em trabalhos semelhantes. Em geral, a estratégia PLS-Raman oferece uma alternativa promissora, rápida e ambientalmente amigável às análises de rotina para monitorar a estabilidade oxidativa do biodiesel. Além disso, poderia ser facilmente adaptado a aplicações no campo ou em processos em linha. Os espectros Raman são altamente informativos das modificações estruturais que ocorrem durante o processo de oxidação, permitindo a compreensão de sua química além da estatística e matemática dos modelos quimiométricos.
Agradecimentos
Os autores agradecem ao PRH-ANP (Nº. 049.1) e ao CNPQ (Nº 405087/2021-7). Os autores também agradecem a Central Multiusario da UFABC e A UFU.
Referências
ALVES, J. C. L.; POPPI, R. J. Biodiesel content determination in diesel fuel blends using near infrared (NIR) spectroscopy and support vector machines (SVM). Talanta, v. 104, p. 155–161, jan. 2013.
BALABIN, R. M.; SAFIEVA, R. Z. Biodiesel classification by base stock type (vegetable oil) using near infrared spectroscopy data. Analytica Chimica Acta, v. 689, n. 2, p. 190–197, mar. 2011.
BAPTISTA, P. et al. Multivariate near infrared spectroscopy models for predicting the methyl esters content in biodiesel. Analytica Chimica Acta, v. 607, n. 2, p. 153–159, jan. 2008a.
BAPTISTA, P. et al. Monitoring the Quality of Oils for Biodiesel Production Using Multivariate near Infrared Spectroscopy Models. Journal of Near Infrared Spectroscopy, v. 16, n. 5, p. 445–454, 1 out. 2008b.
CANHA, N. et al. Multivariate near infrared spectroscopy models for predicting the oxidative stability of biodiesel: Effect of antioxidants addition. Fuel, v. 97, p. 352–357, jul. 2012.
CEN. EN 14112: Fat and oil derivatives - Fatty acid methyl esters (FAME) - Determination of ester and linolenic acid methyl ester contents. [s.l: s.n.].
DE LIRA, L. F. B. et al. Infrared spectroscopy and multivariate calibration to monitor stability quality parameters of biodiesel. Microchemical Journal, v. 96, n. 1, p. 126–131, set. 2010a.
DE LIRA, L. F. B. et al. Infrared spectroscopy and multivariate calibration to monitor stability quality parameters of biodiesel. Microchemical Journal, v. 96, n. 1, p. 126–131, set. 2010b.
HÖSKULDSSON, A. PLS regression methods. Journal of Chemometrics, v. 2, n. 3, p. 211–228, jun. 1988.
KUMAR, N. et al. Chemometrics tools used in analytical chemistry: An overview. Talanta, v. 123, p. 186–199, jun. 2014.
LIU, Z. et al. Raman spectroscopy for the discrimination and quantification of fuel blends. Journal of Raman Spectroscopy, p. jrs.5602, 5 abr. 2019.
LÔBO, I. P.; FERREIRA, S. L. C.; CRUZ, R. S. da. Biodiesel: parâmetros de qualidade e métodos analíticos. Química Nova, v. 32, n. 6, p. 1596–1608, 2009.
MAAWA, W. N. et al. Performance, combustion, and emission characteristics of a CI engine fueled with emulsified diesel-biodiesel blends at different water contents. Fuel, v. 267, p. 117265, maio 2020.
MIRANDA, A. M. et al. Line shape analysis of the Raman spectra from pure and mixed biofuels esters compounds. Fuel, v. 115, p. 118–125, jan. 2014.
PULLEN, J.; SAEED, K. An overview of biodiesel oxidation stability. Renewable and Sustainable Energy Reviews, v. 16, n. 8, p. 5924–5950, out. 2012.
SOARES, S.; ROCHA, F. R. P. Multi-energy calibration to circumvent matrix effects in the determination of biodiesel quality parameters by UV–Vis spectrophotometry. Talanta, v. 209, p. 120584, mar. 2020.
SUBRAMANIAM, Y.; MASRON, T. A.; AZMAN, N. H. N. Biofuels, environmental sustainability, and food security: A review of 51 countries. Energy Research & Social Science, v. 68, p. 101549, out. 2020.
WOLD, S.; ESBENSEN, K.; GELADI, P. Principal component analysis. Chemometrics and Intelligent Laboratory Systems, v. 2, n. 1–3, p. 37–52, ago. 1987.
WOLD, S.; SJÖSTRÖM, M.; ERIKSSON, L. PLS-regression: a basic tool of chemometrics. Chemometrics and Intelligent Laboratory Systems, v. 58, n. 2, p. 109–130, out. 2001.
ZHOU, J. et al. Analysis of the oxidative degradation of biodiesel blends using FTIR, UV–Vis, TGA and TD-DES methods. Fuel, v. 202, p. 23–28, ago. 2017.