ÁREA
Química de Materiais
Autores
Silva, C. (IFPA) ; Gonçalves, W. (IFPA) ; Lima, E. (IFPA) ; Macedo, M. (IFPA) ; Porfírio, R. (IFPA)
RESUMO
As baterias de íon-lítio estão sendo utilizadas massivamente em vários dispositivos eletrônicos e consequentemente maiores quantidades estão sendo descartadas de forma irregular. A reciclagem reduz preocupações ambientais, impulsiona a inovação tecnológica e promove regulamentações para um descarte mais adequado. Nesse trabalho, é proposto uma forma de quantificar, tratar e separar os componentes de três tipos de baterias de celulares destinados a reciclagem, empregando técnicas de análise como a fluorescência de Raio-X que determina os óxidos em cerca de P2O5 (3%), CoO (92%), CuO (3%), MnO (90%) e SO3 (4%), como os compostos mais encontrados nos componentes das baterias de íon- lítio analisadas, mostrando a importância da reciclagem no desenvolvimento sustentável.
Palavras Chaves
Baterias de íon-lítio; Óxidos; Reciclagem
Introdução
• História A trajetória das baterias de íons de lítio tem início com as investigações realizadas pelo físico-químico americano Gilbert Newton Lewis em 1912, explorando as baterias de lítio metálico. Entretanto, somente a partir de 1970 é que as primeiras baterias primárias (não recarregáveis), usando lítio como ânodo, começaram a ser introduzidas no mercado. (ARANHA, 2018) Após várias buscas, o químico americano John B. Goodenough descobriu que a bateria com óxido de lítio-cobalto no cátodo era quase duas vezes mais potente. Na década de 1980, ele publicou a descoberta do novo material catódico denso em energia que, apesar de seu baixo peso, resultou em baterias poderosas e de alta capacidade. Por volta de 1986, foi a vez de Akira Yoshino, da Asahi Kasei Corporation, desenvolveu a primeira bateria de íons de lítio comercialmente viável, com uma vida útil longa, podendo ser carregada por várias vezes sem perda de desempenho. (CFQ, 2019) Foi somente em 1991 que a Sony comercializou a primeira bateria de íons lítio, baseada no ânodo de grafite© e cátodo de óxido cobalto de lítio (LiCoO2). (ARANHA, 2018) • Baterias de íons lítio As baterias de íon-lítio possuem componentes como ânodo, cátodo, eletrólito e separador. O contato elétrico é estabelecido através da sobreposição e compressão dos ânodos, cátodos e separadores. O cátodo é formado por uma placa de alumínio revestida com material catódico ativo, tipicamente LiCoO2, um condutor elétrico, o aglutinante PVDF e aditivos químicos. Enquanto isso, o ânodo consiste em uma placa de cobre revestida com grafite de carbono, juntamente com um condutor elétrico e aditivos. (SILVA, 2022) Em 2019, receberam reconhecimento do Prêmio Nobel de Química devido às suas características notáveis, como alta densidade de energia, peso reduzido, necessidade mínima de manutenção e imunidade ao efeito de memória. Além disso, quando comparadas às baterias de chumbo-ácido ou cádmio, essas baterias demonstraram causar menos impacto ambiental quando descartadas (LI et al., 2012). Em geral, a vida útil das LIBs (do inglês Lithium-Ion Battery) varia de 3 a 10 anos (ZENG et al., 2014). Embora sejam menos poluentes que outros tipos de baterias, os componentes inflamáveis e substâncias tóxicas em sua composição representam uma ameaça ao meio ambiente e à saúde humana se forem descartados em aterros (CHEN et al., 2016). Além da etapa de descarte, é essencial considerar os impactos ambientais negativos na extração de matéria-prima e em outras fases do ciclo de vida das baterias. Por isso, o desenvolvimento de tecnologias de reciclagem é crucial para preservar metais valiosos, aproveitar materiais existentes e reduzir o impacto ambiental. Isso não apenas conserva metais escassos e valiosos, mas também promove a economia circular e incentiva práticas industriais sustentáveis (RONCHINI, 2022). • Problemática Conforme a tecnologia avança, a frequente introdução de novos dispositivos eletrônicos gera uma obsolescência rápida dos modelos antigos. Isso leva ao descarte inadequado de muitos aparelhos, como telefones celulares, computadores, tablets e TVs. Até 2024, estima-se a produção de 221 bilhões de baterias íon-Li, o que resultará em quantidades preocupantes de resíduos. Apenas em 2017, as vendas dessas baterias geraram 25.000 toneladas de resíduos. A taxa de reciclagem ainda é baixa, ficando em torno de 5%. Optar pelo descarte em aterros sanitários tem impactos sérios no meio ambiente e seres vivos, além de desperdiçar fontes secundárias valiosas de metais críticos. (SILVA, 2022) Acredita-se que até 2050 os principais componentes da linha de produção das baterias como lítio, cobalto, grafite, níquel, e manganês aumentarão em mais de 50% a produção atual, se tornando um material crítico para produção tecnológica. Globalmente a capacidade projetada para a produção de baterias irá aumentar quatro vezes de 2021 a 2025 e com isso 700.000 toneladas de baterias de lítio chegarão ao fim de sua vida útil. (MELIN, 2018). Cada país cria suas próprias diretrizes e leis. (RONCHINI, 2022) Regulamentações surgiram para controlar o descarte inadequado de baterias devido ao aumento do consumo e riscos de contaminação. No Brasil, a Resolução do CONAMA n° 257, julho de 1999, e a Resolução n° 263, novembro de 1999, estabeleceram limites para o descarte de metais perigosos. Substituindo-as, a Resolução n° 401, novembro de 2008, proibiu o descarte em aterros. A Política Nacional de Resíduos Sólidos, aprovada no final de 2010, enfatiza a logística reversa, envolvendo consumidores, distribuidores e fabricantes na responsabilidade pelo destino das baterias após o uso.(BARCELOS, 2020) Sendo assim, este trabalho tem como objetivo identificar os óxidos mais utilizados nas baterias de íon-lítio para reciclagem e diminuição dos impactos ambientais.
Material e métodos
MATERIAIS: - Capela e EPI’s apropriados; - Peneira de 80 mesh; - Espectrômetro de fluorescência de raios-x (BRUCKER); - Prensa Hidráulica (TECLAGO, PCA 40). - Balança Analítica (MARTE, Modelo: AY220) • Tratamento das baterias: As baterias foram coletadas em lojas de concerto de celulares e separadas por marcas. Foram abertas em capela com circulação forçada, para facilitar a evaporação dos compostos gasosos liberados. Os componentes materiais foram separados em polímeros, alumínio e cobre. Os resíduos de grafite foram removidos manualmente com auxílio de espátula e armazenados em recipientes herméticos. Para as análises por fluorescência de raio -x, as amostras foram peneiradas em malha #80 e homogeneizadas, separando cerca de 12 g de cada tipo de bateria. • Quantificação das Baterias Após a remoção manual dos compostos amorfos (pós), ocorreu a separação e pesagem de cada componente da bateria, classificados como: polímeros, cobre e alumínio e resíduos. • Preparação da amostra para Fluorescência de Raio-X (FRX) A composição química das baterias foi encontrada pelas análises de fluorescência de raio-x, utilizando o espectrômetro de fluorescência de raios-x da BRUCKER modelo RANGER S2, com tubo de paládio. Para cada amostra analisada, pesou-se 3g de CeraWax para aglutinar os compostos, formando pastilhas pressionadas na prensa hidráulica PCA 40 de 20 ton.
Resultado e discussão
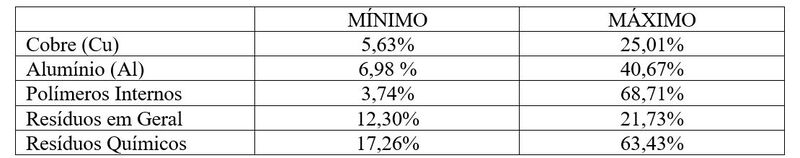
• Quantificação das Baterias:
Na quantificação das baterias, foram pesadas 15 baterias, de onde retirou-se um
intervalo operacional mínimo e máximo para cada componente envolvido no
funcionamento da bateria, como pode ser observado na Tabela. 1.
Essas variações ocorrem devido as diferenças das marcas, dos tamanhos das
baterias de acordo com o celular e quantidade de energia específica que o
aparelho necessita ter para que funcione todo o seu sistema.
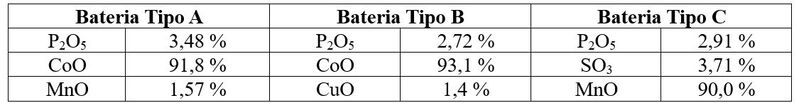
• Análise de Fluorescência de Raio-X
Os resultados mais significativos encontrados nas análises por fluorescência de
raio - X para as baterias avaliadas estão expostas na Tabela. 2.
Os resultados mostrados na Tabela 2, apresentam quais os elementos estão
contidos nos óxidos, responsáveis por algumas características específicas
atribuídas as baterias.
Cada óxido apresenta uma funcionalidade no desempenho e funcionamento do
sistema. O P2O5 encontrados na Bateria A, B e C pode ser originado dos óxidos de
LiFePO4 e LiFePO4F, esses compostos não apresentam tantos problemas como os
demais, por ser termicamente estável, menos danoso ao meio ambiente e possuir
toxidade baixa (RUA, 2015; COSTA, 2010).
O MnO presentes nas Baterias A e C é encontrado no LiMn2O4, este óxido é
bastante utilizado nas baterias de Lítio-íon, devido seu baixo valor econômico,
tornando-se mais rentável para as empresas fabricantes, tem uma boa voltagem
média, em cerca de 4V. Além de apresentar uma capacidade específica considerável
de 120 mAh/g. Seu ponto negativo é a perda de carga em momentos de longos
períodos de inatividade, o que possivelmente, reduz o ciclo de vida desse tipo
de bateria (COSTA, 2010).
O CoO encontrado na análise vem do LiCoO2 sendo o óxido mais utilizado em
baterias, e está presente nas Baterias A e B. Este óxido possui alta densidade
de energia, é mais estável principalmente em elevadas temperaturas, apresenta
uma boa voltagem média e a duração de 500 ciclos de carga/descarga. O seu maior
obstáculo é quanto ao custo de produção, por ser mais elevado (RUA, 2015; COSTA,
2010).
O CuO pode ser devido a contaminação durante o processo de separação. O Cobre é
um dos componentes do eletrodo negativo coberto com uma camada de grafite colada
com resina polimérica PVDF (fluoreto de polivilideno) (COSTA, 2010).
O SO3 é derivado dos sais de lítio inorgânicos encontrados nos eletrólitos das
baterias para facilitar a condução iônica, responsáveis pelos transportes dos
íons de um eletrodo para o outro no processo de carga e descarga (COSTA, 2010).
Fonte: Autor, 2023.
Fonte: Autor, 2023.
Conclusões
Durante o processo de retirada manual do resíduo, pode ocorrer perdas de pequenas quantidades de cobre e alumínio. Essas folhas são coladas ao grafite o que dificulta a retirada completa. Com os resultados obtidos verificou-se que as baterias de lítio-íon são as mais utilizadas atualmente, principalmente nos aparelhos celulares atuais, por mostrarem uma versatilidade quanto ao uso nas baterias. Apesar de possuir componentes que podem ser prejudiciais ao meio ambiente e a saúde humana (SILVA et al., 2018). Ainda assim, tornar-se menos tóxicas que outros tipos de baterias como as gerações anteriores de Ni-Cd. As baterias de Li-Íon atendem ao desempenho dos celulares, e da diminuição dos riscos, como a explosão por isso a escolha dos seus óxidos é de extrema importância (SANTOS, 2018; HANNAN et al., 2018). Cada marca de celular escolhe o óxido litiado que mais se adequa ao aparelho ou modelo. Logo, deve-se utilizar óxidos que sejam mais eficientes em termos de energia, durabilidade e que acompanhe as propostas das linhas dos vários fabricantes. É comum que as empresas utilizem os óxidos litados de LiCoO2 e LiMn2O4, por apresentarem maior capacidade específica e boa voltagem média. Algumas empresas utilizam somente um tipo de óxido ou mistura de dois, para que as suas propriedades sejam integradas a fim de melhorar o potencial da bateria e do ponto de vista econômico, o que torna o processo mais barato. Portanto, esse trabalho teve o objetivo de mostrar quais tipos de óxidos são mais usados em baterias de lítio-íon, algumas vantagens e desvantagens quanto ao uso e sua importância para o bom funcionamento das baterias nos respectivos aparelhos, e de forma caracterizada, manter a sustentabilidade ambiental no descarte responsável e adequado no pós-uso.
Agradecimentos
Nossos agradecimentos ao IFPA - Campus Belém, ao LABTEC e ao PROEX pelo suporte e auxílio para a nossa pesquisa.
Referências
ARANHA, Juliana Cintra Miranda de Souza. Uma contribuição ao estudo de técnicas de estimação de estado de carga e estado de saúde para baterias de Lítio-íon. Dissertação de Mestrado; UNICAMP, Campinas, 2021.
ARANHA, Wesley Monteiro. Caracterização De Bateria Recarregável De Lítio De Veículos Híbridos Visando Sua Reciclagem. Projeto de Graduação; Universidade Federal do Rio de Janeiro, Rio de Janeiro, 2018.
BARCELOS, Lucas Pegrucci. Estudos sobre o reaproveitamento de baterias íon-lítio. Trabalho de Conclusão de Curso, Universidade Federal de Uberlândia, MG, 2020.
COSTA, Rodrigo Calçada da. Reciclagem de baterias de íons de lítio por processamento mecânico. Dissertação de Mestrado; Universidade Federal do Rio Grande do Sul, 2010.
CFQ. Prêmio Nobel de Química vai para cientistas que criaram a bateria de íon de lítio. 2019. Disponível em: <https://cfq.org.br/noticia/premio-nobel-de-quimica-vai-para-cientistas-que-criaram-a-bateria-de-ion-de-litio/>. Acesso em 16 de agosto de 2023.
CHEN J., LI Q., SONG J., SONG D., ZHANG L., SHI X. Environmentally friendly recycling and effective repairing of cathode powders from spent LiFePO4 batteries. Green Chem. 2500–2506. 2016.
HANNAN, M. A. et al. State-of-the-art and energy management system of lithium-ion batteries in electric vehicle applications: issues and recommendations. IEEE Access, v. 6, p. 1–1, 2018
LI, Li et al. Ascorbic-acid-assisted recovery of cobalt and lithium from spent Li-ion batteries. Journal of Power Sources, v. 218, p. 21-27, 2012.
MELIN, H. E. The lithium-ion battery end-of-life market–A baseline study. World Economic Forum: Cologny, Switzerland, v. 2018, p. 1–11, 2018.
RUA, João Luís dos Santos Heleno da. Baterias de Lítio em Filme Fino: Fabrico e caracterização de LiCoO2 para utilização no cátodo. Dissertação de Mestrado; Universidade do Minho, 2015.
RONCHINI, Carolina Magda Bassoto. Separação Do Material Catódico E Anódico De Baterias De Íon Lítio. Dissertação de Mestrado; Universidade Estadual Paulista “Júlio De Mesquita Filho”, São João da Boa Vista, 2022.
SANTOS, Célia Aparecida Lino dos. Baterias de íons lítio para veículos elétricos. Revista IPT: Tecnologia e Inovação, vol.2. Nº 9, p. 62-82, fevereiro, 2018.
SILVA, Rafael Gundim; AFONSO, Júlio Carlos; MAHLER, Claudio Fernando. LIXIVIAÇÃO ÁCIDA DE BATERIAS ÍON-LÍTIO. Química Nova, vol. 41, Nº 5, p. 581-586, Fevereiro, 2018.
SILVA, Adriane Toledo. Viabilidade do uso de solvente eutético para dissolução seletiva de cobalto e lítio oriundos de baterias de íon-lítio descartadas. Dissertação de Pós Graduação; Universidade Federal de Viçosa, MG, 2022.
ZENG X., J.LI J., SINGH N. Recycling of spent lithium-ion battery: a critical review. Crit. Ver. Environ. Sci. Technol. 1129–1165, 2014.