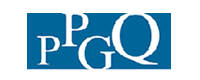ÁREA
Química de Materiais
Autores
Chaves, M.G.M. (UNIVERSIDADE ESTADUAL VALE DO ACARAÚ - UEVA) ; Souza, M.V.L. (UNIVERSIDADE ESTADUAL VALE DO ACARAÚ - UEVA) ; Rodrigues, F.H.A. (UNIVERSIDADE ESTADUAL VALE DO ACARAÚ - UEVA)
RESUMO
Hidrogéis bionanocompósitos baseados em amido enxertado com poli(acrilato de sódio) e nanowhiskers de celulose foram sintetizados por polimerização em solução com o interesse no estudo destes sistemas como adsorventes alternativos de íons metálicos (Pb(II)/Cu(II)) a partir de soluções aquosas. A caracterização por FTIR, DRX e o processo de adsorção competitiva de íons Pb(II) e Cu(II) a partir de hidrogéis bionanocompósitos foram investigados. Os resultados de FTIR e DRX confirmaram a reação de copolimerização e a formação dos hidrogéis bionanocompósitos. Estes resultados de adsorção competitiva demonstraram que os hidrogéis bionanocompósitos possuem alta seletividade para Pb(II) entre Pb(II) e Cu(II).
Palavras Chaves
Polissacarídeos; Íons metálicos; Remediação
Introdução
A água é um recurso natural que atualmente vem trazendo grande preocupação, pois o índice de escassez e poluição estar cada vez aumentando. Os rejeitos gerados pelas indústrias são, em geral, espécies químicas altamente tóxicas para os solos, águas e o homem. Os efluentes contendo metais pesados devem receber tratamentos adequados antes de sua disposição no meio ambiente para evitar o desequilíbrio de ecossistemas aquáticos, haja vista que tais contaminantes não são biodegradáveis. A legislação ambiental tem buscado novos métodos de controlar este descarte afim de que o impacto ambiental seja minimizado. Dentre estes métodos, a adsorção é a técnica mais largamente utilizada devida a sua simplicidade, elevada eficiência, fácil recuperação e reutilização dos adsorventes (Rodrigues et al., 2019). Atualmente, diferentes métodos e/ou tratamentos, incluindo, principalmente, os processos físicos, químicos e biológicos têm sido usados para a adsorção de íons metálicos e corantes iônicos de águas residuais. Dentre estas, a adsorção é a técnica mais largamente utilizada por ser de baixo custo, mais eficiente, energeticamente econômica, de fácil operação, não gerar resíduos tóxicos ou outros subprodutos (Melo et al., 2018). Neste sentido, a síntese de adsorventes à base de polissacarídeos tem despertado particular interesse, porque muitos polissacarídeos são atóxicos e/ou biodegradáveis. Esses novos materiais, denominados como hidrogéis inteligentes, têm despertado grande interesse quanto ao uso como sistemas de separação e adsorção de íons metálicos e/ou corantes iônicos, principalmente os hidrogéis obtidos a partir de polímeros naturais como a celulose, amido e quitosana, que estão sendo constantemente estudados para remoção de tais contaminantes em águas residuais. Por outro lado, o interesse na utilização de nanopartículas de reforço em matrizes poliméricas, compósitos ou nanocompósitos, tem aumentado. Os nanowhiskers de celulose (NWCs) consistem de nanopartículas com alto grau de cristalinidade, com alta área específica e podem ser obtidos a partir da hidrolise ácida de diferentes fontes de fibras naturais tais como o algodão (Spagnol et al., 2012a; 2012b). No presente trabalho hidrogéis nanocompósitos a base de amido enxertados com poli(acrilato de sódio) e NWCs foram sintetizados por polimerização em solução com interesse nestes sistemas como adsorventes de íons metálicos a partir de soluções aquosas, especificamente no processo de adsorção competitiva de íons Pb(II) e Cu(II) a partir de hidrogéis bionanocompósitos.
Material e métodos
Obtenção de NWCs A extração dos NWCs foi feita por hidrólise ácida (HCl, 12 mol.L-1) a 45 ºC e sob agitação por 60 minutos (razão celulose:volume de HCl = 1 g:20 mL). Síntese de hidrogéis bionanocompósitos (St-g-PNaAc/NWCs) Uma quantidade de amido (St) foi gelatinizada a 85 °C sob agitação magnética em 30 mL de água destilada sob fluxo de N2. Em seguida, a temperatura foi arrefecida a 70 °C, e 1 % m/m de KPS foi introduzido para gerar radicais na St. 15 minutos depois, quantidades específicas AA (parcialmente neutralizado com solução de NaOH, 70%), 1 % m/m de MBA e 10 % m/m NWCs foram adicionadas. O produto resultante (St-g-PNaAc/NWCs foi resfriado à temperatura ambiente e, lavado com água destilada, em seguida, seco em estufa a uma temperatura de 70 ºC e macerado até granulometria de 9-24 mesh (2,00-0,71 mm). Além disso, uma amostra sem CNWs, foi preparada (St-g- PnaAc). FTIR e DRX Os espectros de FTIR foram obtidos em equipamento Shimadzu FTIR-8300, operando na faixa de 400-4000 cm-1, em pastilha de KBr. Enquanto os padrões de DRX do pó (DRX) foram registrados em um difratômetro Siemens (modelo D500, Alemanha) equipado com uma fonte Cu-Kα (λ = 0,15418 nm). Adsorção competitiva O experimento de adsorção competitiva foi realizado pela imersão de 25 mg das amostras do adsorvente em 50 mL da mistura contendo 500 mg.L-1 de cada íon metálico bivalente (Pb(II) e Cu(II)), sob agitação por 60 minutos em temperatura ambiente. As soluções resultantes foram filtrados e diluídas adequadamente, e a concentração dos íons metálicos remanescentes na solução foi analisada usando AAS. Em seguida, as concentrações das amostras foram determinadas por meio das equações de regressão linear (ABS = 1,32 x 10-5[Pb(II)] – 6,80 x 10-4; R2 = 0,9958] e ABS = 1,6 x 10-4[Cu(II)] – 9,65 x 10-3, R2 = 0,9984), respectivamente para os íons metálicos Pb(II) e Cu(II). A quantidade dos íons metálicos adsorvidos competitivamente foram calculadas usando a equação (1). qe = (Co-Ce)V/( m) (1) onde, qe é a quantidade do íon metálico adsorvido no equilíbrio (mg.g-1), Co e Ce é a concentração inicial e final do íon metálico (mg.L-1), V é o volume da solução dos íons metálicos e m a massa do hidrogel utilizado (g). Todos os ensaios foram realizados em triplicata. O coeficiente de partição (P) é a razão da concentração de um único íon de metálico pela soma das concentrações dos dois íons metálicos na amostra em equilíbrio, que pode ser calculado pela Equação (2) (Liu et al., 2020). Adicionalmente, o coeficiente de remoção seletiva (α) pode ser calculado usando a Equação (3) [1]. P= Xi/∑(j=1)^n Xj)(j=1,i,…n) (2) α= (qmax⁄Cx,max)/(qmin⁄Cx,min) ) (3) onde, a soma dos coeficientes de partição é igual a 1; Xi e Xj são as capacidades de adsorção de i e j, respectivamente. A concentração inicial para cada um dos íons metálicos foi 500 mg.L-1.
Resultado e discussão
Caracterização dos bionanocompósitos
A Figura 1(a) mostra os espectros de FTIR das fibras de algodão in natura, NWCs,
amido e dos hidrogéis sintetizados na ausência (St-g-PNaAc) e presença de 10%
m/m de NWCs (St-g-PNaAc/NWCs). Os espectros de FTIR das fibras de algodão in
natura e NWCs são bastante semelhantes. Existem bandas características do
material celulósico como estiramento de ligação O-H na região entre 3300-3700
cm-1, estiramento assimétrico da ligação C-H na região de 2900 cm-1, deformação
angular da ligação C-H de 1290 a 1310 cm-1 e estiramento da ligação CO na região
de 950 a 1200 cm-1 e as ligações C-O-C, C-C-O e C-C-H em 898 cm-1 (Satyamurthy
et al., 2011). A partir dos espectros da Figura 1a-b, verificou-se que a reação
de hidrólise ácida, realizada para a obtenção dos nanowhiskers de celulose a
partir das fibras algodão in natura, não afeta a estrutura química dos
fragmentos celulósicos, mas a sua morfologia.
O espectro do amido mostra uma banda alargada na região de 3365 cm-1
correspondente ao estiramento dos grupos hidroxila O-H e as bandas em 1158,
1081, e 1014 cm-1, atribuídas ao estiramento vibracional C-O. Embora os
espectros FTIR dos hidrogéis de St-g-PNaAc e St-g-PNaAc/NWCs apresentem as
bandas procedentes do amido puro, porém, são mais fracas. O espectro da St-g-
PNaAc e pode ser observado um ombro característico em 1723 cm-1 atribuído ao
estiramento -COOH e as bandas em 1572 e 1406 cm-1 atribuída ao estiramento
simétrico e assimétrico da ligação C=O. As bandas de absorção em 1647, 1421 e
1368 cm-1, atribuída a deformação C-OH do amido, não foram observadas, indicando
que os grupamentos C-OH do St participaram da reação de enxertia com o acrilato
de sódio (Gomes et al., 2015). As bandas de absorção em 1723, 1572 e 1408 cm-1
no espectro de St-g-PNaAc/NWCs são atribuídas ao estiramento -COOH, estiramento
assimétrico COO- e estiramento simétrico COO-, respectivamente. Isto confirma
que a parte do ácido acrílico foi neutralizado pela solução de NaOH.
Figura 1. (a) Espectros de FTIR de fibras de algodão in natura, NWCs, St, St-g-
PNaAc e St-g- PNaAc/NWCs. (b) Difratogramas de DRX de fibras de algodão in
natura, NWCs, St-g-PNaAc e St-g- PNaAc/NWCs.
A Figura 1(b) mostra o padrão de difração das fibras de algodão in natura e da
NWCs, respectivamente. Os padrões de difração mostram que ambos possuem
nanocristais de celulose na sua estrutura e esses cristais apresentam picos de
difração em 2θ = 14,5°, 16,3°, 22,4°, e 34,1° que são características das
posições 101, 101’, 002 e 040 típicas da forma cristalina da celulose I. O
índice de cristalinidade de celulose nanowhiskers (ICR) foi determinada pelo
método empírico descrito de acordo com a Equação (4), (Segal et al., 1959):
Icr = [I002- IAM)/I002 ] x 100 (4)
onde: I002 é a intensidade máxima de difração correspondente ao plano 002 dos
cristais de celulose (reflexão atribuída às zonas cristalinas; detectada a um
ângulo 2θ = 22,5°; IAM é a intensidade de difração registrada a um
ângulo 2θ = 18° (reflexão atribuída às zonas amorfas).
O tratamento de hidrólise para obtenção dos nanocristais de celulose aumenta o
índice de cristalinidade (ICr 90,3%) das fibras em relação ao algodão (ICr 80%),
devido ao ataque ácido preferencial as regiões amorfas presentes na celulose, o
que aumenta o teor de domínios cristalinos nos nanocristais de celulose obtidos.
O índice de cristalinidade relativa é de aproximadamente 90%, o que está de
acordo com outros valores obtidos na literatura (Elazzouzi-Hafraoui et al.,
2008). Enquanto o difratograma do St-g-PNaAc não apresentou picos de difração,
indicando que o hidrogel apresenta uma estrutura predominante amorfa. Por outro
lado, o difratograma do hidrogel nanocompósito (St-g-PNaAc/NWCs), a
característica da NWCs cristalina (2θ = 22,78°) foi mantida. Os resultados
observados por DRX e corroborados pelo FTIR para a formação do hidrogel
nanocompósito sugerem a presença da NWCs na matriz polimérica.
Ensaios de adsorção
Sabe-se que vários parâmetros, tais como: pH; temperatura; concentração inicial
de íons; interações íon metálico-adsorvente; grupos funcionais do adsorvente;
propriedades de superfície; a competição de íons metálicos entre si, que por sua
vez, depende de sua mobilidade em solução, afetam a taxa de adsorção e sua
capacidade. Alguns metais pesados, tais como, Pb(II), Cu(II), etc., podem
coexistir em efluentes industriais e, portanto, presença de diversos íons
metálicos em solução pode provocar competição pelos sítios disponíveis do
adsorvente, além de produzir possíveis efeitos de sinergismo, antagonismo ou
não-interação com o adsorvente. A adsorção preferencial de metal em uma mistura
contendo Pb(II) e Cu(II) por hidrogéis St-g-PNaAc e St-g-PNaAc/10% NWCs foi
estudado como mostra os resultados da adsorção competitiva na Tabela 1. A
preferência pelos dois íons por ambos adsorventes seguiu a ordem Pb(II) >
Cu(II).
Tabela 1. Adsorção competitiva de íons metálicos bivalentes partir de hidrogéis
St-g-PNaAc e St-g-PNaAc/10% NWCs.
Íon metálico St-g-PNaAc St-g-PNaAc/10% NWCs
Puro Mistura Puro Mistura
qmax (mg.g-1) P (%) α qmax (mg.g-1) P (%) α
Pb(II) 676,74 358,81 69 5,10 756,36 476,28 67 4,13
Cu(II) - 158,76 31 - 234,32 33
Os resultados obtidos a partir da Tabela 1 podem ser atribuídos aos seguintes
fatores:
(i) A presença simultânea de diversos metais causa interferência e competição
entre estes, bem como o local de adsorção (Febrianto et al., 2009). Além disso,
diversos estudos relataram que a presença de co-íons na solução pode reduzir a
remoção de metais pesados devido à adsorção de competição entre esses
contaminantes (Agarwal et al., 2013).
(ii) Os coeficientes de partição dos hidrogéis St-g-PNaAc e St-g-PNaAc/10% NWCs
para íons Pb(II) foram maiores do que para íons Cu(II), o que pode ser atribuído
ao menor raio iônico hidratado de Pb(II) (4,01 Å) < Cu(II) (4,19 Å),
proporcionando uma maior mobilidade, e consequentemente uma maior interação com
os grupos carboxilatos (COO-) presentes nos hidrogéis. Além disso, a capacidade
de adsorção binária foi significativamente menor do que a adsorção não
competitiva, indicando um efeito de antagonismo/inibição, como competição e
interação lateral entre esses íons nos mesmos sítios ativos, com uma redução de
47 e 37 % (Sellaoui et al., 2018; Zauro et al., 2018).
(iii) Os coeficientes de remoção seletiva para os hidrogéis St-g-PNaAc e St-g-
PNaAc/10% NWCs foram 5,11 e 4,13, respectivamente. Estes resultados demonstram
que os hidrogéis possuem alta seletividade para Pb(II) entre Pb(II) e Cu(II).
Estudos revelaram que a eletronegatividade dos íons metálicos estava diretamente
correlacionada com a capacidade de adsorção dos metais no adsorvente
(Vijayaraghavan et al., 2009). Assim pode-se observar que a capacidade de
adsorção nos hidrogéis apresentou a sequência de seletividade, Pb > Cu,
provavelmente devido ao efeito da eletronegatividade dos metais (3,29, 2,98 para
Pb(II), Cu(II), respectivamente) (Zauro et al., 2018; Hu et al., 2017).
(iv) A ordem Pb(II) > Cu(II), a qual pode ser atribuída à especificidade dos
sítios ativos, a diferentes afinidades de adsorção ou ao efeito competição
(Sekhar et al., 2003). Em sistemas multielementar/multicomponente algumas
interações como, por exemplo, o potencial de eletrodo influencia na remoção de
íons metálicos, E Pb(II) (+ 0,13 V) > E
Cu(II) (- 0,34 V).
(a) Espectros de FTIR. (b) Difratogramas de DRX.
Conclusões
Nanowhiskers de Celulose (NWCs) foram obtidos a partir de fibras de algodão, apresentando índice cristalinidade de aproximadamente 90%. Formou-se hidrogéis nanocompósitos de NWCs e amido enxertado com poli (acrilato de sódio), como observado por FTIR e difração de Raios-X. A presença simultânea de diversos metais causa interferência e competição entre estes, bem como o local de adsorção, em virtude da adsorção de competição entre esses contaminantes. Os coeficientes de partição e os coeficientes de remoção seletiva para os hidrogéis St-g-PNaAc e St-g-PNaAc/10% NWCs para íons Pb(II) foram maiores do que para íons Cu(II).
Agradecimentos
Os autores agradecem à FUNCAP (BP5-0197-00169.01.00/22), ao CNPq e a UEVA pelo apoio financeiro.
Referências
AGARWAL, B.; THAKUR, P. K.; BALOMAJUMDER, C. Use of Iron-Impregnated Granular Activated Carbon for Co-Adsorptive Removal of Phenol and Cyanide: Insight Into Equilibrium and Kinetics. Chemical Engineering Communications, v. 200, n. 9, p. 1278–1292, 2013.
ELAZZOUZI-HAFRAOUI, S.; NISHIYAMA, Y.; PUTAUX, J.L.; HEUX, L.; DUBREUIL, F.; ROCHAS, C. The shape and size distribution of crystalline nanoparticles prepared by acid hydrolysis of native cellulose. Biomacromolecules, v.9, p.57–65, 2008.
FEBRIANTO, J.; KOSASIH, A. N.; SUNARSO, J.; JU, Y.; INDRASWATI, N.; ISMADJI, S. Equilibrium and kinetic studies in adsorption of heavy metals using biosorbent: A summary of recent studies. Journal of Hazardous Materials, v. 162, p. 616-645, 2009.
GOMES, R. F.; AZEVEDO, A. C. N.; PEREIRA, A. G. B.; MUNIZ, E. C.; FAJARDO, A. R.; RODRIGUES F. H. A. Fast dye removal from water by starch-based nanocomposites. Journal of Colloid and Interface Science, v.454, p.200-209, 2015.
HU, C.; ZHU, P.; CAI, M.; HU, H.; FU, Q. Comparative adsorption of Pb(II), Cu(II) and Cd(II) on chitosan saturated montmorillonite: Kinetic, thermodynamic and equilibrium studies. Appl. Clay Sci. v.143, p.320–326, 2017.
LIU, M.; LIU, Y.; SHEN, J.; ZHANG, S.; LIU, X.; CHEN, X.; MA, Y.; REN, S.; FANG, G.; LI, S. Simultaneous removal of Pb(II), Cu(II) and Cd2+ ions from wastewater using hierarchical porous polyacrylic acid grafted with lignin. Journal of Hazardous Materials, v.392, p.122208, 2020.
MELO, B. C.; PAULINO, F. A. A.; CARDOSO, V. A.; PEREIRA, A. G. B.; FAJARDO, A. R.; RODRIGUES, F. H. A. Cellulose nanowhiskers improve the methylene blue adsorption capacity of chitosan-g-poly(acrylic acid) hydrogel. Carbohydrate Polymers, v.181, p.358, 2018.
RODRIGUES, F. H. A.; MAGALHÃES, C. E. C., MEDINA, A.L.; FAJARDO, A. R. Hydrogel composites containing nanocellulose as adsorbents for aqueous removal of heavy metals: design, optimization, and application. Cellulose, v. 26, p. 9119-9133, 2019.
SATYAMURTHY, P.; JAIN, P.; BALASUBRAMANYA, R.H.; VIGNESHWARAN, N. Preparation and characterization of cellulose nanowhiskers from cotton fibres by controlled microbial hydrolysis. Carbohydrate Polymer, v.83, p.122–129, 2011.
SPAGNOL C.; RODRIGUES, F.H.A.; PEREIRA, A.G.B.; FAJARDO, A.R.; RUBIRA, A.F.; MUNIZ, E.C. Superabsorbent hydrogel nanocomposites based on starch-g-poly(sodium acrylate) matrix filled with cellulose nanowhiskers. Cellulose, v.19, p.1225, 2012a.
SPAGNOL, C.; RODRIGUES, F.H.A.; PEREIRA, A.G.B.; FAJARDO, A.R.; RUBIRA, A.F.; MUNIZ, E. C. Superabsorbent hydrogel composite made of cellulose nanofibrils and chitosan-g-poly(acrylic acid). Carbohydrate Polymers, v. 87, p.2038, 2012b.
SEGAL, L.; CREELY, J.J.; MARTIN, A.E.; CONRAD, C.M. An empirical method for estimating the degree of crystallinity of native cellulose using the X-ray diffractometer. Textile Research Journal, v.29, p.786–794, 1959.
SEKHAR, K. C.; KAMALA, C. T.; CHARY, N. S.; ANJANEYULU, Y. Removal of heavy metals using a plant biomass with reference to environmental control, International Journal of Mineral Processing, v.68, p.37-45, 2003.
SELLAOUI, L.; SOETAREDJO, F. E.; ISMADJI, S.; BONILLA-PETRICIOLET, A.; BELVER, C.; BEDIA, J.; BEN LAMINE, A.; ERTO, A. Insights on the statistical physics modeling of the adsorption of Cd2+ and Pb(II) ions on bentonite-chitosan composite in single and binary systems. Chemical Engineering Journal, v.354, p.569–576, 2018.
VIJAYARAGHAVAN, K.; TEO, T.T.; BALASUBRAMANIAN, R.; JOSHI, U.M. Application of Sargassum biomass to remove heavy metal ions from synthetic multi-metal solutions and urban storm water runoff. J. Hazard. Mater. 164, 1019–1023, 2009.
ZAURO, S. A.; VISHALAKSHI, B. Pectin graft copolymer-montmorillonite composite: Synthesis, swelling and divalent metal ion adsorption. Separation Science and Technology, v.53, p.14, 2018.