Autores
Martins Ferreira, J.L. (UERJ) ; Silva Quirgo dos Reis, A.B. (UERJ) ; de Oliveira Domingos, J.L. (UERJ) ; Dias Senra, J. (UERJ)
Resumo
Células solares sensibilizadas por corantes são uma classe de dispositivos que
envolvem a conversão de energia luminosa em energia elétrica a partir do efeito
fotovoltaico, com o uso de compostos orgânicos como absorvedores. Essa abordagem
possui vantagens, tais como: menor custo, leveza, flexibilidade, facilidade na
modulação das propriedades de transporte de carga, dentre outras. Sistemas
conjugados baseados no cerne do carbazol têm sido promissores quando empregados
como sensibilizadores na geração da fotocorrente. O trabalho tem como objetivo a
síntese de novos compostos contendo os cernes carbazólicos, por meio de reações
de Suzuki-Miyaura. Com o emprego de condições reacionais atrativas foi observado
altos rendimentos (>90%) de 3,6-diarilcarbazóis contendo fenil, ttiofenil e
tiofenil
Palavras chaves
9H-carbazol; ácidos arilborônicos; nanopartículas de Pd
Introdução
Os combustíveis fósseis foram responsáveis pelo funcionamento da máquina a vapor
nas indústrias têxteis da Inglaterra, ocasionando o surgimento da Primeira
Revolução Industrial (1760 – 1850). Esse período foi marcado por inúmeras
transformações econômicas e sociais no mundo, mas principalmente no continente
europeu. Os combustíveis fósseis são formados a partir da decomposição de
matéria orgânica. Entretanto, é um processo que acarreta milhares de anos para
acontecer. Por isso, são considerados fontes não renováveis, ainda que continuem
sendo formados na natureza. A sociedade, desde a Primeira Revolução Industrial,
tem utilizado os combustíveis fósseis para sanar a demanda de energia. Contudo,
com a redução e a escassez cada vez maior das reservas de combustíveis fósseis,
foi necessário investir no desenvolvimento de fontes renováveis e “limpas” de
energia, já que a queima de combustíveis fósseis produz o anidrido carbônico
(CO2), o metano (CH4) e o óxido nitroso (N2O), que são “gases estufa”, ou seja,
responsáveis pelo efeito estufa e, consequentemente, pelo aquecimento global. O
9H-carbazol, frequentemente denominado de carbazol, é uma molécula tricíclica
que pode ser obtida a partir de fontes naturais. Foi obtida pela primeira vez
através da fração de antraceno de alcatrão de carvão destilado. Os químicos e
biólogos possuem grande interesse pelos carbazóis em virtude das suas
propriedades farmacológicas. Neste trabalho, serão descritos resultados
preliminares obtidos a partir das reações de acoplamento cruzado de Suzuki
Miyaura entre ácidos arilborônicos e o substrato 3,6-diiodo-9H-carbazol na
presença de carbonato de potássio (K2CO3) e das PdNPs estabilizadas por PEG-
300.
Material e métodos
Síntese dos produtos de Suzuki-Miyaura na presença de PdNPs em refluxo (24h) e
micro-ondas (2h):
Em um balão de fundo redondo de 10 mL equipado com um condensador de refluxo
foram adicionados 0,25 mmol (0,104 g) de 3,6-diiodo-9H-carbazol, 0,5 mmol de
R1B(OH)2, 1,0 mmol de carbonato de potássio (0,138 g) e o catalisador
previamente preparado [4,0 mL de PEG-300 e 4,0 mol% de Pd2(dba)3 (9,15x10-3 g)].
A mistura foi agitada e aquecida a 95 ºC por 24 horas.
A reação foi acompanhada por CCF, utilizando hexano/acetato de etila (9:1) e
revelação UV. Após esse tempo, o meio reacional foi extraído com água/acetato de
etila (3:1), 3x20 mL. A fase orgânica foi seca com sulfato de sódio anidro e
evaporada sob pressão reduzida.
Em virtude das condições de refluxo prolongadas (24 horas), as reações foram
realizadas no reator de micro-ondas, nas mesmas condições reacionais descritas
anteriormente. O meio reacional foi vertido em um tubo de vidro fechado de 10 mL
e a temperatura mantida constante (95 ºC) durante o período de 2 horas, com a
potência variando entre 6 W e 14 W. A mistura reacional obtida foi extraída da
mesma forma que nas condições de refluxo.
As conversões e rendimentos foram calculados a partir das áreas de cada pico
observado nos cromatogramas, seguindo as expressões abaixo:
Conversão (%) = ∑área dos produtos / ∑área dos produtos + área do reagente
halogenado.
Rendimento (%) = ∑área do produto desejado/ ∑área dos produtos + área do
reagente halogenado.
Resultado e discussão
As estruturas dos ácidos borônicos empregados nas reações de acoplamento de
cruzado de Suzuki-Miyaura, e os produtos esperados em cada caso, estão descritas
no Figura 1: O grupo de pesquisa tem explorado o uso de PdNPs em reações de
acoplamento cruzado com substratos halogenados comerciais [1,2] e com o uso do
3,6-diiodo-9H-carbazol [3] na reação de acoplamento de Suzuki-Miyaura. Com o
intuito de preparar carbazois simétricos funcionalizados (π estendidos)
realizou-se as reações de acoplamento cruzado de Suzuki Miyaura, empregando o
3,6-diiodo-9H-carbazol nas condições descritas anteriormente. Os resultados
obtidos preliminarmente em refluxo e micro-ondas estão descritos na Figura 2. As
seletividades para os produtos diarilados foram observadas em maior extensão,
apesar de alguns valores baixos. O uso do PEG-300 como solvente nas reações de
acoplamento cruzado de Suzuki-Miyaura deste trabalho tem por objetivo promover a
troca de solventes orgânicos de alto custo e inflamáveis por um solvente de
baixo custo, que não polui o meio ambiente e reciclável, que permite que o
sistema catalítico seja reutilizado por até 10 ciclos. Contudo, testes
preliminares com a adição de água aumentaram o rendimento dos produtos das
entradas 1, 4 e 7, sob irradiação de micro-ondas (100 ºC). Esse fato pode estar
relacionado à utilização da base inorgânica K2CO3, cuja maior solubilidade na
presença de água pode contribuir para um maior percentual de íons OH- no meio
reacional. A caracterização dos produtos por RMN de H encontram-se em análise.
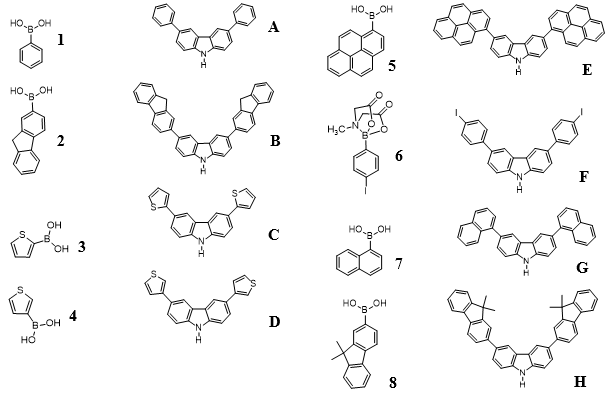
Estrutura dos ácidos borônicos utilizados no trabalho e dos produtos esperados.
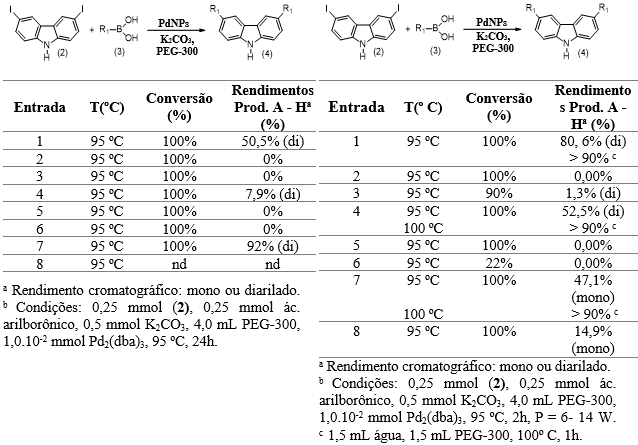
Resultados preliminares da reação de Suzuki-Miyaura nas condições descritas em aquecimento convencional e MW, respectivamente.
Conclusões
A síntese de carbazóis 3,6-funcionalizados (π estendidos), através de reações de
Suzuki-Miyaura catalisadas por PdNPs em PEG-300, apresentaram maior eficiência
em sistemas contendo maior % de água (H2O:PEG-300, 1:1), a 100°C por 1h. O estudo
de outras variáveis do sistema catalítico está em andamento.
Agradecimentos
Os autores agradecem ao CNPq, FAPERJ e CAPES pelo apoio financeiro.
Referências
[1] J. D. Senra, L. F. B. Malta, R. C. Michel, Y. Cordeiro, R. A. Simao, A. B. C. Simas, L. C. S. Aguiar, J. Mater. Chem. 21 (2011) 13516.
[2] J. D. Senra, L. F. B. Malta, R. C. Michel, A. B. C. Simas, L. C. S. Aguiar, O. A. C. Antunes, Adv. Synth. Catal. 351 (2009) 2411.
[3] M. S. Arvelos, A.C. Silva, A. L. F de Souza, C. A. Achete, T. L. Vasconcelos, E. Robertis, B. S. Archanjo, L. C. S. Aguiar, L. F. B. Malta, J. D. Senra, ChemistrySelect, 3(33), 9725–9730, 2018.
















