Autores
Ramos, H. (UFAM) ; Lima, M. (INPA) ; Santos, H. (UFAM) ; Nascimento, C. (INPA) ; Duarte, P. (UFAM) ; Lima, J. (UFAM)
Resumo
Os estudos com serragem da madeira de Dalbergia spruceana Benth foram
disponibilizadas para investigação fitoquímica e avaliação da atividade
inseticida. Após os fracionamentos cromatográficos e análise por RMN, os
objetivos foram alcançados, resultando na obtenção dos esteroides β-sitosterol
(1a), estigmasterol (1b) e um isoflavonoide majoritária, Maackiain (2) no
extrato hexânico. Já no extrato metanólico um isopropanoide foi identificado
como elemicina (3). Considerando o alto potencial biológico das substâncias
pertencente à classe dos flavonoides, foi realizado ensaio inseticida de
mortalidade com a Maackiain (2) frente às ninfas de B. tabaci. (mosca branca), a
qual apresentou atividade de 35% de mortalidade e 7% superior ao produto
comercial utilizado para o controle de mosca branca.
Palavras chaves
Fitoquímica; RMN; Fabaceae
Introdução
A espécie Dalbergia spruceana Benth (Fabaceae) conhecida popularmente no Brasil
como Jacarandá-do-Pará é encontrada em toda região Norte (SANTOS, 1987; SOUZA,
2012). Do ponto de vista econômico é uma madeira de boa qualidade, na qual é
utilizada na fabricação de móveis, objetos de decoração, adornos, caixas e
estojos (RIZZINI, 1978; GONÇALVES et al., 2012). Porém, do ponto de vista
químico é considerada uma madeira carente de estudos científicos, pois há poucos
relatos publicados na literatura. Dessa forma, o objetivo deste trabalho foi
direcionado para estudos de investigação fitoquímica e biológica das serragens
geradas na produção de artefatos da espécie. A proposta de aliar os estudos
fitoquímicos de Dalbergia spruceana com busca de atividade inseticida é devido
ao gênero Dalbergia, bem como vários outros de Fabaceae apresentarem em sua
composição química os flavonoides. Essa classe de substâncias é relatada na
literatura pelo alto potencial biológico, entre elas, o inseticida (ADONIAS,
2020; DALARMI, et al., 2015; SLETOZER, et al., 2021). Nesse sentido, foi
avaliado o potencial de mortalidade do composto majoritário da madeira, contra
as ninfas de B. tabaci, utilizando Torre de Potter como recurso nas aplicações
de 1mL de substância/folha.
Material e métodos
Os extratos de D. spruceana foram obtidos a partir de 1,1 Kg de serragem,
fornecendo um rendimento de 0,065% de (hexânico - DSH) e 3,9% (metanólico -
DSM). O extrato DSH (0,6 g) foi fracionado em sílica gel 60, fornecendo 23
frações. A fração 8 passou em novo fracionamento em sílica flash, resultando nas
substâncias β-sitosterol (1a) e stigmasterol (1b). Enquanto a fração 16 foi
selecionada para separação em placa preparativa de sílica gel 60 em vidro (20x10
cm), fornecendo a substância 2. No extrato DSM (19 g) fracionado em sílica
filtrante forneceu 90 frações. Desta, a subtração 52 resultou no isolado 2,
novamente. Em contrapartida, a 46 foi inserida em cromatoplaca preparativa com
sílica 60 (20x10 cm), concedendo o composto 3.
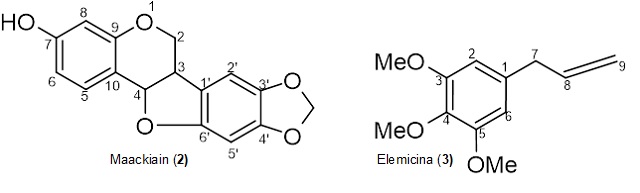
As análises de RMN 1D e 2D possibilitaram na identificação Maackiain (2) e
elemicina (3), fig. 1. O espectro de RMN 1H de (2) apresentou sinais
característicos de anel aromático em δ (7,31-6,40), metilenodioxi em δ (5,93),
hidrogênios do anel C em δ 3,57 (m, H-3), 3,65 (t, H-2), 4,29 (dd, H-2) e 5,50
(d, H-4). No RMN de 13C observou-se sinais aromáticos em δ (158,8-93,0),
metilenodioxi δ 101,2 e os carbonos do anel C apresentaram sinais em 66,4 (C-2),
40,4 (C-3) e 78,9 (C-4). Já na substância (3), no espectro de RMN foi
evidenciado um sinal de aromáticos duplicados em δ 6,43, metilênicos em δ 3,36
(H-7) e 5,0 e 5,15 (H-9), olefínico em 5,97 (H-8) e três metoxilas em δ 3,87-
3,84. No 13C RMN os sinais aromáticos foram encontrados em (105,4-153,1) e a
dupla foi observada em 137,22 (C-8) e 116,03 (C-9). Nos resultados de avaliação
inseticida para substância 2, a mortalidade de 35% foi superior ao produto
padrão, Evidence WG700 com 28,33%. Corroborando com a literatura que os
isoflavonoides atuam como defensores das plantas (ANDERSEN et al., 2006)
Resultado e discussão
Os extratos de D. spruceana foram obtidos a partir de 1,1 Kg de serragem,
fornecendo um rendimento de 0,065% de (hexânico - DSH) e 3,9% (metanólico -
DSM). O extrato DSH (0,6 g) foi fracionado em sílica gel 60, fornecendo 23
frações. A fração 8 passou em novo fracionamento em sílica flash, resultando nas
substâncias β-sitosterol (1a) e stigmasterol (1b). Enquanto a fração 16 foi
selecionada para separação em placa preparativa de sílica gel 60 em vidro (20x10
cm), fornecendo a substância 2. No extrato DSM (19 g) fracionado em sílica
filtrante forneceu 90 frações. Desta, a subtração 52 resultou no isolado 2,
novamente. Em contrapartida, a 46 foi inserida em cromatoplaca preparativa com
sílica 60 (20x10 cm), concedendo o composto 3.
As análises de RMN 1D e 2D possibilitaram na identificação Maackiain (2) e
elemicina (3). O espectro de RMN 1H de (2) apresentou sinais característicos de
anel aromático em δ (7,31-6,40), metilenodioxi em δ (5,93), hidrogênios do anel
C em δ 3,57 (m, H-3), 3,65 (t, H-2), 4,29 (dd, H-2) e 5,50 (d, H-4). No RMN de
13C observou-se sinais aromáticos em δ (158,8-93,0), metilenodioxi δ 101,2 e os
carbonos do anel C apresentaram sinais em 66,4 (C-2), 40,4 (C-3) e 78,9 (C-4).
Já na substância (3), no espectro de RMN foi evidenciado um sinal de aromáticos
duplicados em δ 6,43, metilênicos em δ 3,36 (H-7) e 5,0 e 5,15 (H-9), olefínico
em 5,97 (H-8) e três metoxilas em δ 3,87-3,84. No 13C RMN os sinais aromáticos
foram encontrados em (105,4-153,1) e a dupla foi observada em 137,22 (C-8) e
116,03 (C-9). Nos resultados de avaliação inseticida para substância 2, a
mortalidade de 35% foi superior ao produto padrão, Evidence WG700 com 28,33%.
Corroborando com a literatura que os isoflavonoides atuam como defensores das
plantas (ANDERSEN e MARKHAM, 2006).
Conclusões
O estudo com serragem de D.spruceana, forneceu conhecimentos fitoquímicos da
madeira e ao mesmo tempo evidenciou a importância de agregar valor aos resíduos
madeireiros, uma vez que, a substância (2) isolada mostrou resultados promissores
ao combater ninfas de Bemisia tabaci (mosca branca).
Agradecimentos
Ao Laboratório de Química de Produtos Naturais (LQPN), FAPEAM pelo apoio
financeiro e Central Analítica do Laboratório Temático de Química de Produtos
Naturais (CALTPQN) pelas análises de RMN.
Referências
ADONIAS, A.; LUCIVANIA, R.; RENATO, P.; JUREMA, S.; MARIANA, H. 2019. Flavonoids identification of Machaerium acutifolium by ESI-MS. 7th Brazilian Conference on Natural Product/ XXXIII RESEM, 1: 117-466.
DALARMI, L.; SILVA, C.; OCAMPOS, F.; OLIVEIRA, D.; Burci,; MIGUEL, O.; ZANIN.S.; MIGUEL, M. 2015. Evolution of phytochemical research applied the biological activities of the genus threatened with extinction Dalbergia.Visão Acadêmica,16: 1.
FERREIRA, T.; HADDI, K.; CORRÊA, R. et al. 2019. Prolonged mosquitocidal activity of Siparuna guianensis essential oil encapsulated in chitosan nanoparticles. PLOS Neglected Tropical Diseases, 13: 8.
SPLETOZER, A., SANTOS, C., SANCHES, L., GARLET, J. 2021. Plantas com potencial inseticida: enfoque em espécies amazônicas. Ciência Florestal, 31: 974-997.
GONÇALVES, C.; GAM, V.; OLIVEIRA, A.; OLIVEIRA, C.; ARAÚJO, C.; ALMEIDA, S. 2012. Aspectos mercadológicos dos produtos não madeireiros na economia de Santarém-Pará, Brasil. Floresta e Ambiente,19: 9-16.
HOROWITZ, R.; GHANIM, M.; RODITAKIS, E.; NAUEN, R.; ISHAAYA, I. 2020. Insecticide resistance and its management in Bemisia tabaci species. J. Pest Sci, 93: 893–910.
I.DARREN GRICE,1 KELLY L. ROGERS,2, 3 AND LYN R. 2011. Griffiths Isolation of Bioactive Compounds That Relate to the Anti-Platelet Activity of Cymbopogon ambiguus, 8: 46134.
J. T. COOK, W. D. OLLIS, I. O. SUTHERLAND, O. R. GOTTLIEB. 1978. Phytochemistry, v. 17, 1419.
BRAVO, J; SAUVAIN, M. 2002. first bioguided phytochemical approach to cavanillesia aff. hylogeiton The Bolivian Journal Of Chemistry, 19: 1.
KANAKALA, S.; GHANIM, M. 2019. Global genetic diversity and geographical distribution of Bemisia tabaci and its bacterial endosymbionts. PLoS ONE, 14: 21.
MALINGA, N.; LAING, D. 2021. Efficacy of three biopesticides against cotton pests under field conditions in South Africa. Crop Prot., 145: 105-578.
SCHUTZE, X.; YAMAMOTO, T.; MALAQUIAS, B.; NARANJO, E. 2021. Network correlation to evidence the influence of Bemisia tabaci feeding in the photosynthesis and foliar sugar and starch composition in soybean. Doctoral Dissertation, University Sao Paulo, São Paulo, Brazil,13: 56.
















