Autores
Fonseca, E.K.B. (UNICAMP) ; Barros, A. (UNICAMP) ; Andrade, A.M. (UNICAMP) ; Mazali, I.O. (UNICAMP) ; Arruda, M.A.Z. (UNICAMP)
Resumo
A soja destaca-se entre os grãos mais cultivados mundialmente e a sua
importância econômica se deve a características como abundância e qualidade
nutricional. Atualmente a soja tem sido estudada em relação à toxicidade com
nanopartículas (NPs). Uma das NPs mais utilizadas são as de ouro (AuNPs), devido
às suas propriedades como ressonância plasmônica de superfície e baixa
toxicidade. Portanto, esse trabalho teve como objetivo caracterizar AuNPs, em
relação ao tamanho, à morfologia e à quantificação. Foi observada uma síntese
homogênea de AuNPs esféricas, com diâmetros médios de 16,8 nm, 17,08 nm e 14,9
nm através das técnicas TEM, DLS e spICP-MS, respectivamente. Além de uma
distribuição de tamanho uniforme, o que é necessário para desempenho preciso e
confiável em aplicações analíticas.
Palavras chaves
Nanopartículas de ouro; Ressonância plasmônica; spICP-MS
Introdução
A soja (Glycine max (L) Merril) destaca-se como um dos grãos mais cultivados
mundialmente, representando a quinta maior cultura mundial na produção agrícola
(LEOPOLD et al., 2022), e o Brasil ocupa o primeiro lugar como maior produtor
desse cultivar (CAMPOS et al., 2020). A importância econômica da soja se deve às
suas características como abundância, qualidade nutricional, propriedades
funcionais e baixo custo. No ramo alimentício, por exemplo, é altamente
utilizada por ser rica em proteínas, carboidratos, lipídeos e elementos
essenciais, e, dessa forma, é geralmente utilizada como ração para nutrição
humana e animal, além de ser, também, uma excelente fonte de óleo, utilizada na
produção de biodiesel e em outras aplicações industriais (CAMPOS et al., 2020;
FRACASSO et al., 2014; HERRERA-AGUDELO, MIRÓ e ARRUDA, 2017).
Com a demanda de produção, objetivando melhorar a qualidade, bem como
resistência às pragas e aumento da produtividade, surge nesse contexto a soja
transgênica (T). A mais conhecida, Roundup Ready® (RR), foi desenvolvida por
meio de modificação genética, ao receber o gene exógeno, cp4-EPSPS, tornando-a,
assim, mais produtiva e resistente a um dos herbicidas mais utilizados nessa
cultura: o glifosato (GALAZZI et al., 2019; HERRERA-AGUDELO, MIRÓ e ARRUDA,
2017).
A soja é uma excelente fonte de elementos essenciais incluindo Cálcio (Ca),
Cobre (Cu), Ferro (Fe), Magnésio (Mg), Manganês (Mn), Fósforo (P) e Zinco (Zn)
(HERRERA-AGUDELO, MIRÓ e ARRUDA, 2017), como macro e micronutrientes, e alguns
elementos não essenciais podem ser assimilados pela planta de forma semelhante
aos essenciais. Isso também ocorre com as nanopartículas (NPs). Devido a
alterações bioquímicas resultantes da assimilação ou liberação dos metais, as
NPs podem ser tóxicas, e, dessa forma, interferir na absorção dos nutrientes
pelas plantas (GALAZZI et al., 2019), (GALAZZI e ARRUDA, 2018). Dentre as NPs
mais utilizadas destacam-se as nanopartículas de ouro (AuNPs), que são
amplamente utilizadas em aplicação em diversas áreas. Sua importância deve-se às
características únicas e distintas, tais como: ser biocompatível, inerte, e,
especialmente, apresentar baixa toxicidade (OGAREV, RUDOI e DEMENT’EVA, 2018).
Além disso, nos últimos anos a soja tem sido estudada como um modelo para
estudos de toxicidade com nanopartículas (COMAN et al., 2019; LEOPOLD et al.,
2022), e o conhecimento sobre as propriedades desse cultivar, tanto convencional
quanto modificado geneticamente, faz-se cada vez mais necessário. Nesse sentido,
a caracterização ionômica desempenha um importante papel tanto na compreensão do
metabolismo vegetal de plantas transgênicas, quanto nos possíveis efeitos
associados a estresses bióticos, abióticos e exposição à NPs (ENFISSI et al.,
2021).
Com base em estudos realizados, Galazzi e Arruda (2018) destacam que quando se
comparam transgênicos e não-transgênicos há diferenças marcantes em termos de
assimilação de metais e sua homeostase , bem como na presença de
(metalo)proteínas e enzimas. Para isso, é primordial o emprego de técnicas de
separação, identificação e quantificação. Dentre estas, as mais utilizadas na
avaliação ionômica de plantas expostas tanto a elementos tóxicos, como NPs, está
a espectrometria de massas com plasma indutivamente acoplado (ICP-MS) (PESSÔA
et al., 2017).
Diante disso, e somado à limitação de informações que relacionam efeitos das
AuNPs com a soja, este trabalho justifica-se pela importância de conhecer as
possíveis diferenças, interações e efeitos das AuNPs, e tem como objetivo
principal caracterizar nanopartículas de ouro para, posteriormente, avaliar sua
interação em culturas de soja transgênica.
Material e métodos
A síntese das AuNPs foi realizada segundo o método descrito por Turkevich,
partindo-se de uma solução aquosa de ácido cloroáurico (HAuCl4) (DONG et al.,
2020; TURKEVICH, STEVENSON e HILLIER, 1951; WUITHSCHICK et al., 2015). Aqueceu-
se, até a ebulição, 25,00 mL de uma solução 0,5 mmol L-1 de HAuCl4 em um
erlenmeyer, sob agitação. Adicionou-se rapidamente 1,25 mL de solução 1% de
citrato de sódio e manteve-se a solução em ebulição, tampada e mantendo-se a
agitação. Após atingir a coloração vermelho intenso, o aquecimento do sistema
foi suspenso e a solução foi resfriada à temperatura ambiente. Em seguida, a
solução foi centrifugada por 1h a 8000 rpm.
O comportamento óptico das AuNPs foi estudado utilizando um espectrofotômetro de
absorção UV-Vis (Agilent, 8453), com cubeta de quartzo e 1 cm de caminho óptico.
A análise foi realizada utilizando a infraestrutura do laboratório multiusuário
do Instituto de Química da Unicamp. A imagem TEM das AuNPs foi registrada em
microscópio eletrônico Zeiss – Libra operando a 80 kV. A amostra foi preparada
secando diretamente a suspensão de nanopartículas sobre uma grade de cobre
revestida com filme de carbono. A análise de tamanho e distribuição de
partículas foi obtida utilizando um instrumento Malvern, modelo ZetasizerNano
Zs-Zen3600, equipado com um laser HeNe operando a 632,8 nm e um detector de
espalhamento a 173 graus.
A medição e quantificação das AuNPs sintetizadas foi realizada em um equipamento
Thermo iCAP TQ ICP-MS (Thermo Fisher Scientific, Bremen, Alemanha), equipado com
um nebulizador Micro Mist, uma câmara de pulverização ciclônica (ambos da Thermo
Fisher Scientific) e um amostrador automático ASX-560 (Teledyne CETAC
Technologies, Omaha, NE, EUA). O ICP-MS foi operado no modo single quadrupolo,
de detecção de partícula única, com as condições experimentais dispostas na
Tabela 1.
Soluções de trabalho foram preparadas medindo-se alíquotas de uma solução
intermediária de ouro, em cinco níveis de concentração de 10 a 30 ng L-1. Além
disso, para avaliar a seletividade do método foi utilizado um padrão de
nanopartículas de ouro de 30 nm (Gold Nanospheres 30 nm, Citrate, NanoXact™,
nanoComposix), contendo 1,8x1011 partículas mL-1.
A vazão de amostra (V) foi medida diariamente, e é definida como o volume de
amostra aspirado por unidade de tempo (minutos). V é calculada pela subtração do
volume inicial da amostra e o volume restante (final), após o tempo de aspiração
(120 s), com a rotação da bomba em -50 RPM. Realizou-se três medições e a vazão
de amostra foi determinada pela média dos resultados. Para o cálculo do número
de concentração de partículas (N), foi medida a eficiência de transporte (TE)
diariamente com padrão de Au, pelo método de tamanho e também pelo do número de
nanopartículas (PACE et al., 2011).
Resultado e discussão
As nanopartículas de ouro foram sintetizadas (Figura 1A) de acordo com o método
de Turkevich (TURKEVICH, STEVENSON e HILLIER, 1951). De modo geral, a forma mais
comum de sintetizar nanopartículas de ouro baseia-se na redução de um sal de
ouro que seja solúvel em água com um íon citrato. Nesse caso o sal utilizado foi
o ácido cloroáurico (HAuCl4), reduzido com citrato de sódio (Na3C6H5O7). Este,
além de ser um agente redutor, foi utilizado também como um estabilizador de
partículas (OGAREV, RUDOI e DEMENT’EVA, 2018; SANFELICE et al., 2016).
Observou-se rapidamente uma mudança na coloração da solução, passando de
amarelada, característica da solução de ácido cloroáurico, para avermelhada
(Figura 1A). A mudança da coloração para vermelho escuro é promovida pela adição
do citrato de sódio, devido à redução do Au3+ para Au0, confirmando a obtenção
das partículas de ouro em escala nanométrica (COURA et al., 2018; TURKEVICH,
STEVENSON e HILLIER, 1951). Além disso, a cor vermelho escuro das suspensões de
nanopartículas esféricas de ouro é explicada pela reflexão das ondas
eletromagnéticas das nanopartículas, teoria proposta por Mie, que é útil para
descrever as propriedades ópticas de partículas esféricas metálicas (OGAREV,
RUDOI e DEMENT’EVA, 2018).
As nanopartículas de ouro foram caracterizadas por UV-Vis, TEM, DLS e spICP-MS
(Figura 1). Na Figura 1B é ilustrado o espectro de extinção em função do
comprimento de onda para a suspensão coloidal de nanopartículas de ouro
esféricas, obtido através da espectroscopia na região do ultravioleta visível
(UV-Vis). Observa-se em 518 nm a banda plasmon característica para
nanopartículas de ouro esféricas, referente a oscilação coletiva de elétrons ao
interagir com a luz. Isso confirma a síntese de AuNPs, uma vez que, para
nanopartículas de ouro, o comprimento de onda de ressonância plasmônica de
superfície é cerca de 520 nm, que pode variar a depender do tamanho das
nanopartículas (OGAREV, RUDOI e DEMENT’EVA, 2018).
A imagem da Figura 1B refere-se a uma ilustração esquemática da interação da luz
com a partícula, mostrando o campo elétrico deslocado em função da luz.
Adicionalmente, a partir do espectro de extinção normalizado foi possível
estimar a concentração de Au° para a amostra sintetizada, de 0,83 mmol L-1.
A homogeneidade da síntese e a distribuição de tamanho das AuNPs foram
confirmadas por meio da caracterização por microscopia eletrônica de
transmissão, ilustrada na Figura 1C. Observa-se uma imagem TEM representativa
para AuNPs, bem como um padrão de morfologia esférica para as mesmas. A contagem
das nanopartículas foi realizada por meio do software ImageJ, calculando-se um
tamanho médio de 16,8 ± 2,1 nm de diâmetro, para um total de 550 nanopartículas.
A distribuição homogênea das nanopartículas pode ser observada por meio do
histograma de distribuição de tamanho, na Figura 1D.
Adicionalmente, a distribuição de tamanho e PdI foram determinadas a partir de
análises de DLS. Os resultados indicam a presença de partículas com tamanhos de
ca. 17,08 nm, de acordo com o pico representado na Figura 1E. Essa uniformidade
de pico corrobora com trabalho reportado na literatura para AuNPs (YUAN et al.,
2019). O resultado de PdI para a síntese foi de 0,383, o que indica que a
síntese proposta é monodispersa e pode ser observado pela microscopia realizada
conforme demonstrada na Figura 1C. O tamanho hidrodinâmico das nanopartículas
analisadas por DLS corrobora com o diâmetro médio determinado a partir do
histograma construído das imagens TEM (ver Figura 1D).
Os resultados da caracterização de tamanho e quantificação de padrão de ouro e
das nanopartículas sintetizadas foram obtidos por single-particle ICP-MS. Nas
Figuras 1F e 1G são apresentados os histogramas de distribuição de tamanho das
partículas, e as distribuições observadas indicam uma prevalência de partículas
com tamanhos médios de 27,6 e 14,9 nm para o padrão e para a síntese,
respectivamente.
Os limites de detecção de tamanho para o padrão e a síntese de AuNPs foram
obtidos por meio dos desvios-padrão de 20 brancos analisados e estão dispostos
na Tabela 2. Os dados foram tratados com auxílio de uma planilha disponibilizada
por Givelet et al. (2021). Os limites de detecção de tamanho representam os
menores tamanhos de partícula capazes de gerar sinais superiores ao ruído. Desse
modo, o método consegue detectar partículas de Au com diâmetros a partir de 9 e
9,5 nm para o padrão e para a síntese, respectivamente. O tamanho de partículas
determinado para o padrão corrobora com o valor informado pelo fabricante, igual
a 92% para o tamanho de 30 nm.
O tamanho das partículas presentes nas suspensões analisadas, bem como as
concentrações estão dispostas na Tabela 2. O número de concentração de
partículas mL-1 (N) é obtido a partir do número de partículas (n) determinado
para cada faixa de tamanho, considerando tanto o tempo da análise (ta) quanto o
volume de suspensão aspirado nesse tempo (F), de acordo com a Equação 1 (BAZILIO
et al., 2021).
(Equação 1)
Não só as nanopartículas necessárias devem ser de tamanho e morfologia precisos,
mas também devem ter uma distribuição de tamanho extremamente estreita para
produzir um desempenho preciso e confiável (DONG et al., 2020).
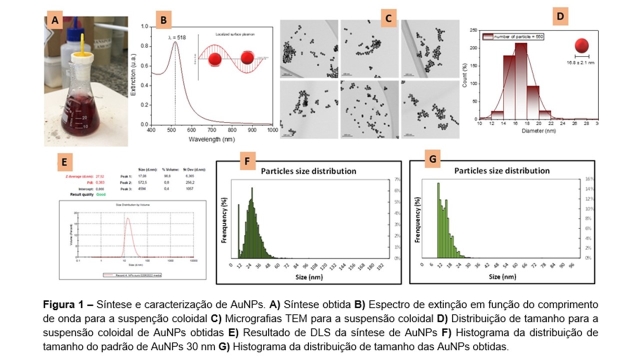
Síntese e caracterização de nanopartículas de ouro (AuNPs)

Conclusões
As nanopartículas de ouro sintetizadas pelo método de Turkevich foram
caracterizadas por diferentes técnicas, para estudo do tamanho, morfologia, e, por
fim, quantificadas. Os resultados corroboram para síntese homogênea de AuNPs, com
morfologia esférica e distribuição de tamanho uniforme, o que é adequado para
aplicação analítica em culturas de plantas, como a soja por exemplo.
A perspectiva desse trabalho é aplicar as nanopartículas de ouro caracterizadas,
em culturas de sojas transgênicas, e, posteriormente estudar, por meio de
avaliação ionômica, possíveis diferenças, interações e efeitos das AuNPs com a
soja.
Agradecimentos
Os autores agradecem à CAPES, pela concessão de bolsa para a aluna EKBF (processo
88887.653200/2021-00), à CNPq e FAPESP.
Referências
BAZILIO, F.; SILVA, C.; SANTOS, L.; VICENTINI, S.; JACOB, S.; ABRANTES, S. DETECÇÃO E QUANTIFICAÇÃO DE NANOPARTÍCULAS DE PRATA POR SPICP-MS. Química Nova, 2021.
CAMPOS, B. K. DE; GALAZZI, R. M.; SANTOS, B. M. DOS; BALBUENA, T. S.; SANTOS, F. N. DOS; MOKOCHINSKI, J. B.; EBERLIN, M. N.; ARRUDA, M. A. Z. Comparison of generational effect on proteins and metabolites in non-transgenic and transgenic soybean seeds through the insertion of the cp4-EPSPS gene assessed by omics-based platforms. Ecotoxicology and Environmental Safety, v. 202, n. June, 2020.
COMAN, V.; OPREA, I.; LEOPOLD, L. F.; VODNAR, D. C.; COMAN, C. Soybean Interaction with Engineered Nanomaterials: A Literature Review of Recent Data. Nanomaterials, v. 9, n. 9, p. 1248, 3 set. 2019.
COURA, M.; ARROYOS, G.; CORREIA, L.; FREM, R. COMO OBTER NANOPARTÍCULAS DE OURO USANDO SUCO DE LIMÃO? Química Nova, 2018.
DONG, J.; CARPINONE, P. L.; PYRGIOTAKIS, G.; DEMOKRITOU, P.; MOUDGIL, B. M. Synthesis of Precision Gold Nanoparticles Using Turkevich Method. KONA Powder and Particle Journal, v. 37, p. 2020011, 10 jan. 2020.
ENFISSI, E. M. A.; DRAPAL, M.; PEREZ-FONS, L.; NOGUEIRA, M.; BERRY, H. M.; ALMEIDA, J.; FRASER, P. D. New plant breeding techniques and their regulatory implications: An opportunity to advance metabolomics approaches. Journal of Plant Physiology, v. 258–259, n. January, p. 153378, 2021.
FRACASSO, A. F.; PERUSSELLO, C. A.; HAMINIUK, C. W. I.; JORGE, L. M. M.; JORGE, R. M. M. Hydration kinetics of soybeans: Transgenic and conventional cultivars. Journal of Cereal Science, v. 60, n. 3, p. 584–588, 2014.
GALAZZI, R. M.; ARRUDA, M. A. Z. Evaluation of changes in the macro and micronutrients homeostasis of transgenic and non-transgenic soybean plants after cultivation with silver nanoparticles through ionomic approaches. Journal of Trace Elements in Medicine and Biology, v. 48, n. December 2017, p. 181–187, 2018.
GALAZZI, R. M.; LOPES JÚNIOR, C. A.; LIMA, T. B. DE; GOZZO, F. C.; ARRUDA, M. A. Z. Evaluation of some effects on plant metabolism through proteins and enzymes in transgenic and non-transgenic soybeans after cultivation with silver nanoparticles. Journal of Proteomics, v. 191, n. August 2017, p. 88–106, 2019.
GIVELET, L.; TRUFFIER-BOUTRY, D.; NOËL, L.; DAMLENCOURT, J.-F.; JITARU, P.; GUÉRIN, T. Optimisation and application of an analytical approach for the characterisation of TiO2 nanoparticles in food additives and pharmaceuticals by single particle inductively coupled plasma-mass spectrometry. Talanta, v. 224, p. 121873, mar. 2021.
HERRERA-AGUDELO, M. A.; MIRÓ, M.; ARRUDA, M. A. Z. In vitro oral bioaccessibility and total content of Cu, Fe, Mn and Zn from transgenic (through cp4 EPSPS gene) and nontransgenic precursor/successor soybean seeds. Food Chemistry, v. 225, p. 125–131, 2017.
LEOPOLD, L. F. et al. The effect of 100–200 nm ZnO and TiO2 nanoparticles on the in vitro-grown soybean plants. Colloids and Surfaces B: Biointerfaces, v. 216, p. 112536, ago. 2022.
OGAREV, V. A.; RUDOI, V. M.; DEMENT’EVA, O. V. Gold Nanoparticles: Synthesis, Optical Properties, and Application. Inorganic Materials: Applied Research, v. 9, n. 1, p. 134–140, 27 jan. 2018.
PACE, H. E.; ROGERS, N. J.; JAROLIMEK, C.; COLEMAN, V. A.; HIGGINS, C. P.; RANVILLE, J. F. Determining Transport Efficiency for the Purpose of Counting and Sizing Nanoparticles via Single Particle Inductively Coupled Plasma Mass Spectrometry. Analytical Chemistry, v. 83, n. 24, p. 9361–9369, 15 dez. 2011.
PESSÔA, G. DE S.; LOPES JÚNIOR, C. A.; MADRID, K. C.; ARRUDA, M. A. Z. A quantitative approach for Cd, Cu, Fe and Mn through laser ablation imaging for evaluating the translocation and accumulation of metals in sunflower seeds. Talanta, v. 167, n. February, p. 317–324, 2017.
SANFELICE, R. C.; PAVINATTO, A.; GONÇALVES, V. C.; CORREA, D. S.; MATTOSO, L. H. C.; BALOGH, D. T. Synthesis of a nanocomposite containing a water-soluble polythiophene derivative and gold nanoparticles. Journal of Polymer Science Part B: Polymer Physics, v. 54, n. 13, p. 1245–1254, 1 jul. 2016.
TURKEVICH, J.; STEVENSON, P. C.; HILLIER, J. A study of the nucleation and growth processes in the synthesis of colloidal gold. Discussions of the Faraday Society, v. 11, p. 55, 1951.
WUITHSCHICK, M.; BIRNBAUM, A.; WITTE, S.; SZTUCKI, M.; VAINIO, U.; PINNA, N.; RADEMANN, K.; EMMERLING, F.; KRAEHNERT, R.; POLTE, J. Turkevich in New Robes: Key Questions Answered for the Most Common Gold Nanoparticle Synthesis. ACS Nano, v. 9, n. 7, p. 7052–7071, 28 jul. 2015.
















