Autores
Carvalho, E.L. (Pontifícia Universidade Católica do Rio de Janeiro) ; Peñafiel, M.J.P. (Pontifícia Universidade Católica do Rio de Janeiro) ; Aucélio, R.Q. (Pontifícia Universidade Católica do Rio de Janeiro)
Resumo
Quatro sondas fotoluminescentes foram
avaliadas para a quantificação de putrescina
usando pontos quânticos de grafeno (GQDs)
produzidos por fusão e hidro-esfoliação.
Diferentes GQDs fotoluminescentes foram
preparados usando ácido cítrico como
precursor, sozinho ou misturado com outros
compostos contendo heteroátomos (N e/ou
S) visando funcionalização da nanoestrutura,
no caso a tiouréia (TU), a ureia (U)
e a glutationa reduzida (GSH). Entre os
trabalhos futuros encontra-se o ajuste das
condições experimentais para melhorar a
resposta analítica e obter parâmetros
analíticos de mérito que permitam a aplicação
do método em amostra de carne
bovina, associando uma estratégia para obter
seletividade na determinação.
Palavras chaves
Putrescina; Sondas fotoluminescentes; Pontos quânticos de grafe
Introdução
A putrescina (1,4 diaminobutano) faz parte de
um grupo de bases orgânicas
nitrogenadas de baixo peso molecular
denominadas aminas biogênicas, que são
encontradas no corpo humano, em animais,
plantas e microrganismos. Como
consequência elas são encontradas em
alimentos, tais como carnes bovinas,
suínas, de frango, pescados, ovos, cogumelos,
produtos à base de leite, vegetais
fermentados, produtos de soja, bebidas como
cervejas e vinhos, dentre outros
(ÖZOGUL; ÖZOGUL, 2019).
Apesar de participar de vários processos
metabólicos importantes - como o ciclo
celular - a intoxicação ocasionada por uma
dieta rica em alimentos com
putrescina pode ocasionar hipotensão, tétano,
paresia das extremidades,
bradicardia e ainda pode potencializar a
intoxicação de outras aminas biogênicas
(SHALABY, 1996). Além disso, a putrescina - e
outras aminas biogênicas - são
marcadores químicos para o sistema olfativo
indicando estágio de decomposição em
tecidos e contaminação bacteriana nas carcaças
(HUSSAIN et al, 2013).
Sendo assim, é possível apontar a putrescina
como indicadores de qualidade de
alimentos e estabelecer o controle do acúmulo
em diversos tipos de produtos
alimentícios, visto que o excesso pode afetar
a saúde humana. Apesar disso, não
existe uma legislação específica estabelecendo
os limites permitidos de cada
amina biogênica em alimentos. No Brasil, a
legislação regulamenta apenas a
histamina em pescados frescos e seus
derivados, limitando a concentração máxima
em 100 mg L-1 (BRASIL, 1997).
Existem diversos métodos analíticos para a
quantificação de aminas biogênicas. A
cromatografia líquida de alta eficiência
(HPLC) com derivatização química (pré
ou pós-coluna) é muito citada na literatura
para a separação e quantificação
dessas aminas em alimentos (ÖNAL, 2007). No
entanto, os métodos baseados no HPLC
apresentam alto custo operacional relativo e
exige muito rigor na preparação das
amostras para não sobrecarregar as colunas de
separação.
Atualmente, os nanomateriais de carbono,
incluindo os ditos pontos quânticos de
carbono (CQDs) e de grafeno (GQDs), estão
sendo usados em aplicações para a
segurança alimentar (SHI et al, 2019; ZHANG et
al, 2022). Os CQDs e GQDs são
materiais muito atraentes devido a sua alta
biocompatibilidade, baixa toxicidade
relativa e propriedades ópticas peculiares.
Além disso, põem ser produzidos por
diversas estratégias, inclusive algumas muito
simples, gerando nanomaterias que
se estabilizam coloidalmente em água,
produzindo intensa fotoluminescência,
larga faixa de extinção óptica e propriedades
redox interessantes (NGAFWAN et
al, 2022).
O presente trabalho se propõe em apresentar um
estudo visando avaliar o
potencial dos pontos quânticos de grafeno
(GQDs) como sondas analíticas
fotoluminescentes para a quantificação da
amina biogênica putrescina. Quatro
dispersões de GQDs em dispersões coloidais
aquosas produzidos por fusão e hidro-
esfoliação foram analisadas para compara a
sensibilidade de cada uma à presença
de putrescina. Diferentes GQDs
fotoluminescentes foram preparados usando
ácido cítrico como precursor, sozinho ou
misturado com outros compostos contendo
heteroátomos (N e/ou S) visando
funcionalização da nanoestrutura, no caso a
tiouréia (TU), a ureia (U) e a glutationa
reduzida (GSH).
Material e métodos
As medições de fotoluminescência foram feitas
em um espectrômetro de
luminescência modelo LS 55 (Perkin-Elmer)
usando velocidade de varredura de 1000
nm min-1, com banda espectral passante de 10
nm. Cubetas de quartzo de
comprimento de caminho óptico de 1 cm foram
usadas para condicionar as sondas no
momento da medição. Os GQDs foram preparados
utilizando a hidro-esfoliação do
ácido cítrico (1,0 g) sozinho ou na presença
de outros precursores orgânicos
(0,3 g) fundidos. Os outros precursores foram
tiouréia (TU), ureia (U) ou
glutationa (GSH), todos da Sigma Aldrich
(EUA). A preparação foi adaptada de
Franco (2019), em que o precursor sólido foi
aquecido em um béquer, a cerca de
240ºC, até que o material fundido atingisse
uma coloração marrom clara. Em
seguida, a massa pirolisada foi despejada em
um béquer contendo água ultrapura
(18,2MΩ cm) na temperatura ambiente, obtida do
ultra purificador Milli-Q
gradient A10 (Millipore, EUA), sob agitação
por 20 min, formando uma mistura
amarelo-pálido rica em GQDs (dispersão
coloidal denominada de dispersão
original). A fotoluminescência foi medida após
as dispersões de trabalho
originais de GQDs terem sido diluídas em água
ultrapura. Os parâmetros
experimentais de todas as dispersões estão
descritos na Tabela 1. A putrescina
foi preparada a partir de uma solução estoque
de 1000 mg L-1.
Resultado e discussão
As dispersões originais foram diluídas conforme o fator de diluição da Tabela 1
para se adequar a intensidade da fotoluminescência em função da saturação do
detector do equipamento, pois a fotoluminescência dos GQDs funcionalizados é
afetada conforme a natureza do modificador químico. O comprimento de onda máximo
de emissão e excitação de cada dispersão são descritas na Tabela 2.
Para comparação de desempenho, curvas analíticas foram construídas para cada
tipo de dispersão com a adição de putrescina nas concentrações de 10, 30, 50, 70
e 90 mg L-1. Os espectros de emissão podem ser observados na Figura 1.
Como pode ser observado na Figura 1, a dispersão de GQD-TU foi a única que
apresentou resposta satisfatória em função da presença de putrescina. Ademais, a
sonda fotoluminescente GQD-TU é do tipo turn-on, ou seja, de ativação, com
aumento da fotoluminescência proporcional ao aumento da concentração de
putrescina. Provavelmente, os grupos C=S do GQDs-TU interagem com o par de
elétrons não ligantes dos grupos NH2 da putrescina, favorecendo a transferência
eletrônica, aumentando a taxa de recombinação excitônica do nanomaterial
(responsável pela fotoluminescência medida). A confirmação desta hipótese
depende do estudo de caracterização que será realizado em etapas posteriores.
Tomando como base a resposta encontrada, se realizou uma série de testes de
diluição em água ultrapura do nanomaterial (GQDs-TU) a fim de otimizar a relação
concentração de putrescina e quantidade de nanomaterial de forma a otimizar a
sensibilidade da sonda. Foi encontrado respostas ainda melhores na proporção 2%
(v/v; GQDs-TU:água) na qual foi possível detectar melhor sensibilidade da
resposta (capacidade de diferenciar concentrações próximas de putrescina) e
comportamento linear do sinal líquido (L –L0, onde L é a luminescência medida da
sonda na presença de putrescina e L é a luminescência medida na ausência de
putrescina). Para otimizar a faixa de trabalho, a curva analítica foi
construída com adição de putrescina nas concentrações de 0,5; 1,0; 5,0; 10,0; e
30,0 mg L-1, conforme detalhado na Figura 2.
Pode-se observar, na Figura 2A, que a intensidade da fotoluminescência fica mais
intensa gradativamente na medida que a concentração de putrescina aumenta. A
curva analítica foi construída usando a fotoluminescência líquida (L - L0) como
mostrado na Figura 2B.
A resposta linear (R2 = 0,9946) abrangeu uma ampla faixa desde 0,50 até 30,0 mg
L-1, (concentração final). O modelo de equação da curva analítica foi (L - L0) =
(0,160) [putrescina]mg L-1 + (19,708). O limite instrumental de quantificação
(LOQ) foi considerado como a concentração mais baixa na faixa de 0,5 a 30 mg L-
1, que ainda mantêm a resposta linear pelo menos em R2 = 0,9946.
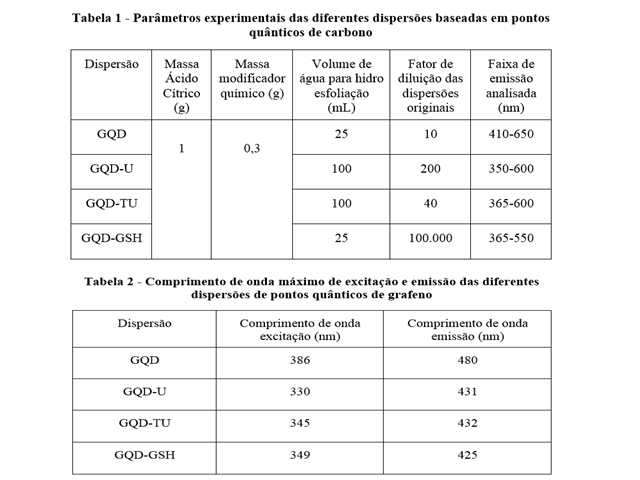
Tabela 1 - Parâmetros experimentais das dispersões de GQDs Tabela 2 - Comprimento de onda máximo de excitação e emissão das dispersões de GQS

Fig1: Espectros das sondas de GQDS com adição de putrescina Fig2: A) Espectro da sonda GQDs-TU com adição de putrescina;B) Curva analítica
Conclusões
A viabilidade de uma sonda fotoluminescente para detecção de putrescina foi
avaliada usando quatro tipos de GQDs, produzidos com diferentes precursores, com o
objetivo de encontrar a mais sensível. A dispersão de GQDs-funcionalizados com
tiouréia foi a única que demonstrou aumento da resposta em termos de intensidade
da fotoluminescência, proporcional ao aumento da concentração de putrescina. A
partir disso, é possível dizer que a sonda fotoluminescente GQDs-TU, apresenta
grande potencial para aplicação em amostra real (carne bovina, por exemplo),
depois de serem ajustadas condições para melhorar a seletividade da resposta
analítica.
Agradecimentos
Os autores agradecem CAPES, FAPERJ e CNPq pelo fomento e bolsas de pesquisa.
Referências
BRASIL. Ministério da Agricultura, Pecuária e Abastecimento (MAPA). Portaria n°185, de 13 de maio de 1997 da Regulamento da Inspeção Industrial e Sanitária de Produtos de Origem Animal, aprovado pelo Decreto n° 30.691, de 29 de março de 1952 e Considerando a Resolução Mercosul GMC n° 40/94, que aprovou o Regulamento Técnico de Identidade e Qualidade de Peixe Fresco (Inteiro e Eviscerado). Diário Oficial da União 1997; 19 maio.
FRANCO, Claudiomar Rodrigues. Evaluation of a turn-off photoluminescent probe based on graphene quantum dots for the determination of Hg2+ in water samples using flow injection analysis.. Rio de Janeiro, f. 90, 2019.. 169 p Dissertação (Química) - Pontifícia Universidade Católica do Rio de Janeiro, Rio de Janeiro, 2019.
HUSSAIN, A. et al. High-affinity olfactory receptor for the death-associated odor cadaverine. Proceedings of the National Academy of Sciences, v. 110, n. 48, p. 19579–19584, 2013.
NGAFWAN, Ngafwan et al. Study on novel fluorescent carbon nanomaterials in food analysis. Food Science and Technology, v. 42, 2022
ÖNAL, A. A review: Current analytical methods for the determination of biogenic amines in foods. Food Chemistry, v. 103, n. 4, p. 1475–1486, 2007.
ÖZOGUL, Y.; ÖZOGUL, F. Chapter 1: Biogenic Amines Formation, Toxicity, Regulations in Food. In: SAAD, B.; TOFALO, R. Biogenic Amines in Food: Analysis, Occurrence and Toxicity. 1 ed. Londres: Royal Society of Chemistry, 2019.. 330 p. cap. 1, p. 1-17. Disponível em: https://pubs.rsc.org/en/content/chapterhtml/2019/bk9781788014366-00001?isbn=978-1-78801-436-6. Acesso em: 1 jun. 2022.
SHALABY, A. R. Significance of biogenic amines to food safety and human health. Food Research International, v. 29, n. 7, p. 675-690, 1996.
SHI, X. et al. Review on carbon dots in food safety applications. Talanta, v. 194, p. 809–821, 2019.
ZHANG, W. et al. Carbon quantum dot fluorescent probes for food safety detection: Progress, opportunities and challenges. Food Control, v. 133, Part A, p.1-24. (2022).
















