Autores
Leão, M.H.S. (UFOPA) ; Santos, A.M.C. (UFOPA) ; Santiago, A.C.P. (UFOPA) ; Saldanha, L.S. (UFPA/CAMPUS ANANINDEUA) ; Santos, P.H.C. (UFPA) ; Favacho, A. (UFPA/CAMPUS ANANINDEUA) ; Figueira, B.A.M. (UFOPA)
Resumo
Os sub-produtos gerados pela indústria mineral da Amazônia (RBA) consistem em um material abundante e disponível na Região, sendo objeto de grande interesse da comunidade científica inserida no conceito de economia circular, cujo foco é a sua transformação em produtos de valor agregado. Neste trabalho, rejeitos de Mn da Amazônia foram estudados como material de partida de baixo custo para obtenção do composto inorgânico MnC2O4·2H2O por lixiviação ácida. Os resultados de caracterização por DRX e MEV, indicaram que o processo de recuperação do Mn no sal MnC2O4·2H2O foi efetivo com a sua obtenção bem cristalina e aparentemente sem impurezas, mostrando assim, que um produto inicialmente sem valor comercial pode ser convertido com sucesso em material de valor agregado.
Palavras chaves
Amazônia; Rejeitos de Mn; MnC2O4·2H2O
Introdução
MnC2O4 é um sal inorgânico pertencente a classe dos ácidos oxálicos, podendo ocorrer na forma non, di e tri-hidratada com a propriedade de baixa estabilidade térmica (LUNGE, GEORG, 1924; DONKOV, B., MEHANDJIEV, D, 2004). De acordo com WANG et al, (2013) e LI et al, (2012) pode ser usado em síntese de materiais catódicos ricos em lítio e manganês através do método de co-precipitação e como catalisador (PUZAN et al., 2018). Algumas estruturas parciais de oxalatos de manganês na forma MnC2O4·2H2O foram descritas por DEYRIEUX et al (1973), que reportaram estruturas com cadeias infinitas unidimensionais de Mn-oxalato, sendo que nessas cadeias cada átomo de manganês é orientado por dois oxalatos quelatos e duas moléculas de H2O em posições axiais e têm como diferença o deslocamento dessas cadeias ao longo do eixo duplo. As diferenças nos parâmetros para esses os dois polimorfos não são de grande importância porque os padrões de pó para eles são quase iguais (PUZAN et al., 2018). Entre os oxalatos de manganês (II) hidratados apenas duas estruturas cristalinas de α -MnC2O4.2H2O e γ-MnC2O4. 2H2O haviam sido obtidas e apresentadas até 2005.
Neste trabalho, avaliou-se a possibilidade de conversão de rejeitos da indústria mineral da Amazônia em oxalato de Mn di-hidratado obtido por lixiviação ácida com ácido oxálico.
Material e métodos
O processo de desenvolvimento de transformação dos rejeitos em MnC2O4.2H2O ocorreu através de reações de fusão alcalina e lixiviação ácida. O efeito da temperatura foi avaliado na formação do produto final livre de impurezas. A caracterização mineral dos produtos foi feita por difração de raios X (DRX), onde se empregou um difratômetro de bancada D2Phaser (Bruker). Este equipamento possui um goniômetro de varredura vertical e um tubo de cobre (CuKa = 1.5406 Å) de 400 W de potência, com uma geometria de Bragg-Brentano no modo contínuo, velocidade de varredura de 0,25° /min, tendo como sistema de detecção um detector rápido modelo LynxEye. A tensão foi de 30 kV e 10mA, respectivamente. A caracterização morfológica do produto final foi por MEV/EDS através da sua metalização com ouro. O microscópio utilizado foi da marca LEO-Zeiss, 430 Vp, em condições de análise utilizando imagens secundárias obtidas a 20 KV, com distância de trabalho de 11 mm.
Resultado e discussão
Uma caracterização dos rejeitos e produtos de síntese foi feita por DRX e apresentada na Fig 1. A composição mineral dos rejeitos se mostrou composta por minerais de ferro e alumínio (hematita e gibbsita), titânio (anatásio), aluminosilicatos (caulinita), além de fases de oxido de Mn tais como: litioforita, birnessita e criptomelana (Fig. 1a). Para o material sintetizado da fusão alcalina, uma estrutura amorfa de MnO2 foi identificada (Fig 1b). Enquanto para o produto final (Fig. 1c) obtido de MnO2 lixiviado, foram observados picos em 18,44; 18,92; 22,67; 24,23; 29,94; 33,76; 38,25 e 49,36 (2 theta) referentes aos planos (-111), (-202), (002), (-112), (-402), (112), (400), (-131) da fase de MnC2O4·2H2O (PDF 025-0544).
A caracterização morfológica do material de partida e de MnC2O4·2H2O foi realizada por microscopia eletrônica de varredura (Fig. 2). Uma morfologia de agregados de partículas sem uniformidade de tamanho e forma pôde ser visto (Fig. 2a). Enquanto que para o produto referente ao sal de Mn, uma nítida morfologia de cristais em placas com tamanho de 2 a 10 m pôde ser notada (Fig. 2b), indicando assim uma completa transformação dos rejeitos para MnC2O4·2H2O, como já observado na difratometria de raios-X.
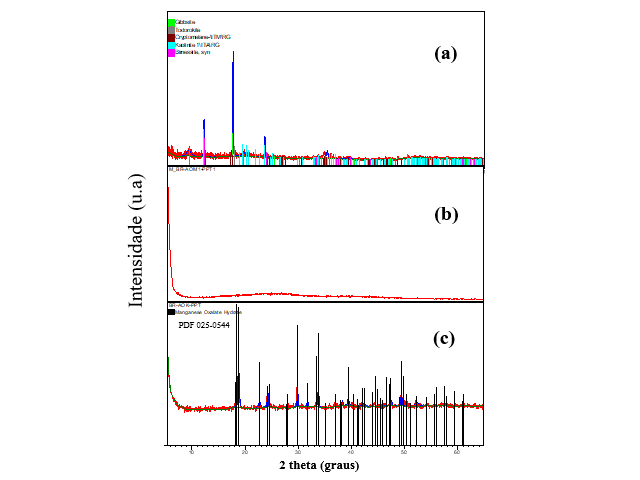
Padrões de DRX dos rejeitos de Mn (a), material sintetizado (b) e MnO2 lixiviado (c).

Microscopia eletrônica de varredura do material de partida (a) e de MnC2O4·2H2O (b).
Conclusões
Este trabalho demonstrou uma possibilidade alternativa de transformação de rejeitos de Mn da indústria mineral da Amazônia em oxalato de Mn di-hidratado (MnC2O4·2H2O). O sal foi obtido a princípio sem impurezas, com estrutura cristalina e morfologia em placas, indicando assim que um produto sem valor econômico pode ser uma interessante matéria prima de baixo custo para um produto de grande relevância tecnológica.
Agradecimentos
Os autores agradecem a CAPES, CNPQ, UFOPA, LCM (IFPA), LAMIGA (UFPA) e CETENE pelo apoio financeiro e analítico que permitiram a execução deste trabalho.
Referências
ANNA N. PUZAN, VYACHESLAV N. BAUMERA, Dmytro V. Structure disordering and thermal decomposition of manganese oxalate dihydrate, MnC2O4·2H2O. Lisovytskiyb, Pavel V. Mateychenkoa. Journal of Solid State Chemistry 260 (2018) 87–94.
DONKOVA, B.; MEHANDJIEV, D. (2004). "Mecanismo de decomposição de oxalato de manganês (II) di-hidratado e oxalato de manganês (II) tri-hidratado" . Termoquímica Acta . 421 (1–2): 141–149. doi : 10.1016/j.tca.2004.04.001 . ISSN 0040-6031.
D. WANG, I. BELHAROUAK, G. ZHOU, K. Amine, Síntese de materiais catódicos ricos em lítio e manganês através de um método de co-precipitação de oxalato, J. Electrochem. Soc. 160 (5) (2013) A3108–A3112.
LUNGE, GEORGunge, (1924). Métodos Técnicos de Análise Química de Lunge e Keane. 2d Ed., Editado por Charles A. Keane ... e PCL Thorne . Gurney e Jackson.
R. DEVRIEUX, CH BERRO, A. PENELOUX, Estrutura cristalina de oxalatos desidratados de manganês, de cobalto, de níquel e de zinco, Bull. Soc. Chim. Pe. (1973) 25-34.
Y. LI, K. CHENXIA, C. HUANG, Y. CHENG, Efeito de nanopartículas de MnC2O4 no decomposição térmica do propulsor TEGDN/NC, J. Therm. Anal. Calorim. 109 (2012) 171-176.
















