Autores
Francelino de Souza, L.V. (IFES- CAMPUS LINHARES) ; Lopes Garcia, A. (IFES- CAMPUS LINHARES) ; Sant'ana Oliveira, C. (IFES- CAMPUS LINHARES) ; Rodrigues Silvério, L. (IFES- CAMPUS LINHARES) ; Biancardi da Silva, M. (IFES- CAMPUS LINHARES) ; Cominote, M. (IFES - CAMPUS LINHARES) ; de Souza Oliveira, R.C. (IFES - CAMPUS LINHARES) ; Vieira Rodrigues, M. (IFES - CAMPUS LINHARES) ; Gazel, F. (IFES - CAMPUS LINHARES)
Resumo
Conceito teórico de ácido-base, por ser muito empírico produz certo grau de
dificuldade, tornando-se essencial o trabalho em conjunto nas aulas práticas.
Porém nem todas as instituições têm condições de adquirir os reagentes
necessários. Assim, o objetivo foi realizar o estudo do extrato das pétalas de
Macroptilim atropurpureum (Siratro), como indicadores ácido-base naturais. Os
extratos obtidos foram o aquoso e alcoólico, estes foram testados em soluções
tampão de pH 1 a 14, amostras do cotidiano e em ensaios titulométricos de
neutralização. Os extratos, aquoso e alcoólico das pétalas apresentam potencial
na identificação do caráter ácido-base de amostras do cotidiano e de soluções
tampão em vários valores de pH e excelentes indicadores como ponto de viragem em
análise titulométrica.
Palavras chaves
antocianinas; titulometria; espectroscopia de UV-Vis
Introdução
A química é uma disciplina de caráter teórico-prática, mas vem sendo
praticamente repassada na base de teoria, podendo acarretar desinteresse dos
alunos. Isso acontece na maioria das vezes pela falta de estrutura e materiais
laboratoriais nas escolas para a realização das práticas (UCHÔA et al, 2016). Um
exemplo é o ensino do conceito teórico de ácido-base, por ser muito empírico
produz certo grau de dificuldade, tornando-se essencial o trabalho da teoria em
conjunto com as aulas práticas (AGOSTINHO et al, 2013).
Uma prática simples e de grande importância que aborda o tema de ácidos-bases é
a reação dessas substâncias na presença de indicadores, onde o aluno consegue
perceber visualmente as reações por meio de mudanças de cores. Porém nem todas
as instituições têm condições de adquirir os reagentes necessários para a
prática, uma alternativa é o uso de indicadores naturais provenientes de frutos,
folhas e flores, destacando-se em suas vantagens quando comparados aos
sintéticos, pois são prontamente disponíveis, não tóxicos e econômicos
(VIJAYANAND et al, 2019).
Muitos trabalhos são pesquisados e publicados sobre a aplicação das antocianinas
como indicadores de ácido e base: SOPIAH (2018) e colaboradores desenvolveram um
papel indicador a partir da antocianina extraída da planta Aerva sanguinolenta
(L.) Blume; PATMAS (2018) e colaboradores utilizaram o extrato etanólico
provenientes das pétalas de flores da Lantana camara L. como indicador de
ácidos-bases e obtiveram bons resultados; GUERRA (2018) e colaboradores fizeram
os testes com o extrato alcoólico das pétalas da flor Ixora chinensis e
observaram que mesmo depois de semanas os indicadores mantiveram as suas
propriedades reacionais perante as mudanças do pH; HASANAH (2018) e
colaboradores, desenvolveram um papel indicador à base de antocianina extraída
de arroz preto que detecta gás amônia (caráter básico) e para subsidiar seus
resultados fizeram a caracterização do extrato por espectroscopia UV-Vis em pH
de 2, 5, 7, 8 e 13.
Nos domínios do Ifes/Campus Linhares, é facilmente perceptível à presença de uma
planta rasteira com flores de cor roxa acentuada, cuja coloração, é um grande
indicativo da presença de antocianina na sua composição (MAZZA et al, 1993). Em
pesquisa, foi possível identificar essa espécie que tem o nome científico
Macroptilium atropurpureum (Siratro). Essa planta é uma leguminosa perene com
hábito de crescimento trepador (rasteiro), tem preferência a solos arenosos,
desde que possua um pequeno grau de fertilidade e bem drenados, tolera bem o
consórcio com gramíneas. Ela também possui um sistema radicular muito vigoroso e
profundo e de difícil erradicação por métodos mecânicos (capinas e aração).
Adapta-se facilmente as condições de clima tropical e subtropical tendo uma
distribuição geográfica em todas as regiões brasileiras (MARQUES, 1997).
Com base nessas informações, teve-se como objetivo realizar o estudo do extrato
das pétalas de Macroptilim atropurpureum (Siratro) perante a variação de pH e o
seu potencial como indicador ácido-base.
Material e métodos
1. Obtenção dos extratos e caracterização.
Todas as amostras das flores do Siratro (Macroptilim atropurpureum) foram
coletadas na área do jardim do Ifes/Linhares pela manhã. Após a coleta as
pétalas eram deixadas na bancada do laboratório de Química do Ifes/Linhares,
para a evaporação das gotículas de água (orvalho) a temperatura ambiente.
Aproximadamente após 1 hora iniciava-se a remoção das pétalas e a pesagem.
Devido a logística de trabalho e o quantitativo de pétalas que se obtinha
diariamente, foi necessário armazena-las, e para não sofrerem alterações
químicas optou-se conserva-las a temperatura inferior a 0°C, ausência de luz e à
vácuo.
Foram obtidos dois extratos do substrato indicador ácido-base da planta. Para um
extrato utilizou-se a água destilada como solvente e para o outro fez-se uso da
solução alcoólica 51,9°GL = 46,2º INPM como solvente. A proporção da massa das
pétalas e volume do solvente empregada foi de 1:5 (g/ml).
Após a adição dos solventes nos béqueres contendo as pétalas a temperatura
ambiente, promoveu-se a maceração de forma moderada, durante 3 min, com auxílio
de um bastão de vidro e em seguida os dois béqueres foram vedados com plástico
insulfilm. O tempo de extração, contato das pétalas com os solventes, foi de 24h
em repouso com ausência de luz e sob refrigeração a temperatura de 4 a 8ºC.
A remoção dos resíduos das pétalas dos extratos resultantes foi feita por meio
de filtração com auxílio de uma peneira de plástico com poros de aproximadamente
1mm.
Os extratos foram caracterizados por meio das análises de pH (pHmetro:
Quimis/Q400MT), condutividade (condtivímetro: ION-DDS12DW) e varredura espectral
na faixa do UV-Vis (espectrofotômetro: Agilent-Cary60/UV-Vis).
2. Uso dos extratos como indicadores ácido-base em amostras do cotidiano.
Os extratos foram testados com amostras do cotidiano (vinagre, sabão em pedra +
água, sabão em pó + água, leite, ketchup + água, fermento químico + água). Para
efeito de comparação, o caráter ácido-base dessas amostras também foram
identificados utilizando o equipamento pHmetro e o indicador: solução de azul de
bromotimol.
3. Uso dos extratos como indicadores do ponto de viragem em reações de
neutralização.
Na verificação do potencial dos extratos aquoso e alcoólico como indicadores de
ponto de viragem em reações de neutralização, utilizou-se como titulante a
solução de NaOH (0,1mol/L) e como titulado as soluções de vinagre de álcool e
ácido clorídrico (≈ 0,1mol/L).
Os volumes das soluções tituladas de vinagre e de ácido clorídrico foram
respectivamente: 1ml (acrescentando aproximadamente mais 9 ml de água destilada)
e 10ml. A cada alíquota do titulado adicionou-se 0,5ml do extrato aquoso ou
alcoólico. Considerou-se como fim da titulação (neutralização) a mudança de cor
de rosa para verde.
Para efeito de comparação esses ensaios foram repetidos, mas no lugar do extrato
utilizou-se como indicador a solução de fenolftaleína (3 gotas).
Resultado e discussão
1.Caracterização dos extratos aquoso e alcoólico.
Após o tempo de extração (24h = 1°dia) e filtração, obteve-se os extratos aquoso
e alcoólico em que ambos apresentaram uma coloração entre roxa e vermelha-
púrpura bem intensa.
Os resultados obtidos de pH, demonstram que ambos os extratos são ácidos, onde o
extrato aquoso é mais ácido (pH = 5,26) o que proporciona uma maior
condutividade (21,4 mS) em relação ao extrato alcoólico (pH = 6,11; Cond.: 12,0
mS). Isso possivelmente se deve a fermentação da antocianina por microrganismos
que ocorre no meio aquoso e que é inibido no meio alcoólico.
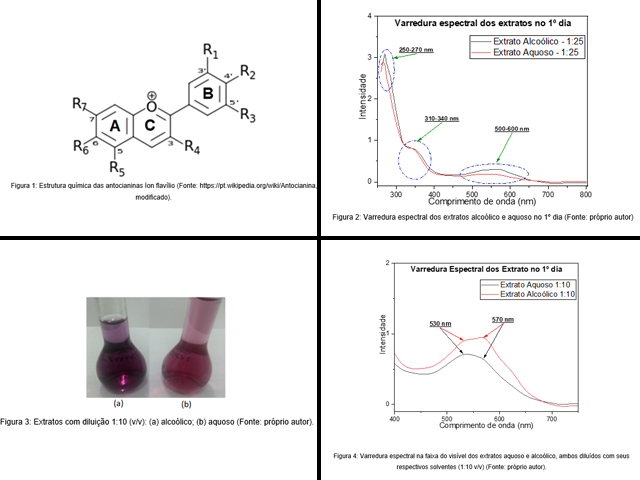
Em relação a espectroscopia de UV-Vis, em geral, as antocianinas mostram alta
absorbância na faixa de 250 a 270 nm (região UV) e na faixa de 500 a 600 nm
(região visível). Isto têm sugerido que a absorção UV pode ser atribuída
principalmente ao anel A, enquanto a absorção visível deve-se ao pirano e ao
anel B (figura 1) (Lopes et al, 2007).
Os espectros UV-Vis dos extratos aquoso e alcoólico do siratro (figura 2),
apresentam este padrão de absorção típico de antocianina. Além disso, um pico
adicional é observado na faixa de comprimento de onda de 310 a 340 nm referente
acilação na molécula de açúcar da antocianina (Saha et al, 2020).
Comparando os extratos diluídos (1:10 v/v) percebe-se visualmente que o extrato
alcoólico possui uma intensidade na cor maior que a do extrato aquoso (figura
3).
Essa diferença nas tonalidades/intensidades das cores entre os dois extratos,
pode ser explicada pelo fato que, além da água como solvente a solução alcoólica
possui o álcool, que proporciona um aumento na extração de outras substâncias
entre elas algumas classificadas como cromóforos presentes nas pétalas, que
intensificam a cor do extrato quando comparado ao aquoso. Essa diferença também
é perceptível nos espectros UV-Vis dos extratos na região do visível (figura 4),
analisando os espectros, observa-se dois ombros, uma em 530 nm e outra em 570
nm, em que, na solução alcoólica o ombro em 570 nm é mais intenso quando
comparada com a solução aquosa, esse aumento na intensidade pode ser explicado
pela extração realizada pelo álcool de substâncias cromóforas que sofrem
absorção nessa região de comprimento de onda.
2. Comportamento dos extratos aquoso e alcoólico na presença de soluções tampão
(pH 1 a 14).
A figura 5 apresenta modificações nas estruturas das antocianinas em função do
pH (FILHO et al., 2012) e as mudanças de coloração obtidas a partir da adição de
0,250 mL do extrato aquoso, em tubos de ensaio contendo soluções tampão com
valores de pH de 1 a 14.
Nas soluções tampão de pH 1 e 2, os extratos apresentaram coloração vermelha,
relacionada à presença do cátion flavilium. As soluções tampão de pH 3 e 4
apresentaram cor vermelha mais clara, e a de pH 5, roxa, relacionadas ao
carbinol, que apresenta uma hidroxila ligada a um carbono saturado da
antocianina. Em soluções com valores de pH 6, 7 e 8 as antocianinas se
encontram na forma estrutural anidrobase, que pode ser formada pela
desprotonação do cátion flavílium ou pela perda de uma molécula de água do
carbinol, e as cores observadas nestas soluções foram, roxa para o pH 6, azul-
cinza para o pH 7 e roxa para o pH 8. Entre os valores de pH 6, 7 e 8, as
soluções assumem colorações que variam da roxa ao azul-cinza, devido à presença
da forma estrutural anidrobase.
Com a elevação do pH, a anidrobase produzida vai sofrendo ionização e, à medida
que esta ionização aumenta, a solução primeiro assume uma coloração azul-
esverdeada entre pH 9 e 10, depois passa do verde ao verde-amarelado entre pH 11
e 12. Acima de pH 13, a solução se torna amarela ocorrendo a abertura do anel
benzopirilium, dando origem a estruturas chamadas pseudobase chalcona (LOPES et
al., 2007).
Resultados semelhantes foram observados para as soluções tampão de pH de 1 a 14
contendo 0,100 ml do extrato alcoólico, porém com colorações de menor
intensidade, devido à adição de uma menor quantidade de extrato. Isso é possível
observar comparando as figuras 6 e 7, que apresentam respectivamente o uso dos
extratos aquoso e alcoólico.
Coutinho e colaboradores investigaram os extratos aquoso e alcoólico da
Macroptilium Atropurpureum, para uso como indicadores de pH, e perceberam que
para valores de pH entre 4 e 9 não há mudança significativa de cor da solução
(COUTINHO et al., 2016). Nunes e colaboradores estudaram o extrato
hidroalcoólico da flor Macropitilium Lathyroides (L.) Urb e observaram que para
os valores de pH entre 5 e 10 a cor da solução é pálida e pouco perceptível
(NUNES et al., 2021). Tanto Santos e colaboradores, utilizando extrato
hidroalcoólico da Brassica oleracea L Var. capitata Rubra (repolho roxo) (SANTOS
et al. , 2019), quanto Oliveira, que investigou os extratos alcoólicos das
flores da Allamanda blanchetii (Alamanda roxa), Delonix regia (Flamboyant),
Begonia cucullata (Azedinha-do-brejo), Hippeastrum puniceum (Amarílis),
Asystasia gangetica (Violeta chinês ou Coromandel) e Ixora coccinea (Ixora
coral) (OLIVEIRA, 2021), obtiveram resultados semelhantes aos obtidos neste
trabalho.
3. Uso dos extratos como indicadores ácido-base em amostras do cotidiano.
Foram utilizadas 6 amostras do cotidiano, são elas: 1) sabão em pó + água; 2)
fermento químico + água; 3) ketchup + água; 4) leite; 5) vinagre de álcool; 6)
sabão em pedra + água.
As amostras 1, 3 e 4, já trazem uma coloração (respectivamente: azul claro,
vermelho sangue e branco), podendo comprometer visualmente os ensaios de análise
do caráter ácido-base por meio de indicadores, principalmente em soluções. Na
figura 8, pode-se observar o comportamento colorimétrico e comparar o extrato
alcoólico com o indicador azul de bromotimol em contato com as amostras do
cotidiano. Sabe-se que o indicador azul de bromotimol apresenta coloração azul
em meio básico e amarelo em meio ácido, com base nisso pode-se afirmar que as
amostras 1, 2, e 6 possuem caráter básico e as 3, 4 e 5 caráter ácido.
Foi discutido que os extratos alcoólico e aquoso das pétalas das flores da
espécie Macroptilium atropurpureum (Siratro) apresentam uma tendência de
coloração esverdeada para o meio básico e vermelha para o meio ácido e azul-
cinza para o meio próximo de neutro. Com base nisso pode-se afirmar que as
amostras 1 e 6 apresentam caráter básico e a amostra 5 o caráter ácido (Figura
8). As amostras 2 e 4, com o extrato alcoólico, mostraram uma tonalidade azul-
cinza indicando um pH próximo de neutro. Na amostra 3, com o extrato alcoólico,
a sua tonalidade original (vermelho sangue) sobrepôs a coloração vermelha que se
esperava para o caráter ácido. A tabela 1 apresenta de forma resumida os
resultados obtidos dos caráteres ácido-base das amostras do cotidiano com os
indicadores azul de bromotimol e extrato alcoólico, e também os valores de pH
obtidos com o equipamento pHmetro.
4.Uso dos extratos como indicadores do ponto de viragem em reações de
neutralização.
Com os ensaios de titulação das amostras de vinagre de álcool e solução de HCl
usando a solução de NaOH (0,1mol/L) como titulante, pode-se averiguar que os
extratos das pétalas das flores da Siratro, apresentaram os pontos de viragem
visual bem nítidos, passando da cor rosa para a cor verde.
Os volumes da solução titulante na neutralização da amostra de HCl, apresentaram
valores médios semelhantes comparando entre os extratos e com o indicador
fenolftaleína (11,5 ml). Pode-se afirmar também com base nos resultados, que
ambos extratos, aquoso e alcoólico, possuem potencial para a identificação do
ponto de viragem entre base forte e ácido fraco (amostra de vinagre de álcool),
pois os valores dos volumes gastos da solução titulante foram bem próximos
comparando com fenolftaleína (8,1 ml; 8,2 ml; 8,4 ml respectivamente). Nunes
(2021) e colaboradores, analisaram o extrato da flor da espécie Macroptilium
lathyroides (feijão-de-rola), e verificaram resultado semelhante.

Conclusões
Os extratos aquoso e alcoólico das pétalas de Macroptilim atropurpureum (Siratro)
apresentam potencial na identificação do caráter ácido-base de amostras do
cotidiano e de soluções tampão em vários valores de pH.
Ambos extratos demostraram ser excelentes indicadores como ponto de viragem em
análise titulométrica de neutralização entre base forte com ácido forte e fraco.
Agradecimentos
Agradecemos à Fundação de Amparo à Pesquisa e Inovação do Espírito Santo (FAPES)
pelo financiamento das bolsas de Iniciação científica.
Referências
AGOSTINHO, C. L.; DA NASCIMENTO, L. L.; CAVALCANTI, B. L. D. F.. Uma abordagem do conteúdo de ácidos-bases no ensino da educação de jovens e adultos–EJA. Revista Lugares de Educação, 2(4), 3-15, 2013.
COUTINHO, M. E. C. P.; INÁCIO, M. D. S; SOUSA, D. S. Indicadores de pH a partir das flores das espécies Macroptilium Atropurpureum, Centrosema Brasilianum e Ipomoea Asarifolia. 4ª Semana de Química – IFRN, 2016,
FILHO, N.R.A.; GUIMARÃES, W.; ALVES, M.I.R. Antocianinas em extratos vegetais: aplicação em titulação ácido-base e identificação via cromatografia líquida/espectrometria de massas. Química Nova, Vol. 35, nº. 8, 1673-1679, 2012.
GUERRA, M. H. F. S.; VASCONCELOS, A. K. P.; DA SILVA FIRMINO, E.; NOJOSA, A. C. A. B.; SALDANHA, G. C. B.; DE GOES SAMPaio, C.. Uma abordagem das atividades experimentais no Ensino de Química: uso da flor Ixora Chinensi como indicador ácido-base. Revista Thema, 15(3), 834-847, 2018.
HASANAH, B. H; IMAWAN, C. Effect of Paper Matrix on the Properties of the Ammonia Gas Indicator Label. In. Journal of Physics: Conference Series. IOP Publishing, 1120(1), 012032, 2018.
LOPES, T. J.; XAVIER, M. F.;, QUADRI, M. G. N.; QUADRI, M. B. Antocianinas: uma breve revisão das características estruturais e da estabilidade. Revista Brasileira Agrociência, v.13, n.3, p. 291-297, jul-set, 2007
MARQUES, M. A. L. Purificação e caracterização parcial de um potyvirus isolado de siratro e produção de anti-soro específico. 1997. 64. Dissertação (Mestrado em Agronomia). Departamento de Pós-graduação em Agronomia, UNIVERSIDADE FEDERAL DO CEARÁ Fortaleza/CE.
MAZZA, G; MINIATI, E. Anthocyanins in Fruits, Vegetables, and Grains. Press Inc.: Boca Raton, FL, 362, 1993.
NUNES, D. R.; ARAUJO, J. F. de; PRATA, E. G.; FREITAS, N. M. da S.; FREITAS, M. C. da C.; CORREIA, L. M. Indicadores ácido-base: extrato hidroalcoólico da flor da espécie Macroptilium lalhyroides (L.) Urb. Scientia Naturalis, v. 3, n° 1, 288-299, 2021.
OLIVEIRA, W. S. de. Produção de indicadores ácido-base naturais em solução e em papel a partir de estratos de plantas com potencial aplicação no ensino de química. Trabalho de Conclusão de Curso (Licenciatura em Química) - Instituto Federal do Piauí, Cocal - PI, 2021.
PATMAS, M.; SHETE, D.; PATIL, S.; KUMBHAR, S. Use of ethanolic extract of L. flowers as pH indicator Lantana camara. Asian Journal of Pharmacy and Pharmacology, 4(6), 802-805, 2018.
SAHA, S.; SINGH, J.; PAUL, A.; SARKAR, R.; KHAN, Z.; BANERJEE, K. (2020). Anthocyanin profiling using uv-vis spectroscopy and liquid chromatography mass spectrometry. Journal of AOAC International, 103(1), 23-39.
SANTOS,V. M. da S.; MATIAS, T. B.; ADAMS, S. I.; GOMES, A.; GIUSTI, E. D.; STADLER, J. P. Emprego do extrato de Brassica Oleracea l. como indicador alternativo de pH em titulações ácido-base: uma atividade experimental integradora para o ensino de química. Experiências em Ensino de Ciências V.14, No.1, 2019
SOPIAH, S.; SARI, S.; WINDAYANI, N. Development of paper indicator from sambang colok (Aerva sanguinolenta) plant extract. In: IOP Conference Series: Materials Science and Engineering. IOP Publishing, 434(1), 012082, 2018.
UCHÔA, V. T.; CARVALHO, F. R. S. M.; LIMA, A. M. M.; ASSIS, J. B. Utilização de plantas ornamentais como novos indicadores naturais ácido-base no ensino de química. HOLOS, 2, 152-165, 2016.
VIJAYANAND, S.; KHALID, MOHAMMED. AJ Csian OURNALOF HEMISTRY AJ Csian OURNALOF HEMISTRY. Asian Journal of Chemistry, 31(2), 251-254, 2019.
















