Autores
Gomez, B. (UNIVERSIDAD NACIONAL DE COLOMBIA) ; Granados, G. (UNIVERSIDAD NACIONAL DE COLOMBIA)
Resumo
Se prepararon N-CQDs a partir de cáscaras de chontaduro. Posteriormente, se
funcionalizaron con cisteína (CYS) para formar los NCQDs/CYS. Estos materiales
se caracterizaron, obteniendo para los N-CQDs un material semicristalino con un
núcleo grafítico y una superficie rica en grupos amino y carboxilato que
estabilizan la nanopartícula en agua, estos materiales presentaron una elevada
absorción y fluorescencia en el visible, obteniendo un ⲫ del 29%. Los NCQDs/CYS
conservaron el núcleo grafítico, además de una superficie funcionalizada con
cisteína; presenta un aumento en la absorción y fluorescencia en el visible,
incrementando el ⲫ al 34%. Las características mencionadas hacen de los N-
CQDs/CYS excelentes candidatos para su posterior uso en la detección
fluorescente de mercurio.
Palavras chaves
Chontaduro; Nanopartículas; Fluorescencia
Introdução
Recientemente, los puntos cuánticos de carbono o por sus siglas en inglés CQDs
(Carbon Quantum Dots), son un nuevo miembro de nanopartículas (NPs) de carbono
que han originado un gran interés en los investigadores (LIU, Y.; ZHOU, Q.; LI,
J.; LEI, M.; YAN, X., 2016). Los CQDs se caracterizan por tener una estructura
usualmente esférica con un tamaño inferior a los 10 nm, tienen diferentes
propiedades ópticas (absorción y fluorescencia) y se destacan por formar
soluciones acuosas estables con alta fluorescencia en el visible. Además de que
la fluorescencia emitida por los CQDs depende de la longitud de onda de
excitación (JELINEK, R., 2004), cabe resaltar que los CQDs pueden ser preparados
por métodos simples y rápidos, con materiales precursores económicos,
disponibles y de baja toxicidad (DAS, R.; BANDYOPADHYAY, R.; PRAMANIK, P.,
2018). Los CQDs pueden ser obtenidos a partir de carbón, nanotubos de carbono,
moléculas orgánicas y biopolímeros (SIMÕES, E. F.; LEITÃO, J. M.; DA SILVA, J.
C., 2016). Recientemente se han dedicado grandes esfuerzos en la obtención de
estas nanopartículas a partir de fuentes naturales como vegetales y frutas (GU,
D.; SHANG, S.; YU, Q.; SHEN, J., 2016). Sin embargo, todavía hay pocos trabajos
en el aprovechamiento de residuos provenientes de fuentes naturales para la
obtención de CQDs, como las cáscaras de frutas y ninguno utilizando cáscara de
chontaduro, siendo estrategias de síntesis verde, económica y de baja toxicidad.
La cáscara de chontaduro es un residuo orgánico conformado por diferentes
compuestos que bajo condiciones adecuadas pueden ser precursores carbonáceos de
CQDs (MARTÍNEZ, J.; RODRÍGUEZ, X.; PINZÓN, L.; ORDÓÑEZ, L., 2017).
Adicionalmente, los CQDs pueden ser obtenidos a partir de calentamiento por
irradiación con microondas de una fuente carbonácea, presentando diferentes
ventajas en la síntesis, como por ejemplo, calentamiento rápido y homogéneo, lo
que genera un ahorro de tiempo y energía, así como también, optimización de
rendimientos y de las condiciones de reacción (DÍAZ, Á.; PRIETO, P.; DE LA HOZ,
A., 2019). Además, para mejorar las propiedades ópticas, los CQDs pueden ser
dopados con nitrógeno (N-CQDs). Sin embargo, estos CQDs no poseen sitios de
reconocimiento superficial que generen cierta afinidad a un analito de interés,
por tal motivo, para aumentar dicha afinidad, los N-CQDs prístinos (sin
funcionalizar) pueden ser modificados superficialmente (funcionalizados) con
moléculas estratégicas dotándolos con mayor especificidad y reconocimiento hacia
un analito para su posterior detección (YAN, F.; JIANG, Y.; SUN, X.; BAI, Z.;
ZHANG, Y.; ZHOU, X., 2018). La funcionalización de los N-CQDs se puede hacer con
biomoléculas como cisteína (Cys) una base blanda, formando lo que de aquí en
adelante se denominará N-CQDs/CYS, lo que les podrían brindar mayor afinidad a
los iones metálicos pesados como el mercurio (ácido blando). Esta mayor afinidad
química se debe a la fuerte estabilidad que tienen los ácidos blandos con sus
correspondientes bases blandas, descrita en la teoría de Pearson, por sus siglas
en inglés HSAB (hard-soft-acid base) (PEARSON, R., 1968). Las destacadas
propiedades de los CQDs, como su elevada fluorescencia y solubilidad,
estabilidad en agua y a la irradiación con luz, además, de la posibilidad de ser
funcionalizados superficialmente con biomoléculas estratégicas y la variación de
sus propiedades ópticas (fluorescencia o absorción) en presencia de iones
metálicos pesados, los hacen buenos candidatos para ser usados eficientemente en
la detección óptica de los iones mercurio de una forma sencilla y económica.
Sumado a lo anterior, los CQDs pueden ser sintetizados de forma sencilla usando
precursores económicos, disponibles y de muy baja toxicidad, en contraste a los
sensores ópticos basados en moléculas orgánicas, nanoclústers metálicos y puntos
cuánticos inorgánicos.
Material e métodos
La síntesis de los N-CQDs prístinos se efectuó a través del método de
irradiación con microondas por 2 horas, utilizando 1.8 g de cáscaras de
chontaduro (fuente de carbono), 4.5 mL de etilendiamina (fuente de nitrógeno) y
15.5 mL agua como solvente (LIU, Y.; JIANG, L.; LI, B.; FAN, X.; WANG, W.; LIU,
P.; XU, S.; LUO, X., 2019), asimismo, para la síntesis de los CQDs sin dopar se
realizó exactamente el mismo método de síntesis pero sin agregar etilendiamina.
Los N-CQDs obtenidos, se purificaron utilizando centrifugación, microfiltración,
diálisis y liofilización, obteniendo nanopartículas de carbono en polvo. La
funcionalización de los N-CQDs prístinos con cisteína (CYS) se realizó a través
de la reacción de acoplamiento de amida (YAN, F.; JIANG, Y.; SUN, X.; BAI, Z.;
ZHANG, Y.; ZHOU, X., 2018). Para lo anterior, se hizo reaccionar una solución
acuosa de los N-CQDs activada con 1-etil-3-(3-dimetilaminopropil) carbodiimida
(EDC) con una solución de CYS en buffer fosfato. La EDC es un catalizador que se
utiliza en la activación de los grupos -COOH acoplándose a los grupos
funcionales amino, formando así los N-CQDs/CYS. Finalmente, los N-CQDs
funcionalizados fueron purificados para su posterior caracterización de la forma
anteriormente descrita.
Los espectros de absorción UV-VIS se midieron en un espectrofotómetro UV-VIS
EMC-11-UV con lámpara de tungsteno. Los espectros de fluorescencia se midieron
en espectrofluorometro Cary Eclipse, con lámpara de xenón como fuente de
excitación. El sulfato de quinina se usó como el estándar para la determinación
del rendimiento cuántico de fluorescencia (ⲫFl) (el ⲫFl del sulfato de quinina
es 0.55 disuelta en ácido sulfúrico). Los espectros FT-IR se midieron en un
espectrómetro Thermo Scientific Nicolet iS10. Las medidas de difracción de rayos
X (DR-X) se midieron en un Difractómetro PAnalytical modelo X'pert PRO - MPD,
con tubos de generación de rayos X con ánodos de Cu (Cobre), Mo (Molibdeno) y Fe
(Hierro), operando a 45kV y 40mA con una λ = Cu-Kα. (1.54Å). El potencial Z se
midió en el equipo SZ-100 Horiba, realizando una prefiltración con microfiltros
de las soluciones acuosas previamente preparadas de los CDQs, N-CQDs y N-
CQDs/CYS respectivamente.
Resultado e discussão
Para la caracterización estructural se hicieron medidas de DR-X, FT-IR y
potencial Z. En los difractogramas de los CQDs se obtiene un ángulo de
difracción de (22,8) con una distancia interplanar de 0,389 nm que es
característica de los CQDs reportados en la literatura, atribuyendolo a planos
grafíticos dentro del material (PRASANNAN, A.; IMAE, T., 2013). Por otro lado,
para los N-CQDs se obtiene un ángulo más pequeño (20,6) aumentando la distancia
interplanar a 0,430 nm, debido a que al dopar con etilendiamina los planos
grafíticos se separan gracias a los grupos nitrogenados. Finalmente, para los N-
CQDs/CYS observamos que el ángulo de difracción se vuelve más grande (21,7) y la
distancia interplanar disminuye a 0,408 nm con respecto a los N-CQDs, esto se
debe a un efecto de compresión sobre los planos grafíticos que realiza la
cisteína que se funcionaliza. En la figura 1A, se muestra el espectro FT-IR de
los CQDs, en el que podemos evidenciar las bandas a 3399, 2935, 1705 y 1089 cm-1
debido a la presencia de los grupos funcionales O-H, C-H sp2, C=O, -COO- y C-OH
respectivamente, lo que nos indica un material carbonáceo rico en grupos
oxigenados como carboxilatos sin aparente presencia de grupos aminos (PRASANNAN,
A.; IMAE, T., 2013). Asimismo, en la figura 1B tenemos el FT-IR de los N-CQDs en
donde se puede observar los mismas bandas de los CQDs, además de las bandas a
3380, 2852 y 1460 cm-1 del N-H, C-H sp3 y C-N correspondientemente (CHANDRA, S.,
DAS, P., BAG, S., LAHA, D., PRAMANIK, P., 2011), lo que nos indica que los N-
CQDs fueron dopados correctamente con la etilendiamina aportando a su superficie
grupos aminos. Lo anteriormente mencionado se puede corroborar con las medidas
de potencial Z de los materiales en agua, siendo para el CQDs negativo (-17,4
mV) debido principalmente a los grupos -COO-, y para el N-CQDs positivo (+5,4
mV) debido principalmente a los grupos amonio. Estos valores del potencial Z
también nos están indicando que los materiales tienen una buena estabilidad
coloidal y solubilidad en medio acuoso. En la figura 1C, finalmente observamos
el FT-IR de los N-CQDs/CYS, en el que se pueden observar cambios pequeños pero
significativos en las bandas con respecto a los N-CQDs, que nos puede indicar la
funcionalización de la cisteína a la superficie del N-CQDs, por ejemplo, se
puede observar que la banda 1653 cm-1 (C=O del carboxilato) se transforma en dos
bandas a 1638 y 1560 cm-1 lo que nos indica formación de la amida (CHANDRA, S.,
DAS, P., BAG, S., LAHA, D., PRAMANIK, P., 2011). Por otro lado, también podemos
observar la disminución de la banda a 1375 cm-1 del carboxilato debido a que muy
probablemente la reacción de acoplamiento de amida se dio entre el carboxilato
de los N-CQDs y los grupos aminos de la cisteína. Adicionalmente, podemos
observar en el FT-IR de los N-CQDs/CYS un hombro a 2560 cm-1 (S-H) y una banda
a 572 cm-1 (C-S) lo que nos indica la presencia del grupo tiol de la cisteína en
estos materiales (MILENKOVIĆ, M., et al, 2021), este resultado se puede
corroborar debido al cambio del potencial Z que presenta los N-CQs (+5,4 mV) a
potenciales negativos (-15 mV) cuando se funcionaliza, debido principalmente al
grupo tiol cargado negativamente. Todo lo anterior nos indica una adecuada
funcionalización de los N-CQDs con cisteína para formar los N-CQDs/CYS. Para la
caracterización óptica se usó UV-VIS y fluorescencia. En la figura 2A tenemos
en color negro el espectro de absorción de los CQDs, N-CQDs y N-CQDs/CYS, en los
cuales se puede observar que la banda π-π* atribuida al (C=C del carbono
grafítico) que está alrededor de 270 nm se va moviendo levemente hacia el rojo,
disminuyendo su intensidad a medida de que los CQDs son dopados con nitrógeno y
posteriormente funcionalizados con cisteína. Asimismo, la banda n-π* se mueve
hacia el rojo, pero en este caso su intensidad aumenta indicándonos que el
material se está volviendo rico en heteroátomos y grupos funcionales cromóforos
como aminas y tioles, dotándolos de una mayor absorción en el visible (KIM, J.
K.; et al, 2013). En la figura 2A tenemos en color rojo los espectros de
fluorescencia de los CQDs, N-CQDs y N-CQDs/CYS en los que también se puede
observar un leve corrimiento hacia el rojo en el máximo de emisión (443, 448 y
458 nm) correspondientemente, debido al dopaje con nitrógeno y posterior
funcionalización con cisteína, lo anterior acompañado también de un incremento
en el rendimiento cuántico de fluorescencia de los materiales, siendo del 12%,
29% y 34% para el CQDs, N-CQDs y N-CQDs/CYS respectivamente. La fluorescencia
obtenida en los materiales excitando a 360 nm fue de color azul, siendo muy
parecida a la de los CQDs reportados en la literatura. Finalmente, en la figura
2B tenemos los espectros de fluorescencia de los CQDs, N-CQDs y N-CQDs/CYS en
los que podemos observar que la banda de fluorescencia se mueve hacia el rojo a
medida que cambiamos la longitud de onda de excitación a menor energía,
observando la propiedad característica de los CQDs de emisión multicolor, que se
atribuye al confinamiento cuántico y la variedad superficial de heteroátomos,
generando diferentes niveles de trampas de emisión fluorescente (KIM, J. K.; et
al, 2013). Teniendo en cuenta todos los resultados anteriormente descritos
podemos indicar que se obtuvieron N-CQDs, que absorben considerablemente en el
visible, tienen elevada fluorescencia y estabilidad coloidal, además, estos
materiales poseen un núcleo grafítico con una superficie rica en grupos aminos y
carboxilatos. Adicionalmente, estos N-CQDs fueron funcionalizados adecuadamente
con cisteína, sugiriendo un acoplamiento de amida entre los carboxilatos del N-
CQDs y la amina de la cisteína, obteniendo finalmente los N-CQDs/CYS con una
superficie rica en grupos tioles cargados negativamente, actuando como sitios de
coordinación para los iones mercurio, favoreciendo así su posteriormente
aplicación en la detección fluorescente de iones mercurio.
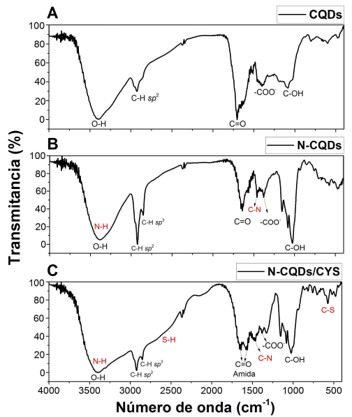
Espectros FT-IR (A) CQDs, (B) N-CQDs, (C) N-CQDs/CYS
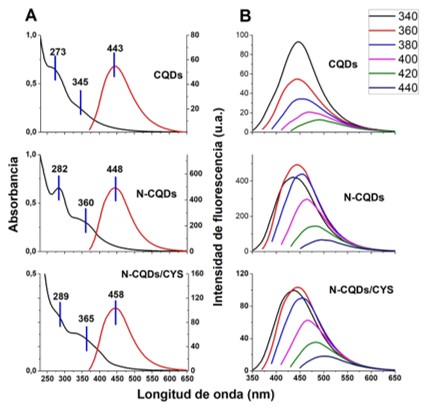
(A) Espectros UV-VIS y de fluorescencia excitando a 360 nm y (B) Espectros de fluorescencia excitando a diferentes longitudes de onda
Conclusões
Se sintetizaron N-CQDs a partir de cáscaras de chontaduro, obteniendo un material
semicristalino con un núcleo grafítico y una superficie rica en grupos amino y
carboxilato, adicionalmente presentó una elevada absorción y fluorescencia en el
visible con un rendimiento cuántico del 29%. Se obtuvieron NCQDs/CYS a partir de
la posterior funcionalización N-CQDs con cisteína (CYS) por medio de una reacción
de acoplamiento de amida, conservando así el núcleo grafítico, además, de una
superficie rica en grupos tioles cargado negativamente debido a la adecuada
funcionalización con cisteína. Este material también presentó un aumento en la
absorción y fluorescencia en el visible con respecto a los N-CQDs, incrementando
su rendimiento cuántico al 34%. Las características mencionadas hacen de los N-
CQDs/CYS excelentes candidatos para su posterior aplicación en la detección
fluorescente de iones mercurio.
Agradecimentos
Los autores desean agradecer al Departamento de Química, especialmente al grupo de
investigación de Síntesis Orgánica Sostenible y Nuevos Materiales Nano y
Supramoleculares de la Universidad Nacional de Colombia.
Referências
CHANDRA, S., DAS, P., BAG, S., LAHA, D., PRAMANIK, P. Synthesis, functionalization and bioimaging applications of highly fluorescent carbon nanoparticles. Nanoscale, v. 3, n. 4, 1533-1540, 2011.
DAS, R.; BANDYOPADHYAY, R.; PRAMANIK, P. Carbon quantum dots from natural resource: A review. Materials Today Chemistry, n. 8, 96–109, 2018.
DÍAZ, Á.; PRIETO, P.; DE LA HOZ, A. A Critical overview on the effect of microwave irradiation in organic synthesis. The
Chemical Record, v. 19, n.1, 85–97, 2019.
GU, D.; SHANG, S.; YU, Q.; SHEN, J. Green synthesis of nitrogen-doped carbon dots from lotus root for Hg (II) ions detection and cell Imaging. Applied Surface Science, v. 390, 38–42, 2016.
JELINEK, R. Carbon quantum dots synthesis, properties and applications. Springer International Publishing, Cham, 2004.
KIM, J. K., PARK, M. J.; KIM, S. J.; WANG, D. H.; CHO, S. P.; BAE, S.; PARK, J. H.; HONG, B. H. Balancing light absorptivity and carrier conductivity of graphene quantum dots for high-efficiency bulk heterojunction solar cells. Acs Nano, v. 7, n 8, 7207-7212, 2013.
LIU, Y.; JIANG, L.; LI, B.; FAN, X.; WANG, W.; LIU, P.; XU, S.; LUO, X. Nitrogen Doped Carbon Dots: Mechanism Investigation and Their Application for Label Free CA125 Analysis. Journal of Materials Chemistry B, v. 7, n. 19, 3053–3058, 2019.
MARTÍNEZ, J.; RODRÍGUEZ, X.; PINZÓN, L. X.; ORDÓÑEZ, L. E. Caracterización fisicoquímica de harina de residuos del fruto de Chontaduro (Bactris Gasipaes Kunth, Arecaceae) obtenida por secado convectivo. Ciencia y Tecnología Agropecuaria, v. 18, n. 3, 599–613, 2017.
PEARSON, R. G. Hard and soft acids and bases, HSAB, Part I: Fundamental Principles. Journal of Chemical Education, v. 45, n. 9, 581–587, 1968.
PRASANNAN, A.; IMAE, T. One-pot synthesis of fluorescent carbon dots from orange waste peels. Industrial & Engineering Chemistry Research, v. 52, n. 44, 15673-15678, 2013.
SIMÕES, E. F.; LEITÃO, J. M.; DA SILVA, J. C. Carbon dots prepared from citric acid and urea as fluorescent probes for hypochlorite and peroxynitrite. Microchimica Acta, v. 183, n. 5, 1769–1777, 2016.
YAN, F.; JIANG, Y.; SUN, X.; BAI, Z.; ZHANG, Y.; ZHOU, X. Surface modification and chemical functionalization of carbon dots: A review. Microchimica Acta, v.185, n. 9, 2018.
















