Autores
Silva, N.A.A. (UNIVERSIDADE FEDERAL FLUMINENSE) ; Martins, D.L. (UNIVERSIDADE FEDERAL FLUMINENSE) ; Xavier, R.F. (FUNDAÇÃO OSWALDO CRUZ) ; Rangel, L. (UNIVERSIDADE FEDERAL FLUMINENSE)
Resumo
A esquistossomose é uma doença parasitária causada por espécies de vermes do
gênero Shistosoma e que apresenta como hospedeiro intermediário caramujos, como o
Biomphalaria glabrata. Essa é a espécie mais associada à disseminação da
esquistossomose no Brasil e que precisa ser combatida através do emprego de
moluscicidas. Neste trabalho, foram preparadas naftoquinonas moluscicidas através
do acoplamento de Suzuki catalisado por paládio.
Palavras chaves
Biomphalaria glabrata; Suzuki; Esquistossomose
Introdução
A esquistossomose é a segunda doença parasitária que mais acomete indivíduos a
nível mundial, abaixo apenas da malária (CHITSULO, 2000). Esta doença é causada
por helmintos do gênero Schistosoma. No Brasil, a espécie mais comum deste
gênero é o Schistosoma mansoni (NELWAN, 2019). Para que ocorra o ciclo de
transmissão da doença, o parasita utiliza como hospedeiro intermediário
caramujos do gênero Biomphalaria; sendo o Biomphalaria glabrata a principal
espécie associada à transmissão da esquistossomose no Brasil (ZANARDI, 2019). O
controle e erradicação do B. glabrata está diretamente relacionado com a
interrupção do ciclo de transmissão da doença. Para isso, no entanto, apenas a
niclosamida (1) é utilizada em larga escala como pesticida (COELHO, 2016). Face
ao exposto, a pesquisa e desenvolvimento de novas substâncias com atividade
moluscicida que sejam seguras, de baixo custo e seletivas é de grande
importância para o controle da Esquistossomose.
Quinonas são substâncias naturais amplamente distribuídas na natureza, podendo
ser encontradas em plantas, fungos, bactérias, algas, vírus, insetos, entre
outros. As quinonas são constituídas de uma cadeia carbônica fechada e
insaturada contendo duas carbonilas adjacentes aos grupamentos vinílicos. Os
grupamentos carbonílicos podem estar em posições orto ou para entre si (DA
SILVA, 2013). No presente trabalho, foram sintetizadas 3-aril-2-hidróxi-1,4-
naftoquinonas através do emprego da reação de Suzuki entre ácidos arilborônicos
e a 3-iodo-2-hidróxi-1,4-naftoquinona. As substâncias obtidas tiveram sua
atividade moluscicida avaliada frente ao B. glabrata (MARTINS, 2022).
Material e métodos
Inicialmente foi preparado o complexo 1 para iodação da naftoquinona. Para isto,
utilizou-se KI (280 mmol),I2 (100 mmol) e morfolina (100 mmol) em água. Na
sequência, a lausona 2 (30 mmol), K2CO3 (90 mmol) e o complexo morfolino-iodo
(37,5 mmol) foram submetidos à agitação magnética em meio aquoso (30 min). Após
acidificação da mistura de reação, obteve-se a 2-hidróxi-3-iodo-1,4-
naftoquinona 3 (3-iodolausona).
A 3-iodolausona 3 foi empregada em reações de acoplamento C-C junto à
diferentes ácidos fenilborônicos. Para isto, as reações foram submetidas, por 10
minutos, à irradiação de micro-ondas à 100°C. No tubo de reação,foram
adicionados 2-hidróxi-3-iodo-1,4-natoquinona 3 (0,5 mmol), K2CO3 (2,5 mmol),
ácido arilborônico (0,75 mmol), Pd(OAc)2 (1% mol) como catalisador e água
destilada como solvente. Os produtos obtidos foram caracterizados por 1H e 13C-
RMN e espectroscopia na região do IV e seus pontos de fusão capilares não
corrigidos foram determinados.
Resultado e discussão
Foram preparadas diferentes 3-aril-2-hidróxi-1,4-naftoquinonas através de reação
de Suzuki (Esquema 1).A concentração letal das naftoquinonas foi determinada
pela exposição do B. glabrata aos compostos por 48 horas (Figura 1). AN-12, 13,
15 e 16 foram as mais potentes, o que parece indicar que a presença de
substituintes polares no anel fenílico leva a melhores atividades. Observou-se
que substâncias que apresentaram melhor atividade moluscicida possuem
substituintes retiradores de elétrons no anel benzênico, que são as substâncias
AN-15 e AN-16. AN-15 apresentou os melhores resultados (CL90 0,98ppm) (Figura1).
Os estudos in sílico demostraram menor toxicidade ambiental para AN-15, quando
comparado com a niclosamida.
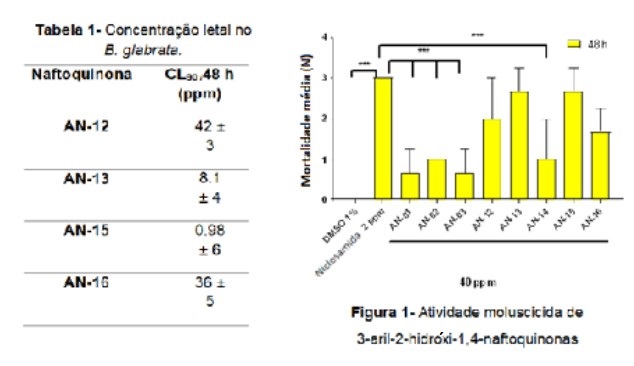
Concentração letal (CL90) de arilnaftoquinonas frente ao B. glabrata
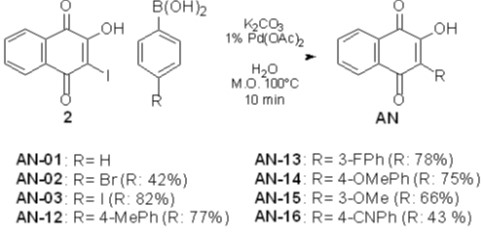
Reação de Suzuki para obtenção de 3-Aril-2-hidróxi-1,4-naftoquinonas
Conclusões
A molécula sintética AN-15 apresentou boa atividade moluscicida frente ao B.
glabrata com potência superior à niclosamida, o moluscicida aprovado pela OMS. O
potencial do AN-15 no combate do caramujo hospedeiro sugere que a classe das
naftoquinonas pode ser promissora no desenvolvimento de agentes moluscicidas de
importância no combate à esquistossomose.
Agradecimentos
Os autores agradecem à CNPq (Processo n° 308755/2018-9), FAPERJ (Processo N° E-
26/203.246/2017 e Processo N° E-26/211.025/2019) e CAPES.
Referências
CHITSULO, L. et al. The global status of schistosomiasis and its control. Acta Tropica, v.77, 41-51, 2000.
COELHO, P. M. Z., Caldeira, R.L. Critical analysis of molluscicide application in schistosomiasis control programs in Brazil. Infectious Diseases of Poverty, v. 5, 56-6, 2016.
DA SILVA, M. N. et al. Um panorama atual da química e da farmacologia de naftoquinonas, com ênfase na beta-lapachona e derivados. Química Nova, v. 26, 407-416, 2013.
MARTINS, D. L. et al. Molluskicidal activity of 3-aryl-2-hydroxy-1,4-naphthoquinones against Biomphalaria glabrata. Acta Tropica, v. 231,106414-106427, 2022.
NELWAN, M. Schistosomiasis: Life Cycle, Diagnosis, and Control. Current Therapeutic Research, Clinical and Experimental, v. 91, 5-9, 2019.
ZANARDI, V. S. et al. Prevalence of Infection of Biomphalaria glabrata by Schistosoma mansoni and the risk of urban Schistosomiasis mansoni in Salvador, Bahia, Brazil, Revista da Sociedade Brasileira de Medicina Tropical, v. 52:e20190171, 1-9, 2019.
















