Autores
Miranda de Farias, P.H. (UFPE) ; Brito de Medeiros, L.F. (UFPE) ; de Sá Magalhães Vieira, G. (UFPE) ; Bezerra de Moraes Medeiros, E. (UFPE) ; Medeiros de Lima Filho, N. (UFPE)
Resumo
A baixa demanda de glicerol no mercado e sua alta oferta, refletem na
necessidade
de novas rotas sintéticas para valorização desse subproduto industrial. Foram
realizados experimentos de oxidação catalítica do glicerol para produção de
ácido
glicérico. O catalisador utilizado foi níquel dopado com paládio suportados em
carvão ativado. As reações foram conduzidas em um reator encamisado batelada e
um
banho termostático. Foi realizado um planejamento fatorial para avaliar a
influência de três parâmetros: temperatura, razão molar NaOH/glicerol e vazão de
oxigênio. A temperatura foi o parâmetro mais significativo. Foram encontrados
valores de conversão da matéria prima e seletividade na produção de ácido
glicérico
nos valores de 39% e 91%, respectivamente.
Palavras chaves
Oxidação catalítica; Glicerol; Ácido Glicérico
Introdução
O biodiesel é um combustível renovável produzido a partir de óleos de fontes
animais e vegetais, que pode ser utilizado sozinho ou em blendas de quaisquer
proporções. A rápida expansão do biodiesel gerou um acumulo produtivo do
glicerol, seu principal subproduto, já que a quantidade gerada se aproxima de
10-20% do combustível. Esse triol é uma molécula altamente funcionalizada, capaz
de percorrer várias vias e gerar vários produtos importantes para as indústrias
alimentícias, farmacêuticas e de cuidados pessoais, podendo ser utilizada como
solvente ou como composto intermediário para sínteses (Zhang, 2021; Brainer,
2014; Wolski, 2020).
Os principais produtos das reações do glicerol são a 1,3 – dihidroxiacetona
(DHA), ácido glicérico (GA), gliceraldeído (GLYAD), ácido tartrônico (TA) e
ácido purúvico (PA), como pode ser vista na Figura 1. Esses produtos podem ser
obtidos ela oxidação estequiométrica com a utilização de ácidos minerais, porém
essa produção é danosa ao meio ambiente, sendo preferível a utilização de
catalisadores heterogêneos de metais nobres e oxigênio molecular. Com a sua
utilização, a seletividade da reação é bastante sensível, sendo dependente das
condições da reação, como pH, temperatura, razão substrato-metais, natureza do
suporte e estruturas geométricas e elétricas das nanopartículas metálicas (He,
2021; Demirel-Güllen, 2005).
Diversos trabalhos na literatura citam a utilização de platina, paládio e ouro,
como metais seletivos para oxidação do glicerol, com alta seletividade para
ácido glicérico, porém os dois últimos sendo mais seletivos em meios básicos.
Entretanto são citadas também melhoras com a utilização de catalisadores
bimetálicos, levando a uma estabilização termodinâmica mais favorável à reação e
a um efeito bifuncional na interação com os reagentes, sendo aplicado tanto na
oxidação em reatores batelada quanto em oxidações eletroquímicas (Muneeb, 2016;
Ribeiro, 2012; Freitas, 2018). Essa combinação de fatores pode influenciar
diretamente os resultados de seletividade que se busca em relação a reação.
Neste sentido, o objetivo geral do trabalho é estudar a oxidação do glicerol
seletiva em ácido glicérico por meio da utilização de catalisador bimetálico de
Ni(10%)-Pd(1%)/CA. Serão variados parâmetros reacionais como concentração de
hidróxido de sódio, fazendo valer a influência da razão molar NaOH/glicerol,
vazão volumétrica de oxigênio e temperatura, por meio de um planejamento
fatorial. De modo, a observar as respostas em termos de seletividade, conversão
e rendimento.
Material e métodos
Ensaio de oxidação do Glicerol
A oxidação do glicerol foi realizada no reator encamisado de temperatura
controlada por meio de um banho ultra termostático. Nele consta de um agitador
mecânico, poço para remoção dos produtos da reação, tubulação de adição de
oxigênio no seio do líquido, condensador e termopar para aferição da temperatura
reacional.
A reação ocorre por meio da adição do glicerol, hidróxido de sódio, oxigênio e
do catalisador no reator de 700 ml. As condições da reação serão variadas por
meio do planejamento fatorial desenvolvido.
Planejamento fatorial dos experimentos
Observaremos a influência do hidróxido de sódio pela sua variação nas
concentrações de 40 e 60g/L. Já em relação a vazão de O2 serão realizadas sua
variação nas vazões de 100 e 150L/h. A temperatura da reação será variada em 40
e 60°C.
Resultado e discussão
De posse dos dados da tabela 1, observa-se que a melhor condição, de resposta
combinada, foi obtida pelos níveis positivos de todos os fatores utilizados no
planejamento fatorial, com valores de conversão do glicerol e seletividade à
ácido glicérico de 39% e 91%, respectivamente.
Além disso, a modificação da temperatura se mostrou o fator determinante na
variação dos parâmetros da reação. A comparação entre os níveis baixos e altos,
a partir dos ensaios 7 e 8, indicaram uma melhora de quase 490% da conversão do
glicerol, consequência direta de um favorecimento cinético pelo aquecimento do
sistema reacional.
Foi observada a influência da vazão de oxigênio na condução da reação. A
modificação do fator se mostrou pouco efetiva quanto a melhoria dos parâmetros
de resposta. Analisando os ensaios 1 e 3, por exemplo, não há variação
significativa na conversão ou seletividade. Algo que pode ser justificado por,
mesmo na condição de menor nível, já existir alta concentração de oxigênio nos
poros do catalisador, fazendo com que seu aumento não influencie na cinética da
reacional.
Outro fator observado foi a variação da concentração de hidróxido de sódio.
Comparativamente com relação a temperatura, o seu efeito em a resposta foi menos
efetivo, como pode ser observado na conversão do glicerol. Há uma melhoria
aproximada de 50% em sua conversão, a partir dos ensaios 4 e 8.
Em relação a seletividade, pode-se notar que, ao modificarmos em conjunto os
fatores que tem influencia na reação, ou seja, temperatura e concentração da
base, observa-se pelos ensaios 3 e 8 a ocorrência de uma redução da seletividade
à ácido glicérico, mas um aumento da conversão do glicerol. Por favorecermos o
desenvolvimento da reação, o glicerol é convertido em outros subprodutos comuns
da reação de oxidação assim como o ácido glicérico, obtendo como resposta uma
redução no parâmetro da seletividade. Entretanto, em relação ao rendimento, o
ensaio número 8 se mostrou o melhor, visto que temos a maior seletividade em
comparação com a conversão, com um valor de 39%.
Como a reação é realizada em meio alcalino, a presença do hidróxido de sódio
forma os sais carboxilatos dos respectivos ácidos produzidos. No entanto, ao
analisar na cromatografia, pela fase móvel ser meio ácido, os produtos são
convertidos em seus ácidos carboxílicos e assim analisados.
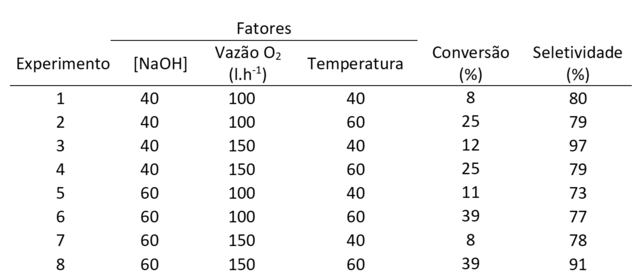
Valores de conversão e seletividade.

Conclusões
Diante do exposto, pode-se concluir que o parâmetro que mais interfere na reação
de oxidação catalítica do glicerol é a temperatura. Além disso, para um maior
rendimento para produção do ácido glicérico, as melhores condições encontradas
foram uma concentração de hidróxido de sódio de 60g/l, uma temperatura de 60°C e
uma vazão de oxigênio de 150 l/h.
Agradecimentos
Os agradecimentos vão para o Laboratório de Processos Catalíticos, onde foi
possível realizar os experimentos.
Ao CNPQ, CAPES e FACEPE pelo fomento à pesquisa.
À Universidade Federal de Pernambuco.
Referências
BRAINER, J. E. N. et al. Wet oxidation of glycerol into fine organic acids: catalyst selection and kinetic evaluation. Brazilian Journal of Chemical Engineering, v. 31, n. 4, p. 913-923, 2014.
DEMIREL-GÜLEN, Séval; LUCAS, Martin; CLAUS, Peter. Liquid phase oxidation of glycerol over carbon supported gold catalysts. Catalysis Today, v. 102, p. 166-172, 2005.
FREITAS, Luís Fonseca de. Oxidação do glicerol em reator de leito de lama laboratorial para produção seletiva de ácido glicérico e derivados empregando catalisadores de Pd/C, Cu-Pd/C e Ni-Pt/C. 2018.
HE, Zhiyan et al. Selective oxidation of glycerol over supported noble metal catalysts. Catalysis Today, v. 365, p. 162-171, 2021.
MUNEEB, Omar et al. Electrochemical oxidation of polyalcohols in alkaline media on palladium catalysts promoted by the addition of copper. Electrochimica Acta, v. 218, p. 133-139, 2016.
RIBEIRO, Lucília Graciosa de Sousa et al. Catalisadores suportados em nanotubos de carbono para a oxidação seletiva de glicerol. 2012.
WOLSKI, L. Factors affecting the activity and selectivity of niobia-based gold catalysts in liquid phase glycerol oxidation. Catalysis Today, v. 354, p. 36-43, 2020.
ZHANG, Mengyuan et al. Reduced graphene oxide decorated with PtCo bimetallic nanoparticles: facile fabrication and application for base-free oxidation of glycerol. Catalysis Today, v. 298, p. 234-240, 2017.
















