Autores
Bejarano R., N. (CENTRO DE ESTUDIO DE COMPUESTOS ORGANICOS-UNLP) ; Esteche, J. (CENTRO DE ESTUDIO DE COMPUESTOS ORGANICOS-UNLP) ; Santiago, C. (CENTRO DE ESTUDIO DE COMPUESTOS ORGANICOS-UNLP) ; Guaymas, O. (CENTRO DE ESTUDIO DE COMPUESTOS ORGANICOS-UNLP) ; Ponzinibbio, A. (CENTRO DE ESTUDIO DE COMPUESTOS ORGANICOS-UNLP)
Resumo
Los glicósidos que en su estructura contienen grupos funcionales amino en las
distintas posiciones del anillo son de interés por ser generalmente bioactivos.
Este tipo de carbohidratos suelen encontrarse en numerosos medicamentos como
subestructuras de antibióticos como la neomicina. Los antecedentes sobre el
estudio de la síntesis de amino azúcares son escasos. En este trabajo se
sintetizaron una serie de derivados de 6-amino-6-deoxigalactopiranosas a partir
de D-galactosa. Se realizó una reacción de condensación utilizándose anilinas
sustituidas con halógenos en distintas posiciones y un azúcar con una función
aldehído para obtener iminas. Y estas fueron reducidas para obtener todas las
moléculas objetivo cuyas estructuras fueron confirmadas mediante espectroscopia
de RMN.
Palavras chaves
Síntesis orgánica; amino azúcares; haloanilinas
Introdução
Los carbohidratos son las biomoléculas orgánicas más abundantes en la naturaleza
(STICK, 2001) y están involucrados en numerosas funciones vitales en los
organismos (WONG et al., 2019). La síntesis orgánica de derivados de hidratos de
carbono se constituye en un área de investigación relevante. El desarrollo de
nuevos métodos de síntesis permite preparar compuestos naturales o derivados
sintéticos con el objetivo de ser empleados en áreas como diseño de fármacos,
agroquímicos, aditivos, cosméticos, entre otros (LEVY et al., 2006). En
particular los glicósidos que tienen sustituyentes amino unidos en las distintas
posiciones del anillo son de interés como subestructuras de antibióticos. (ROTH
et al., 2000). Este trabajo tiene como objetivo la síntesis y el análisis
estructural de nuevos compuestos derivados de la D- galactosa que cuenten con
una función amino sustituida en el C6 utilizando anilinas halogenadas.
Material e métodos
Se realizó una reacción de protección selectiva de los grupos hidroxilo de la D-
galactosa utilizando acetona, CuSO4 y H2SO4 como catalizador. La oxidación del
hidroxilo libre del C6 se llevó adelante con dimetilsulfóxido y
diciclohexilcarbodiimida (DMSO/DCC). A continuación, se realizó una reacción de
condensación del aldehído con distintas haloanilinas utilizando diclorometano
anhidro como solvente de reacción. Por último, las iminas obtenidas fueron
reducidas con un hidruro, en este trabajo se utilizó NaBH4 e isopropanol como
solvente. Los productos fueron aislados y purificados por cromatografía en
columna. Las estructuras se determinaron de manera inequívoca mediante RMN
analizando espectros de 1H, 13C, gHSQC y gCOSY.
Resultado e discussão
Para la obtención de estos nuevos compuestos se propuso la ruta sintética
representada en la Imagen 1.
La preparación de 1,2;3,4-di-O-isopropiliden-α-D-galactopiranosa se llevó a cabo
siguiendo técnicas conocidas (RAUTER et al., 1995) y probadas en nuestro
laboratorio con anterioridad. Para la oxidación de hidroxilos primarios, uno de
los métodos más ampliamente utilizados emplea DMSO/DCC (MILJKOVIĆ, 2010).
Siguiendo esta técnica se obtuvo como producto un glicósido con una función
aldehído en C6. En general, las reacciones de aldehídos con aminas ocurren
mediante un mecanismo de adición-condensación, en ésta la adición es el primer
paso que da origen a una especie intermediaria carbinolamina y la segunda etapa
es la condensación en donde se elimina una molécula de agua (CIACCIA, 2015).
Cuando la reacción se da con una amina primaria se generan iminas, en este caso
las aminas utilizadas fueron haloanilinas. Y finalmente, las 6-amino-6-
deoxigalactopiranosas sustituidas fueron obtenidas por reducción de las iminas
correspondientes siguiendo técnicas estándar. Todas las estructuras de los
compuestos sintetizados fueron analizadas y confirmadas mediante espectroscopia
de resonancia magnética nuclear (RMN).
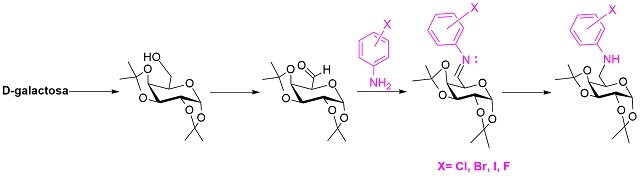
Esquema completo de síntesis de 6-amino-6- deoxigalactopiranosas
Conclusões
Se diseñó una ruta de síntesis con el objetivo de preparar derivados de 6-amino-6-
deoxigalatopiranosas a partir de la D-galactosa. Se sintetizaron nuevos compuestos
empleando variadas técnicas de síntesis, aislamiento y purificación. Se realizó un
estudio estructural completo de todos los productos de síntesis mediante técnicas
de RMN de 1H y 13C y bidimensionales gHSQC y gCOSY logrando elucidar sus
estructuras de manera inequívoca.
Agradecimentos
Los autores agradecen a la UNLP, a la Comisión de Investigaciones Científicas de
la Provincia de Buenos Aires y al CONICET por el financiamiento prestado para
llevar a cabo el presente trabajo.
Referências
CIACCIA, M.; DI STEFANO, S. Mechanisms of imine exchange reactions in organic solvents. Organic & Biomolecular Chemistry, 13, 646-654, 2015.
LEVY, D. E.; FÜGEDI, P. The Organic Chemistry of Sugars. Primera edición, 2006.
MILJKOVIĆ, M. Oxidation of Monosaccharides. En Carbohydrates. Springer, 245-290, 2010.
RAUTER, et al. A new method of acetonation with the zeolite HY as catalyst. Synthesis of O-Isopropylidene sugar derivatives. Tetrahedron,51, 6529-6540, 1995.
ROTH, H. J.; FENNER, H. Arzneistoffe: Struktur-Bioreaktivität-wirkungsbezogene Eigenschaften; mit etwa 2500 Strukturformeln. Dt. Apotheker-Verlag, 65-72, 2000.
STICK, R. V. Carbohydrates: the sweet molecules of life. Elsevier, 2001.
WONG, C. H.; KRASNOVA, L. Highlights in Chemical Glycobiology. Israel Journal of Chemistry, 59, 18-22, 2019.
















