Aumento da solubilidade de Norfloxacino através da cocristalização farmacêutica
- Home
- Trabalhos
ÁREA
Química Analítica
Autores
Costa, G.P. (UNESP BAURU) ; Ferreira, P.O. (UNESP BAURU) ; de Almeida, A.C. (UNESP BAURU) ; Ekawa, B. (UNESP ARARAQUARA) ; Ferreira, L.T. (UNESP ARARAQUARA) ; Caires, F.J. (UNESP BAURU)
RESUMO
Cocristais farmacêuticos são sistemas multicomponentes capazes de melhorar as propriedades físico-químicas de substâncias farmacologicamente ativas, tais como solubilidade e dissolução. Uma vez que, o Norfloxacino (NOR) é um antibiótico que apresenta baixa solubilidade aquosa, foi realizada a cocristalização através do liquid assisted grinding utilizando como coformador o Ácido Pirazinóico (PZCA). A caracterização do sistema formado abrangeu técnicas termoanalíticas (TG-DTA e DSC), difratométrica (DRXP) e espectroscópica (FTIR). Após a confirmação da formação do cocristal NOR-PZCA, a avaliação da solubilidade foi realizada através do método shake-flask, mostrando que esta abordagem aumentou a solubilidade do NOR em 26,4 vezes.
Palavras Chaves
COCRISTAL; NORFLOXACINO; SOLUBILIDADE
Introdução
Diversos fármacos possuem baixa solubilidade aquosa, reduzindo sua absorção no organismo, em consequência disto, estes são administrados em maiores doses diárias e por um período maior de tempo, podendo causar efeitos adversos nos pacientes (BHATTACHARYA et al., 2018; BREDA et al., 2009). Em vista disso, a formação de cocristais é uma abordagem que visa a melhora das propriedades físico-químicas dos fármacos em desenvolvimento e já comercializados (KAVANAGH et al., 2019). Os cocristais farmacêuticos são formas sólidas cristalinas multicomponentes, formadas por interações intermoleculares não covalentes (formando também synthons supramoleculares) entre o insumo farmacêutico ativo (IFA) e um ou mais coformadores (DE ALMEIDA et al., 2020; JAYRAM; SUDHEER, 2020). A vantagem da formação de cocristais através das interações intermoleculares é devido a capacidade de não interferência na atividade terapêutica do fármaco, além de que contribui de forma positiva nas propriedades físico-químicas, como solubilidade e taxa de dissolução (BHATTACHARYA et al., 2018; BOLLA; NANGIA, 2016; ROCHA et al., 2016). O Norfloxacino (NOR) é um antibiótico de amplo espectro utilizado no tratamento de diversas doenças infecciosas como gonorreia, infecções da próstata e outras infecções do trato gastrointestinal e do trato urinário (BARBAS; PROHENS; PUIGJANER, 2007; P. FERREIRA et al., 2019). Contudo, o NOR é classificado na classe IV do sistema de Biopharmaceutical classification System devido sua baixa solubilidade aquosa e baixa permeabilidade (BASAVOJU; BOSTRÖM; VELAGA, 2006). Neste contexto, a formação de cocristais farmacêuticos de Norfloxacino é uma abordagem de significativa relevância científica, social e econômica.
Material e métodos
Os cocristais foram sintetizados pelo método mecanoquímico, utilizando moinho de bolas vibratório da RETSCH, modelo MM 400, com emprego de solvente, após a síntese os sistemas foram colocados em estufa com circulação e renovação de ar para a eliminação do solvente residual. Para a caracterização dos sistemas foram utilizadas as técnicas termoanalíticas: Termogravimetria e Análise Térmica Diferencial Simultânea (TG-DTA) no equipamento da NETZSCH, modelo STA 449 Jupiter, razão de aquecimento de 10 °C min-1, atmosfera de ar sintético com vazão de 50 mL min-1 e intervalo de temperatura de 30-800 °C e Calorimetria Exploratória Diferencial (DSC) utilizando o equipamento DSC 1 STARe System da METTLER TOLEDO, razão de aquecimento de 10 °C min-1, atmosfera de ar sintético com vazão de 50 mL min-1; difratométrica: Difratometria de Raios X do Pó (DRXP) no difratômetro da RIGAKU, Modelo MiniFlex, utilizando tubo de cobre, submetido a 40 kV, corrente de 15 mA, Cu κα, λ = 1,54056 Å, 5 ≤ 2θ ≤ 50, no modo de varredura contínuo, com velocidade de 4° min-1 e espectroscópica: Espectroscopia Vibracional de Absorção na Região do Infravermelho (FTIR) no espectrômetro da Thermo Scientific, modelo Nicolet iS10, através da técnica de refletância total atenuada com cristal de germânio, no intervalo de 675 cm-1 a 4000 cm- 1, resolução de 4 cm-1 e 32 acumulações por espectro. Para o estudo da solubilidade foi utilizado o método do shake-flask em uma incubadora shaker da Marconi, modelo MA 410 com leituras em triplicata no comprimento de onda em 277 nm em um espectrofotômetro UV-VIS da Agilent Technologies, modelo Cary 8454 utilizando a metodologia de quantificação do NOR validada no UV- Vis (CHIERENTIN; SALGADO, 2014).
Resultado e discussão
A confirmação da formação do cocristal NOR-PZCA foi evidenciada por: (1) no
TG-DTA e DSC (Figura 1 (a) e (b)) o sistema apresentou estabilidade térmica
intermediária (235,2 °C) e ponto de fusão superior (254,8 °C) aos
componentes isolados, o que indica a formação de uma nova forma sólida
multicomponente. (2) no DRXP (Figura 1 (c)) o sistema apresentou um novo
padrão de difração que difere de seus percursores isolados, evidenciado pela
formação de novos picos de difração em 2θ igual a 5,88°; 13,55°; 23,54°;
27,04° e 28,44°, indicando que o sistema formado apresenta um novo composto
multicomponente cristalino. (3) No FTIR (Figura 1 (d)) foi observado
mudanças nos padrões espectroscópicos, sendo os mais relevantes para o
estudo: o deslocamento da banda do PZCA C-N para menores frequências (1311
cm-1 para 1363 cm-1), a redução da intensidade da banda do NOR em 1250 cm-1
que é atribuída ao estiramento da amina alifática ( C-N) e a mudança de
padrão de bandas do fármaco e do coformador na região de 3100 cm-1 até 2600
cm-1, esses resultados sugerem a formação de uma interação intermolecular
dos componentes através do grupo amina, confirmando que a nova forma sólida
multicomponente cristalina formada é um cocristal de NOR-PZCA. O cocristal
NOR-PZCA formado, foi submetido ao estudo da solubilidade, os resultados
obtidos (Figura 2 (a)), foram colocados em comparação com os dados do NOR
isolado e mostraram uma melhora de 26,4 vezes na solubilidade aquosa (Figura
2 (b)), evidenciando que a cocristalização farmacêutica atingiu o objetivo
de melhorar a solubilidade do fármaco.

Análises de (a) TG-DTA, (b) DSC, (c) DRXP e (d) FTIR do sistema NOR-PZCA e seus percursores.
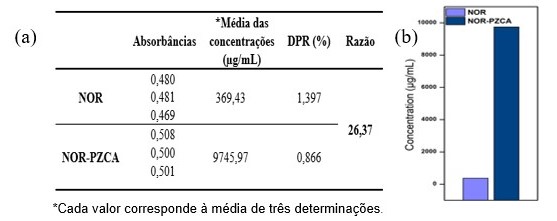
(a)Valores de absorbâncias, média de concentrações, DPR e razão do cocristal (b) Gráfico das concentrações do NOR e do cocristal em sistema aquoso.
Conclusões
A metodologia utilizada foi assertiva para a formação de um cocristal, evidenciado pela mudança da estabilidade térmica e ponto de fusão; presença de um novo padrão de difração; e deslocamento e mudanças na intensidade de bandas espectroscópicas. O estudo da solubilidade mostrou-se favorável e condizente com o esperado, revelando que o cocristal NOR-PZCA possui maior solubilidade aquosa que o NOR. Os resultados asseguram que a cocristalização farmacêutica é uma abordagem efetiva para a melhora da solubilidade de fármacos em desenvolvimento e já comercializados.
Agradecimentos
FAPESP: Proc. 2017/14936-9, 2018/12463-9, 2020/07724-8 CNPq: Proc. 143246/2017-8 CAPES PrInt: Proc. 88887.582123/2020-00 CAPES: Proc. 88887.495141/2020-00
Referências
BARBAS, R.; PROHENS, R.; PUIGJANER, C. A new polymorph of Norfloxacin. Journal of Thermal Analysis and Calorimetry, [s. l.], v. 89, n. 3, p. 687–692, 2007. Disponível em: <http://scripts.iucr.org/cgi-bin/paper?S1600536807016455>
BASAVOJU, S.; BOSTRÖM, D.; VELAGA, S. P. Pharmaceutical Cocrystal and Salts of Norfloxacin. Crystal Growth & Design, [s. l.], v. 6, n. 12, p. 2699–2708, 2006. Disponível em: <https://pubs.acs.org/doi/10.1021/cg060327x>
BHATTACHARYA, B.; MONDAL, A.; SONI, S. R.; DAS, S.; BHUNIA, S.; BAL RAJU, K.; GHOSH, A.; MALLA REDDY, C. Multidrug salt forms of norfloxacin with non-steroidal anti-inflammatory drugs: solubility and membrane permeability studies. CrystEngComm, [s. l.], v. 20, n. 41, p. 6420–6429, 2018. Disponível em: <http://xlink.rsc.org/?DOI=C8CE00900G>
BOLLA, G.; NANGIA, A. Pharmaceutical cocrystals: walking the talk. Chemical Communications, [s. l.], v. 52, n. 54, p. 8342–8360, 2016. Disponível em: <https://www.ncbi.nlm.nih.gov/pubmed/27278109%0Ahttp://pubs.rsc.org/en/Content/ArticleLanding/2016/CC/C6CC02943D>
BREDA, S. A.; JIMENEZ-KAIRUZ, A. F.; MANZO, R. H.; OLIVERA, M. E. Solubility behavior and biopharmaceutical classification of novel high-solubility ciprofloxacin and norfloxacin pharmaceutical derivatives. International Journal of Pharmaceutics, [s. l.], v. 371, n. 1–2, p. 106–113, 2009. Disponível em: <https://linkinghub.elsevier.com/retrieve/pii/S0378517308008600>
CHIERENTIN, L.; SALGADO, H. R. N. Performance Characteristics of UV and Visible Spectrophotometry Methods for Quantitative Determination of Norfloxacin in Tablets. Journal of Scientific Research, [s. l.], p. 12, 2014.
DE ALMEIDA, A. C.; FERREIRA, P. O.; TORQUETTI, C.; EKAWA, B.; CARVALHO, A. C. S.; DOS SANTOS, E. C.; CAIRES, F. J. Mechanochemical synthesis, characterization and thermal study of new cocrystals of ciprofloxacin with pyrazinoic acid and p-aminobenzoic acid. Journal of Thermal Analysis and Calorimetry, [s. l.], v. 140, n. 5, p. 2293–2303, 2020. Disponível em: <https://doi.org/10.1007/s10973-019-08958-3>
JAYRAM, P.; SUDHEER, P. Pharmaceutical co-crystals : a systematic review. International Journal of Pharmaceutics, [s. l.], v. 10, n. 3, p. 246–252, 2020.
KAVANAGH, O. N.; CROKER, D. M.; WALKER, G. M.; ZAWOROTKO, M. J. Pharmaceutical cocrystals: from serendipity to design to application. Drug Discovery Today, [s. l.], v. 24, n. 3, p. 796–804, 2019. Disponível em: <https://doi.org/10.1016/j.drudis.2018.11.023>
P. FERREIRA, P. O.; TORQUETTI, C.; ALMEIDA, A. C. De; CARVALHO, É. Thermoanalytical study of a new norfloxacin solvate. Brasilian Journal of Thermal Analysis, [s. l.], p. 1–7, 2019.
ROCHA, A. B. O.; KUMINEK, G.; MACHADO, T. C.; ROSA, J.; RAUBER, G. S.; BORBA, P. A.; SIEDLER, S.; STULZER, H. K.; CUFFINI, S. L.; RODRIGUEZ-HORNEDO, N.; CARDOSO, S. G. Cocristais: uma estratégia promissora na área farmacêutica. Química Nova, [s. l.], v. 39, n. 9, p. 1112–1125, 2016. Disponível em: <http://quimicanova.sbq.org.br/audiencia_pdf.asp?aid2=6497&nomeArquivo=RV20160069.pdf>


