Novos alilditiocarbimatos para o controle de Alternaria Solani
- Home
- Trabalhos
ÁREA
Química Orgânica
Autores
Vidigal, A.E.C. (UFV) ; Rubinger, M.M.M. (UFV) ; Pereira, A.B.D. (UFV) ; Zambolim, L. (UFV)
RESUMO
Os ditiocarbimatos são espécies químicas ainda pouco estudadas. Recentemente, foi descoberta a atividade antifúngica de alilditiocarbimatos obtidos a partir de derivados do benzaldeído e de sulfonilditiocarbimatos. Este trabalho descreve a síntese de sais inéditos de alilditiocarbimatos a partir de derivados do 4-trifluorometilbenzaldeido e de oito arilsulfonilditiocarbimatos, contendo o cátion tetrafenilfosfônio. Os novos compostos foram caracterizados por suas massas exatas (HRMS), espectroscopias vibracional e de ressonância magnética nuclear de 1H e 13C. A atividade dos compostos foi testada contra Alternaria solani, causador de doenças em batata e tomate. Os resultados mostraram significativa atividade antifúngica dos compostos sintetizados.
Palavras Chaves
Alilditiocarbimatos; Alternaria solani; Fungicidas
Introdução
Doenças em plantas podem reduzir drasticamente a produção de alimentos. O uso de fungicidas em alguns casos é a única ferramenta disponível para o controle dos patógenos, evitando severas perdas econômicas, podendo muitas vezes ser associado a outras ações como a rotação de culturas e o uso de controle biológico. Os ditiocarbamatos são usados como fungicidas em larga escala desde a década de 1940, puros ou em misturas com fungicidas sistêmicos específicos (HEARD, 2005). Os ditiocarbimatos são estruturalmente semelhantes aos ditiocarbamatos, porém bem menos estudados. A literatura reporta a atividade antifúngica de alilditiocarbimatos obtidos a partir de derivados do benzaldeído e de sulfonilditiocarbimatos contra Botrytis cinerea (TAVARES et al, 2016). Os resultados promissores reportados indicam que a ampliação dessas pesquisas com a síntese de compostos análogos e a inclusão de testes com outros fungos patogênicos tem potencial para a descoberta de novos antifúngicos de aplicação agrícola. A presença de halogênios, em especial o flúor, em moléculas biologicamente ativas usualmente acarreta importantes alterações nas atividades observadas (FUJIWARA e O’HAGAN, 2014). Assim, este trabalho descreve a síntese de novos alilditiocarbimatos contendo o grupo trifluorometila. As novas substâncias foram testadas frente a Alternaria solani, importante patógeno causador da doença pinta preta, que se manifesta por lesões nas folhas, além de podridão em frutos e bulbos. Em muitas regiões esta é a principal doença da batata (HORSFIELD et al., 2010).
Material e métodos
A Figura 1 apresenta a rota sintética utilizada para a preparação dos novos alilditiocarbimatos. O brometo alílico de partida (A) foi preparado a partir de 4-trifluorometilbenzaldeído e acrilato de metila, e reação do aduto resultante com brometo de lítio em meio ácido, conforme descrito na literatura (FERREIRA et al, 2009). A preparação dos ditiocarbimatos de potássio, K2(R-SO2N=CS2), foi feita segundo procedimento semelhante ao descrito na literatura (OLIVEIRA e De Bellis, 1999), a partir das sulfonamidas primárias contendo grupos R aromáticos (1-8) em reação com dissulfeto de carbono e hidróxido de potássio em solução de dimetilformamida. Os oito compostos inéditos (Z)-2-(metoxicarbonil)-3-(4- (trifluorometil)fenil-R-sulfonilcarbonimidoditioatos de tetrafenilfosfônio foram obtidos a partir da reação do brometo alílico (A) com os N-R- sulfonilditiocarbimatos de potássio e o cloreto de tetrafenilfosfônio em acetona/água 1:1 (v/v). Os novos compostos sintetizados foram caracterizados por suas temperaturas de fusão, massas exatas (HRMS), espectroscopias vibracional e de ressonância magnética nuclear de 1H e 13C. A atividade antifúngica foi avaliada in vitro frente a A. Solani, pelo método Poison food (ALVES et al., 2009) nas concentrações 30, 60, 120, 240, 360, 480 e 960 micromol/L. O crescimento micelial foi comparado com o controle negativo, obtendo-se percentagens de inibição. A partir das curvas dose-resposta, foram determinados os valores de IC50. Os resultados também foram comparados com um controle positivo, o fungicida mancozeb (9) aplicando-se o teste de Tukey ao nível de significância de 5%. Todo o experimento foi repetido para confirmação dos resultados.
Resultado e discussão
As fórmulas moleculares dos alilditiocarbimatos foram confirmadas por massas
exatas obtidas por espectrometria de massas de alta resolução. Por exemplo, o
pico do íon molecular do composto 8 foi observado no modo negativo em m/z
530,6147 (valor teórico: 530,6158). Nos espectros no infravermelho foram
observadas bandas de estiramento em torno de 1064 cm-1
(CF3), 1708 cm-1 (C=O de éster), 1321 cm-1
(C=N), 1265 e 1162 cm-1 (SO2) e 941 cm-1
(CS2). As bandas de νC=N foram deslocadas para maior número de onda
em relação aos dados dos ditiocarbimatos de potássio originais (1260-1300
cm-1) (TAVARES et al, 2016). As curvas de integração nos
espectros de RMN de 1H confirmaram a proporção 1:1 entre cátion e
ânion. Nos espectros de RMN de 13C, os sinais do cátion apareceram
como dupletos devido ao acoplamento C-P. O quarteto em aproximadamente 128 ppm
(J = 270 Hz) foi atribuído ao sinal do CF3. A presença do flúor
também desdobrou os sinais aromáticos observados em torno de 130,5 ppm (J =
31,5 Hz, C7') e 125,5 ppm (J = 3,8 Hz C6’ e C8'). Os demais sinais observados
também estão em total acordo com as fórmulas propostas. Os alilditiocarbimatos
inibiram o crescimento micelial de A. solani. A Figura 2 exemplifica os
resultados obtidos a 960 micromol/L e mostra que os novos compostos foram mais
ativos que o mancozeb. A partir das curvas dose-resposta obtidas foram
calculados os valores de IC50 para os compostos 1 a 8,
respectivamente iguais a 119; 106; 120; 123; 78; 100; 148 e 219 micromol/L. O
menor valor foi obtido com o composto 5, que apresenta um átomo de bromo como
substituinte no anel aromático do ditiocarbimato.
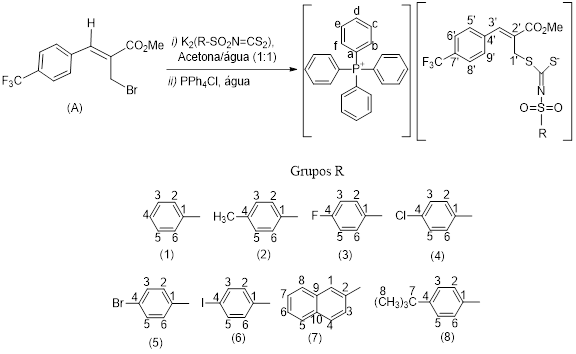
Esquema de síntese dos novos sais de alilditiocarbimatos
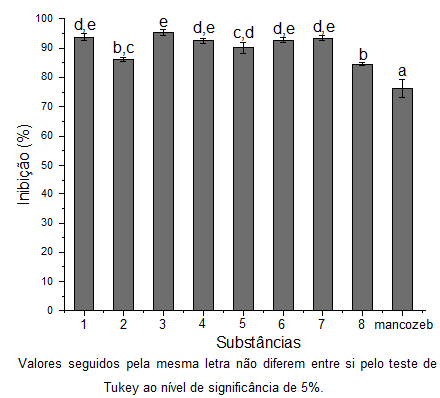
Inibição (%) do crescimento micelial de A. solani causada pelos compostos 1-8 e o mancozeb a 960 micromol/L.
Conclusões
Foram sintetizados oito novos alilditiocarbimatos com a configuração Z. Esses ânions foram isolados na forma de sais de tetrafenilfosfônio e foram caracterizados por espectrometria de massas e espectroscopias no IV e de RMN. Os novos compostos inibiram o crescimento de A. solani, com valores de IC50 entre 78 e 219 micromol/L. Os novos compostos inibem entre 85 e 96% do crescimento fúngico a 960 micromol/L, sendo mais ativos que o fungicida mancozeb. Os compostos sintetizados têm potencial aplicação como agroquímicos.
Agradecimentos
FAPEMIG (APQ-02382-17), CAPES (001), CNPq, UFV
Referências
ALVES, L. C.; RUBINGER, M. M. M., LINDEMANN, R. H.; PERPÉTUO, G. J.; JANCZAK J.; MIRANDA, L. D. L.; ZAMBOLIM, L.; OLIVEIRA, M. R. L. Syntheses, crystal structure, spectroscopic characterization and antifungal activity of new N-R-Sulfonyldithiocarbimate metal complexes. Journal of Inorganic Biochemistry. no 103, 1045-1053, 2009. FERREIRA, M., FERNANDES, L., SÁ, M. M. A Highly Efficient and General Method for the Preparation of (Z)-Allylic Bromides Derived from Morita-Baylis-Hillman Adducts. Journal of the Brazilian Chemical Society, 564-568, 2009. FUJIWARA T., O’HAGAN D., Successful fluorine-containing herbicide agrochemicals. Journal of Fluorine Chemistry, no 167, 16-29, 2014. HEARD, P. J. Main Group Dithiocarbamates Complexes. Progress in Inorganic Chemistry. no 53, 1-561, 2005. HORSFIELD, A.; WICKS, T.; DAVIES, K.; WILSON, D.; PATON, S. Effect of fungicide use strategies on the control of early blight (Alternaria solani) and potato yield. Australasian Plant Pathology, no 39, 368-375, 2010. OLIVEIRA, M. R. L.; de BELLIS, V. M.; Preparation of novel cobalt(III) complexes with dithiocarbimates derived from sulfonamides. Transition Metal Chemistry, no 24, 127-130, 1999. TAVARES, E. C.; RUBINGER, M. M. M.; VENTURINI, E.; OLIVEIRA, M. R. L.; PILÓ-VELOSO, D.; ELLENA, J.; GUILARDI, S.; SOUZA, R. A. C.; ZAMBOLIM, L. Tetraphenylphosphonium allyldithiocarbimates derived from Morita-Baylis-Hillman adducts: Synthesis, characterization, crystal structure and antifungal activity. Journal of Molecular Structure, no 1106, 130-140, 2016.


