COMPLEXO NIMESULIDA-PRATA E ASSOCIAÇÃO POLIMÉRICA COM O QUITOSANA: SÍNTESE E CARACTERIZAÇÃO
ISBN 978-85-85905-25-5
Área
Química Tecnológica
Autores
Mosquera Narvaez, L.E. (UFPA) ; Monteiro de Sousa, P.R. (UFPA) ; Monteiro Chagas, M. (UFPA)
Resumo
O presente trabalho descreve a síntese e caracterização do sistema de absorção usando quitosana (Ch) e o complexo de coordenação Ag (I) Nimesulida (NMS), pelo método de associação polimérica e evaporação. O complexo NMS-Ag foi sintetizado com êxito em uma razão molar de NMS de 8,0x10-3 mol e AgNO3 de 8,8x10-3 mol, sendo posteriormente absorbido em Ch pela mudança de pH. As amostras obtidas foram caracterizadas por espectrometria ultravioleta visível em estado solido (UV-vis), Infravermelho (IV), Termogravimétria (TG) e cinética de liberação da NMS. As micropartículas apresentam um modelo cinético de Baker-Lonsdate (NMS-Ag) e de Korsmeyer (NMS-Ag-Ch)
Palavras chaves
Nimesulida; Quitosana; Complexo metalo-orgânico
Introdução
Dentro da ampla família dos AINEs, encontra-se a Nimesulida (NMS) a qual pertencente ao grupo sulfonanilida, usada no tratamento de inflamações do trato respiratório, tendinite, sinovite e artrite reumatoide (SINGLA; CHAWLA; SINGH, 2000). Apesar dos benefícios terapêuticos, estudos demonstram que a NMS está associada a efeitos adversos pela administração oral, causando distúrbios gastrointestinais relacionados à concentração da droga, além de toxicidade hepática e renal. (DUPONT et al., 1995). Diversas estratégias têm sido pesquisadas para reduzir ou evitar os efeitos colaterais, incluindo: a modificação estrutural, (Su et al., 2010), como a adição de grupos funcionais (PERICHERLA et al., 2007) à formação de complexos metalo- orgânicos (DE PAIVA et al., 2012) e a utilização de carregadores (PIEL et al., 1997). Sendo as duas últimas de especial interesse, pois demostram que a formação de complexos pode conferir caraterísticas duplas ou sinérgicas dependendo das moléculas a qual irá comporta-lo, em conjunto com a mudança de algumas propriedades físico- químicas. Ademais, sabe-se que as micropartículas de biopolimeros (BP) que contém o ativo apresentam a possibilidade de liberação controlada, importante para o suprimento do ativo por um período de tempo mais prolongado (ALVES et al., 2007). Este trabalho teve como objetivo desenvolver uma estratégia baseada na síntese de um complexo (NMS-Ag) e associação polimérica com a quitosana (NMS-Ag-Ch), caracterizando-o físicoquímicamente e testando a liberação controlada da NMS nas amostras em solução de fosfato a pH 7.4. A descoberta de novas alternativas para a liberação de ativos é um grande desafio na pré-formulação e formulação, gerando a necessidade de pesquisar uma variedade de materiais e novos métodos.
Material e métodos
O complexo com a NMS foi obtido por reação de NMS (8,0 x10-3 mol) com a AgNO3 (8,8 x10-3 mol) baixo condições controladas. A síntese foi realizada com agitação constante à temperatura ambiente durante uma hora. O sólido foi recuperado por centrifugação a 5000 rpm e foi secado usando um dessecador à vácuo. Para a associação polimérica foi utilizado 0,8 g de Ch, a qual foi dissolvida em uma solução de ácido acético a 1%, a mistura foi deixada sob agitação constante durante 1 hora. O pH da solução foi ajustado para um valor de cerca de 7 com a adição gota a gota de uma solução de NaOH. Foram recolhidos uma quantidade da solução para dispersar 0,4 g de NMS-Ag, lavando sucessivamente com o restante. A suspensão foi agitada durante 10 min, depois foi filtrada e secada a 40°C. A espectroscopia IV e a espectroscopia UV-Vis em estado sólido foi feita para os complexos NMS-Ag e NMS-Ag-Ch e seus precursores com finalidade de determinar mudanças nas vibrações moleculares em alguns grupos funcionais e identificar as possíveis transições eletrônicas. A análise termogravimétrica foi feita para observar a velocidade de degradação térmica e determinar se existe um efeito térmico protetor do biopolímero sobre o ativo. A cinética de liberação foi feita com uma massa de, aproximadamente, 4mg das amostras, suspensas cada uma em 2 mL de solução de buffer fosfatos com pH 7,4. O tubo eppendorf foi incubado a 37 °C com agitação constante, em intervalos pré-determinados, o tubo foi centrifugado a 12000 rpm durante 5 min, 1mL da camada de sobrenadante foi removida para quantificação no espectrofotômetro UV-Vis a comprimento de onda de 394nm, e foi adicionado um volume igual de solução buffer fosfatos fresco ao tubo eppendorf.
Resultado e discussão
A solubilização da NMS foi realizada em pH alcalino, para que a molécula
esteja desprotonada. A Figura 1A mostra a eletroquímica, representando um
mecanismo acordo à química de coordenação, onde são expostos os sítios de
ligação. O rendimento da síntese foi do 83,2%. A associação polimérica com a
Ch foi feita com mudança de pH. O rendimento do processo foi de 74,2%. A
caracterização dos materiais foi realizada por técnicas analíticas. Os
espectros de UV-Vis (Figura 1B), apresentaram deslocação no comprimento de
onda, mostrando interação entre os locais de coordenação da Ag+ e alguns
grupos funcionais da NMS (DE PAIVA et al., 2012). A Figura 3 e 4 trazem as
análises de Infravermelho obtidos para a NMS e para a NMS-Ag. O alongamento
de (NH) é um pico fino a 3282 cm-1 (Figura 1C). O espectro da NMS-Ag revelou
evidências que comprovam a formação da ligação de coordenação entre o NMS e
Ag+, tais como, o desaparecimento da banda de absorção característica de (N-
H) (Figura 2A). Na análise termogravimétrica dos complexos (Figura 2B),
constata-se que a perda de massa ocorre de 40°C até 206°C, devido ao
conteúdo de água, depois, os produtos de decomposição de 206°C até 393°C.
Após 400°C há uma diminuição da massa até 1000°C. O tempo de degradação foi
mais rápido para a NMS-Ag em comparação com a NMS-Ag-Ch. A liberação da NMS,
dos materiais ocorre por um processo de difusão devido à quebra da NMS-Ag
liberando a NMS, já que a estabilidade do complexo é relativa das condições
trabalhadas. No entanto, a liberação para NMS-Ag-Ch ocorre através dos poros
presentes no material polimérico. Na Figura 2C pode-se observar o tempo e
concentração à qual é liberada a NMS. A cinética de liberação para NMS-Ag
apresenta um modelo de Baker Lonsdate e para NMS-Ag-Ch apresenta um modelo
de Weibull.

A.Ionização da estrutura da nimesulida e ressonância B. Espectro de absorção ultravioleta dos sólidos C. Espectro infravermelho da nimesulida
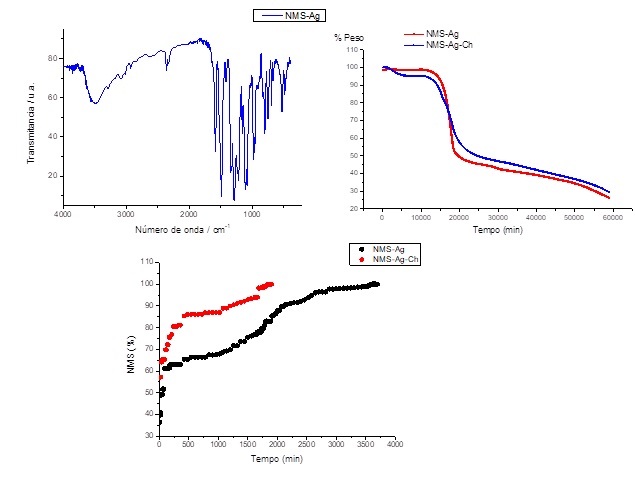
A.Espectro infravermelho do complexo Nimesulide-Prata B. Análise termogravimétrica dos materiais sintetizados C. Curva de liberação das micropartícula
Conclusões
Foi possível sintetizar e caracterizar as micropartículas pelos métodos analíticos sugeridos. Calculando e comparando o coeficiente de determinação (R2) para cada modelo cinético proposto, foram selecionados os que apresentaram melhor resultado. O modelo de Baker Lonsdate foi selecionado para descrever a cinética da NMS-Ag, no qual a estrutura não é homogênea e apresenta fraturas ou capilares que possam contribuir para a liberação, pela possível estrutura de coordenação. Enquanto para NMS-Ag-Ch o modelo de Weibull descreve a liberação do fármaco a partir de uma matriz polimérica (Ch)
Agradecimentos
À UFPA pelas instalações e estrutura de trabalho. À CAPES, CNPq e OEA pela bolsa de fomento à pesquisa. Aos colegas estrangeiros e de laboratório que estiveram auxiliando durante toda a pesquisa
Referências
ALVES, M. P. et al. Human skin penetration and distribution of nimesulide from hydrophilic gels containing nanocarriers. International Journal of Pharmaceutics, v. 341, n. 1–2, p. 215–220, 2007.
DE PAIVA, R. E. F. et al. Synthesis, spectroscopic characterization, DFT studies and antibacterial assays of a novel silver(I) complex with the anti-inflammatory nimesulide. Polyhedron, v. 36, n. 1, p. 112–119, 2012.
DUPONT, L. et al. Nimesulide. Acta Crystallographica Section C Crystal Structure Communications, v. 51, n. 3, p. 507–509, 1995.
FERNÁNDE, J. A. et al. Estudio Cinético De Liberación in Vitro En Un Biomaterial. Rev. Iberoamer Polim, v. 10, n. 2, p. 119–130, 2009.
KEAN, T.; THANOU, M. Biodegradation , biodistribution and toxicity of chitosan ☆. Advanced Drug Delivery Reviews, v. 62, n. 1, p. 3–11, 2010.
NAKAMOTO, K. Infrared and Raman Spectra of Inorganic and Coordination Compounds. [s.l: s.n.].
NUNES, J. H. B. et al. Synthesis, spectroscopic characterization, crystallographic studies and antibacterial assays of new copper(II) complexes with sulfathiazole and nimesulide. Journal of Molecular Structure, v. 1112, p. 14–20, 2016.
PERICHERLA, S. et al. Chemical modifications of nimesulide. Journal of the Brazilian Chemical Society, v. 18, n. 2, p. 384–390, 2007.
PIEL, G. P. X. et al. Study of the Influence of Both Cyclodextrins and L -Lysine on the Aqueous Solubility of Nimesulide ; Isolation and Characterization of Nimesulide − L -Lysine − Cyclodextrin Complexes. v. 86, n. 4, p. 475–480, 1997.
SINGLA, A K.; CHAWLA, M.; SINGH, A. Nimesulide: some pharmaceutical and pharmacological aspects - an update. The Journal of pharmacy and pharmacology, v. 52, p. 467–486, 2000.









