EFEITOS DO NO E SO[sub]2[/sub] PRESENTES EM GASES DE COMBUSTÃO NO PROCESSO DE METANAÇÃO DO CO[sub]2[/sub]
ISBN 978-85-85905-25-5
Área
Química Tecnológica
Autores
de Castro, J.H. (PUCRS) ; de Araujo, G.E. (PUCRS) ; Monteiro, W.F. (UFRGS) ; Ligabue, R.A. (PUCRS) ; Lourega, R.V. (PUCRS)
Resumo
Estudos focados em transformar o CO2 do gás de combustão em metano por meio do processo de metanação têm recebido destaque. No entanto, as reações de metanação são extremamente sensíveis a poluentes (ex.: enxofre, comum no gás de combustão), devido ao uso de catalisadores. A fim de entender melhor a possibilidade de usar o gás de combustão como uma fonte de CO2 para a metanação, este estudo testou o impacto de dois dos principais poluentes, dióxido de enxofre (SO2) e monóxido de nitrogênio (NO), sobre um catalisador comercial de NiO/SiO2. Pioneiro na realização de testes com NO, o estudo demonstra que, embora com diferentes magnitudes, tanto o NO como o SO2 envenenam e diminuem a atividade do catalisador ao longo do tempo.
Palavras chaves
Metanação ; Dióxido de carbono; Poluentes
Introdução
As altas emissões de CO2 causadas pelo homem aumentam a concentração deste gás na atmosfera, transformando o processo natural de efeito estufa em um problema ambiental muito prejudicial ao planeta (OLIVEIRA, 2014). Atualmente, cerca de 85% das fontes de energia no mundo ainda são altamente baseadas em combustíveis fósseis (MAHA ENERGY AB, 2018) e o processo de queima destes combustíveis, resulta em uma mistura de gases contendo CO2, NOx, SOx, H2, N2 e vários outros compostos nocivos à atmosfera, chamados gases de combustão. Atualmente, os gases de combustão são uma das principais fontes de CO2 para a atmosfera, sendo assim, as tecnologias que possam capturar e armazenar/transformar esse componente para mitigar os efeitos ambientais são de suma importância (YEN et al., 2015). Processos visando a conversão química de CO2, são as opções mais comuns para reduzir a emissão deste poluente e, também obter produtos com maior valor de mercado. Entre muitas opções de processos químicos, a metanação é uma alternativa promissora para o uso de CO2, uma vez que produz metano puro que pode ser para fins térmicos ou elétricos e até usado para transporte. A metanação do CO2 necessita de catalisadores eficientes e dentre os mais usados, podemos citar os metais nobres e metais de transição (Ru, Rh, Ir, Pd, Ni, Fe, Co) suportados em óxidos (α-Al2O3, γ-Al2O3, TiO2, SiO2, CeO2) (MARCONI et al., 2019). Devido à cinética de reação, a temperatura de operação é normalmente mantida entre 250 e 550 °C, variando para processos isotérmicos e adiabáticos. Pressão de reação mais alta pode aumentar a conversão de CO2, razão pela qual a maioria dos reatores opera de 10 a 30 bar. No que diz respeito ao projeto do reator e do leito, existe uma grande variedade de opções, das quais a mais aplicada em escala industrial é o reator adiabático de leito fixo. Por fim, a mistura ideal de alimentação de gás seria uma mistura apenas de CO2 e H2, em uma proporção de 1:4, uma vez que qualquer outro componente pode facilmente alterar a eficiência da reação (por exemplo, oxigênio). No entanto, em escala industrial, conseguir uma mistura de CO2 e H2 sem qualquer outro componente pode ser extremamente difícil e caro, especialmente quando as fontes de reagentes originalmente contêm elementos tóxicos para os catalisadores, como enxofre ou cloro (GÖTZ et al., 2016; GÖTZ et al., 2014). A fim de entender melhor a possibilidade de usar gás de combustão como fonte de CO2 para metanação, estudos recentes têm analisado o impacto de contaminantes na mistura de alimentação para a atividade do catalisador. A composição média do gás de combustão em uma usina de carvão é de 65,2% (v/v) de N2, 18,8% (v/v) de H2O, 11,6% (v/v) de CO2, 4% (v/v) de O2, 0,35% (v/v) de SOx e 0,05% (v/v) de NOx (MÜLLER, 2013). Estudos como os realizados por Baraj et al. (2016), Czekaj et al. (2011) mostram que a presença de enxofre na alimentação do gás causa perda considerável da atividade do catalisador, sendo limitada a menos de 10 ppb, a fim de garantir uma vida útil aceitável do catalisador. Com relação aos efeitos do NOx na atividade do catalisador, diferentes estudos testaram a influência do NO2 na reação de metanação e não encontraram efeito negativo. Além disso, a presença de oxigênio no gás de alimentação pode ser considerada poluente, já que o oxigênio consome o hidrogênio que deveria formar metano e produz água, o que diminui a conversão da reação (MÜLLER et al., 2013). Diversos parâmetros, como temperatura, pressão, composição da alimentação e tipo de catalisador podem afetar o desempenho da reação, por isso a metanação direta do CO2 torna-se um desafio tecnológico e científico nos dias de hoje. Dentro deste contexto, este trabalho tem como objetivo descrever o sistema desenvolvido especialmente para a reação de Sabatier em escala laboratorial, bem como realizar reações de metanação investigando a influência dos poluentes mais importantes encontrados nos fluxos de gases de combustão.
Material e métodos
Os gases usados para as reações foram dióxido de carbono (Air Products 5.0), hidrogênio (Air Products 5.0), nitrogênio (Air Products 4.0), mistura de óxido de nitrogênio (Linde 375 ppm NO/N2) e mistura de dióxido de enxofre (Linde 125 ppm SO2/N2). Estas duas misturas (NO e SO2) foram utilizadas alternativamente em cada experimento. O catalisador utilizado foi o óxido de níquel, suportado em óxido de silício com um teor de 60% em peso de NiO (Sigma-Aldrich) e foi distribuído em um leito com sílica gel (relação mássica sílica:catalisador: 15:1). No total, 7 g da mistura catalítica foi introduzida em um tubo de reator de aço inoxidável (aço Swagelok 316/316L) de ½ pol de diâmetro e 300 mm de comprimento. O reator foi instalado em um forno tubular horizontal (Sanchis), que fornece distribuição de temperatura homogênea durante a reação catalítica. O fluxo de gás de entrada é pré-aquecido na seção do reator preenchida com esferas de vidro localizada antes do leito catalítico. Inicialmente, o leito de catalisador foi reduzido sob atmosfera de hidrogênio usando 20 mL/min de hidrogênio puro a uma temperatura constante de 400 °C e pressão ambiente por 4h, tempo suficiente para que somente hidrogênio puro fosse encontrado na corrente de produto, simbolizando o término da etapa de redução do catalisador. No intuito de analisar o impacto dos diferentes compostos encontrados em uma corrente de gás de combustão sobre a reação catalítica, as reações de metanação foram realizadas de acordo com um planejamento experimental. Em todos os cenários a temperatura de reação foi mantida constante a 350 °C e a pressão ambiente. Enquanto os fluxos de poluentes foram manipulados para simular a concentração usual desses elementos na corrente de gases de combustão utilizadas, a vazão total de 100 mL/min e relação molar H2:CO2:N2 de 4:1:5 foram sempre mantidas constante (MÜLLER et al., 2013, 2017). Os experimentos foram divididos em três partes: (1) teste de estabilidade (1540 min) da reação base sem a adição de poluentes, (2) testes de curta duração (120 min) com cinco concentrações diferentes de SO2 (5, 10, 20, 50 e 100 ppm) e (3) testes de curta duração (120 min) com quatro diferentes concentrações de NO (25, 50, 100 e 200 ppm). Os produtos da reação foram amostrados usando um sistema simples composto de uma válvula de três vias e um septo. Seringa e agulha comuns foram usadas para amostrar a mistura de gás do produto através do septo e, em seguida, armazená-lo em frascos de vidro com vácuo projetados para armazenamento de gás (Exetainer - Labco). As amostras foram analisadas em um cromatógrafo a gás (Perkin Elmer - Clarus 580) com coluna Elit Plot Q e um detector de ionização de chama (FID) para detectar a composição do produto e calcular a conversão de CO2 de cada reação. A coleta de amostras de produto foi realizada a cada 30 minutos.
Resultado e discussão
O primeiro conjunto de reações de metanação foi realizado para validar o
sistema e os métodos de reação, de acordo com os resultados da literatura.
Esses primeiros testes mostraram que o sistema é extremamente estável para a
metanação, como é possível ver através dos dados da curva de conversão média
e do desvio padrão apresentados na Figura 1. Com o objetivo de confirmar o
efeito gás inerte (N2) no sistema, essas reações foram feitas com
uma corrente de gás N2:CO2 molar de 5:1, simulando a
concentração média de dióxido de carbono em uma corrente de gás de
combustão. A Figura 1 mostra a alta conversão de CO2 obtida para
o teste de estabilidade da reação com a presença de gás inerte, indicando
que o nitrogênio não tem efeito nesta reação, em escala laboratorial,
conforme relatado anteriormente por MÜLLER et al. (2013). Para essas
reações, a seletividade e o rendimento de metano não foram mostradas na
imagem devido à alta estabilidade desses valores, com uma seletividade
sempre superior a 99,5%. No entanto, em experimentos em escala piloto ou
industrial, a presença de nitrogênio mostrou ser uma complicação. De acordo
com MÜLLER et al. (2017) nestes casos, a presença do gás inerte impede que o
calor gerado do sistema seja suficiente para manter a reação na temperatura
desejada, exigindo uma fonte externa de calor para que se atinja a
temperatura mínima na qual a conversão de dióxido de carbono é adequada.
No intuito de compreender o impacto da presença de SO2 e NO em um
sistema de metanação direta dos gases de combustão, diferentes concentrações
destes elementos no reagente foram testadas em experimentos de curta duração
(Figura 2). Os resultados mostram que para baixas concentrações de
SO2 (Figura 2-a), como 5 ppm, a exposição por um curto tempo de
reação apresentou uma perda pouco significativa de atividade catalítica,
diminuindo a conversão de CO2 em 0,5% (5 ppm) e 0,7% (10 ppm),
para 120 minutos cada. No entanto, o comportamento do catalisador para
concentração de SO2 maiores (20 e 50 ppm) leva a uma alta perda
de conversão no primeiro contato (antes de 30 minutos) de aproximadamente
2,5%. Posteriormente, a taxa de perda diminui e, ao final de 120 minutos,
uma redução total de 3,5% e 4,0% foi notada para 20 e 50 ppm,
respectivamente. Finalmente, para 100 ppm, a conversão diminui
significativamente de 81,0% para 59,5%. Estes resultados mostram que uma
exposição de mais de 10 ppm, mesmo por um curto tempo de reação, pode causar
danos significativos ao catalisador, especialmente para situações próximas a
100 ppm, que são extremamente comuns mesmo após um sistema de lavagem do gás
de exaustão, conforme descrito por CHAPEL et al. (1999).
Juntamente com a redução da conversão de CO2 em função do tempo
de exposição e concentração de poluentes, outros dados importantes obtidos
nos experimentos de curto prazo são a diminuição da seletividade. Uma vez
que o catalisador é exposto a uma quantidade elevada de SO2
(acima de 10 ppm), a seletividade de metano (SCH4) começa a
diminuir e a presença de monóxido de carbono na corrente de produto aumenta.
A quantidade de formação de CO a 350 °C e pressão ambiente deve ser
extremamente baixa, sendo relevante apenas acima de 500 °C. Entretanto, o
efeito do SO2 sobre o catalisador provavelmente alterou sua
estrutura e aumentou a formação de monóxido de carbono, especialmente
através da deposição de carbono sólido sobre a superfície do catalisador.
Devido à alta toxicidade do CO, o limite heurístico adotado
internacionalmente para a presença de monóxido de carbono no gás natural é
de 1% (v/v). Portanto, conforme apresentado por JÜRGENSEN et al. (2015) e
STANGELAND et al. (2017) a presença de enxofre na reação de metanação é um
problema devido à diminuição da eficiência da reação e também à alta
formação de monóxido de carbono.
Com relação ao efeito do NOx, trabalhos anteriores, como MÜLLER
et al. (2013), já haviam reportado que a presença de NO2 não
interferia significativamente na reação, mesmo em concentrações altas como
150 ppm. Todavia, estudos como DELL'ANTONIA et al. (2010) e BATRAKOV (2016)
mostram que, em processos de combustão de combustíveis fósseis, uma parcela
significativa do NOx é formada por monóxido de enxofre, motivo
pelo qual os autores decidiram avaliar pela primeira vez o efeito deste
componente sobre a reação. Distintamente do reportado para o NO2,
a presença de NO (Figura 2-b) tornou o sistema completamente instável,
resultando em um comportamento anômalo da conversão de dióxido de carbono.
Após cada alteração de concentração de NO, ocorre uma diminuição acentuada
na conversão nos primeiros 30 minutos, após os quais a eficiência da reação
aumenta novamente, até um valor próximo do último ponto da concentração de
NO anterior. No entanto, após 60 minutos em contato com a mesma concentração
de NO, um perfil de decaimento linear parece se formar para cada
concentração de NO (linha de decaimento linear no gráfico). Embora a perda
de eficiência da reação tenha sido menos significativa para experimentos com
NO quando comparados ao SO2, os resultados de em tempos curtos
fornecem a ideia de que a presença de NO na reação de metanação tem um
efeito negativo, diminuindo a conversão de CO2 e levando a um
sistema instável. A seletividade do metano também oscilou durante o
experimento, apesar de apresentar valores próximos a 99%, diferentemente da
reação com SO2.
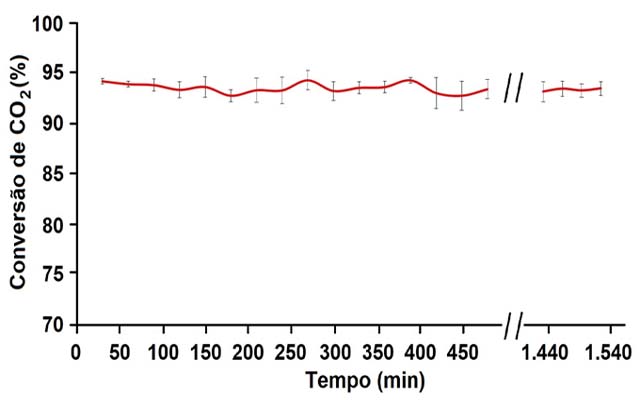
Avaliação da estabilidade do sistema reacional (Pressão - 1,0 atm; Temperatura - 350 °C e Vazão total: 100 mL/min).
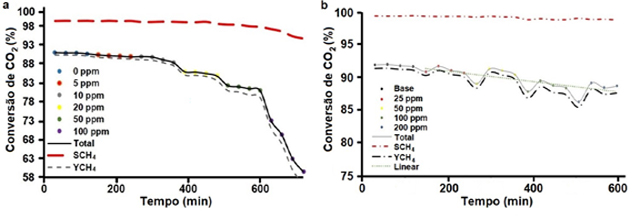
Experimentos com diferentes concentrações de SO[sub]2[/sub] (a) e NO (b). SCH[sub]4[/sub] = seletividade e YCH[sub]4[/sub] = rendimento em metano.
Conclusões
O teste de longa duração (1540 min) realizado sem poluentes comprovou a estabilidade do sistema para a metanação frente aos dados já apresentados anteriormente na literatura. Além disso, a reação de conversão do CO2 foi realizada sob condições usuais de metanação, testando separadamente diferentes concentrações de SO2 e NO, para experimentos de curta duração (120 minutos). Pode-se concluir que enxofre é o poluente mais nocivo, pois apresentou o impacto esperado como elemento de envenenamento ao catalisador, reduzindo a sua atividade mesmo em baixas concentrações (por exemplo, 5 ppm) e por um curto tempo de exposição (120 min). Além disso, o monóxido de nitrogênio, que é um dos principais componentes do NOx, porém, testado pela primeira vez na reação de metanação neste trabalho, mostrou-se prejudicial ao catalisador.
Agradecimentos
Os autores gostariam de agradecer ao Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq) e à Pontifícia Universidade Católica do Rio Grande do Sul (PUCRS).
Referências
BARAJ, E. et al. The Influence of Sulphur Dioxide on The Methanation Activity of a Nickel Based Catalyst. International Journal of Advances in Science, Engineering and Technology, v. 4, n. 1, 2016.
BATRAKOV, P. A. The nitrogen oxide formation studying at natural gas combustion in non-circular profile furnaces of fire-tube boilers. Procedia Engineering, v. 152, p. 144-150, 2016.
CHAPEL, D. G.; MARIZ, C. L.; ERNEST, J. Recovery of CO[sub]2[/sub] from Flue Gases: Commercial Trends. Canadian Society of Chemical Engineers Annual Meeting, 1999.
CZEKAJ, I. et al. Sulphur poisoning of Ni catalysts used in the SNG production from biomass: Computational studies. Catalysis Today, v. 176, n. 1, 2011.
DELL'ANTONIA, Daniele et al. Gaseous emissions from fossil fuels and biomass combustion in small heating appliances. Journal of Agricultural Engineering, v. 41, n. 4, p. 37-46, 2010.
GÖTZ, Manuel et al. Renewable Power-to-Gas: A technological and economic review. Renewable energy, v. 85, p. 1371-1390, 2016.
GÖTZ, Manuel; KOCH, A. M.; GRAF, Frank. State of the art and perspectives of CO[sub]2[/sub] methanation process concepts for power-to-gas applications. In: International Gas Union Research Conference. Fornebu, Norway: International Gas Union, 2014.
JÜRGENSEN, L. et al. Dynamic biogas upgrading based on the Sabatier process: Thermodynamic and dynamic process simulation. Bioresource Technology, v. 178, 2015.
MAHA ENERGY AB. Annual Report 2018. Disponível em: <http://mahaenergy.ca/wp-content/uploads/2019/04/maha-energy-2018-annual-report-english.pdf>. Acessaado em 21 de maio de 2019.
MARCONI, E.; TUTI, S.; LUISETTO, I. Structure-Sensitivity of CO[sub]2[/sub] Methanation over Nanostructured Ni Supported on CeO[sub]2[/sub] Nanorods. Catalysts, v. 9, n. 4, 2019.
MÜLLER, K. et al. Direct Methanation of Flue Gas at a Lignite Power Plant 2 Problem Formulation. v. 2, 2017.
MÜLLER, K. et al. Sabatier based CO[sub]2[/sub]-methanation of flue gas emitted by conventional power plants. Energy Procedia, v. 40, 2013.
OLIVEIRA, F.G. João. Curso: Princípios de Sustentabilidade e Tecnologias Portadoras de Inovação. Desafios da Sustentabilidade: Eco Footprint e Inovação.Veduca. USP, 2014. Disponível em< http://www.veduca.com.br/play/7229>. Acessado em 04 de dezembro 2014.
STANGELAND, K. et al. CO[sub]2[/sub] Methanation: The Effect of Catalysts and Reaction Conditions. Energy Procedia, v. 105, n. 1876, 2017.
YEN, H.W.; HO, S.H.; CHEN, C.Y., CHANG, J.S. CO[sub]2[/sub], NO[sub]x[/sub] and SO[sub]x[/sub] removal from flue gas via microalgae cultivation: a critical review. Biotechnology Journal, 10, pp. 829-839, 2015.









