ESTUDO TEÓRICO DAS PROPRIEDADES VIBRACIONAIS DE MESOIÔNICOS DA CLASSE 1,3-TIAZÓLIO-5-TIOLATO
ISBN 978-85-85905-25-5
Área
Físico-Química
Autores
Lira Anesio, I. (UFPB) ; Paulo Soares Martins, E. (UESPI) ; Filgueiras de Athayde-filho, P. (UFPB) ; Valeriano de Lima, M. (UFPB) ; Santos Vieira de Lima, P. (UFPB) ; da Silva Alves, F. (UFPB) ; Diógenes da Silva Souza, H. (UFPB) ; Silva Soares, F. (UFPB) ; Bruno Rocha, G. (UFPB) ; Pinheiro de Sousa, A. (UFPB)
Resumo
O surgimento de novas doenças trouxe a necessidade de um crescente desenvolvimento de pesquisas que buscam sintetizar novos fármacos. Dentre os compostos têm demonstrado significância no mercado, grande maioria é derivado de heterocíclicos, que são compostos que possibilitam a substituição de um heteroátomo dentro do anel estabilizada por deslocalização de elétrons e cargas. Os compostos obtidos foram caracterizados pelas técnicas espectroscópicas de Infravermelho por Transformada de Fourier, onde as principais bandas foram atribuídas aos estiramentos ν(C⎯S-) e ν(CS, CN, CC) do anel mesoiônico e anel aromático, respectivamente. Os cálculos de DFT foram realizados para avaliar os funcionais B3LYP e M06-2X na predição dos espectros de infravermelho desses compostos.
Palavras chaves
Mesoiônicos; Cálculos DFT; Infravermelho
Introdução
Ao longo dos anos as doenças foram se tornando cada vez mais difíceis de combater pelo surgimento de patologias desconhecidas que foram causadas por fatores como mudanças climáticas, poluição, mudança no estilo de vida, administração de medicamentos de forma inadequada, dentre outros. Os compostos orgânicos representam significativa parcela do mercado farmacêutico, sendo 62% deles heterocíclicos, de onde temos os mais conhecidos como compostos mesoiônicos que, (LIRA et. al, p. 12, 2004) constituem um grupo de betaínas heterocíclicas estabilizadas por deslocalização de elétrons e cargas. Sua síntese tem se mostrado satisfatória pela larga atividade biológica e pela facilidade de utilização para acoplamento e obtenção de novos fármacos, além de participarem em diversas reações através de reações de cicloadição e cicloreversão 1,3- dipolar originando vários outros compostos mesoiônicos de diferentes sistemas e também novos heterocíclicos não mesoiônicos (ATHAYDE-FILHO et al, p. 1565, 2000). Várias atividades biológicas atribuídas aos compostos mesoiônicos e seus derivados foram citados em excelentes revistas a partir de uma série de patentes nacionais, como sendo: antibacteriana, antitumoral, fungicida, antimalárica, antiparasitária, analgésica, antiinflamatória, hipotensiva, hiperglicêmica, diurética, hepatotóxica, inseticida, anticonvulsivante, etc (PEIXOTO et. al, p. 1811, 2016). Este trabalho tem por objetivo a caracterização espectroscópica e estudo teórico das frequências vibracionais de dois mesoiônicos da classe 1,3-tiazólio-5-tiolato.
Material e métodos
Os compostos mesoiônicos, 2-(4-clorofenil)-3-metil-4-(metilfenil)-1,3- tiazólio-5-tiolato (M1) e 2-(4-clorofenil)-3-metil-4- (metóxifenil)-1,3-tiazólio-5-tiolato (M2) foram sintetizados de acordo com o procedimento descrito por (BARBOSA-SILVA et. al, p. 678, 2019). Neste trabalho, as geometrias do estado fundamental e as frequências vibracionais dos compostos foram calculadas a nível teórico DFT/B3LYP (LEE et. al, p. 1988) e M06-2X (ZHAO et. al, p. 215-241, 2007) com conjunto de base cc-pVTZ. As frequências inferiores a 1000 cm-1 foram corrigidas com os fatores de escala: 0,9673 (B3LYP) e 0,9568 (M06-2X) e as superiores, com os fatores de correção: 0,9844 (B3LYP) e 0,9631 (M06-2X) (LAURY et. al, p. 2380–2387, 2012). A escolha dos funcional B3LYP foi baseada na sua boa performance na predição de parâmetros geométricos e vibracionais de compostos orgânicos (SERT et. al, 2014 e SANTOS et. al, 2013). O funcional M06-2X tem mostrado melhor performance na descrição das interações não covalentes e dados termoquímicos de compostos orgânicos (ZHAO et. al, 2011). No entanto, há poucos estudos sobre a qualidade desse funcional no cálculo das frequências vibracionais. Além disso, ressaltamos que não encontramos na literatura trabalhos que avaliem a qualidade dos funcionais DFT na predição das frequências vibracionais de compostos mesoiônicos. Os cálculos foram realizados com o programa Gaussian 09 (FRISCH et. al, 2009) e os dados obtidos foram comparados a dados experimentais, que foram realizados com espectrofotômetro Shimadzu, nas seguintes condições de análise: Região 4000-400 cm-1; Resolução: 4 cm-1; Nº acumulações: 20; Modo: Transmitância; Preparo da amostra dispersa em KBr na proporção 1:100 mg para confecção de pastilhas.
Resultado e discussão
Na Figura 1, é mostrado as geometrias otimizadas dos derivados mesoiônicos a
nível teórico DFT/B3LYP. Com objetivo de fazer uma completa atribuição dos
principais modos vibracionais dos compostos, os seus espectros de
infravermelho foram simulados e comparados com os experimentais. A Tabela 1
exibe as frequências experimentais e calculadas para ambos os derivados
mesoiônicos. Para o composto M1, foram observados três bandas no espectro
experimental, em 1292, 1270 e 1202 cm-1, as quais foram
atribuídas às frequências de estiramento do grupo exocíclico ν(C⎯S-
) e ν(CS, CN, CC) do anel mesoiônico e anel aromático,
respectivamente, calculadas em 1261, 1241, 1188 cm-1(B3LYP) e
1310, 1243, 1198 cm-1(M06-2X). Para o mesoiônico M2, as
frequências de estiramento ν(C⎯S-) e ν(C⎯O⎯C) foram observadas em
1282, 1252 cm-1 e calculadas 1268, 1238 cm-1 (B3LYP) e
1277, 1246 cm-1 (M06-2X). Essas bandas, são de grande utilidade
para interpretação de mudanças estruturais dos derivados mesoiônicos, pois
representam o acoplamento entre os modos vibracionais do anel mesoiônico e
os grupos aromáticos.
Nossos resultados mostram que as frequências vibracionais calculadas com
funcionais B3LYP e M06-2X corroboram os dados experimentais, apresentando
desvios médios absolutos (DMA) entre 24-33 cm-1. Os desvios
observados podem ser principalmente atribuídos ao uso da aproximação
harmônica e efeitos de correlação eletrônica. Ambos os funcionais foram mais
extados na predição das frequências do mesoiônico M1, com DMA de 24
cm-1 contra 33 cm-1 para M2.
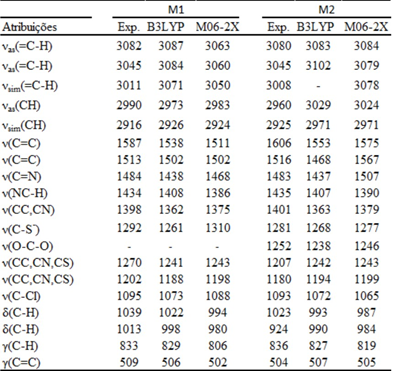
ν =estiramento ,νas=estiramento assimétrico, νsim=estiramento simétrico, δ= deformação angular no plano, γ=deformação angular fora do plano, Exp.=expe
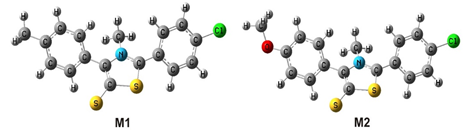
Imagem das estruturas otimizadas dos derivados de mesoiônico M1 e M2
Conclusões
Dois derivados mesoiônicos foram sintetizados e caracterizados por técnicas espectroscópicas. As frequências vibracionais calculadas por ambos os métodos B3LYP e M06-2X/cc-pVTZ apresentam boa concordância com os dados experimentais. Como resultado, uma análise detalhada de alguns modos vibracionais desses compostos foi realizada, contribuindo para uma melhor interpretação dos seus espectros de infravermelho.
Agradecimentos
Os autores agradecem ao CENAPAD-SP pelo suporte computacional, aos órgãos de fomento Capes e CNPq e ao Programa de Pós-Graduação em Química da UFPB.
Referências
ATHAYDE-FILHO, P. F.; SIMAS, A. M.; MILLER, J. Mesoionic compounds: Amphiphilic heterocyclic betaines. Synthesis, Journal of Synthetic Organic Chemistry, n° 11, 1565-1568, 2000.
BARBOSA-SILVA, R.; NOGUEIRA, M. A. M.; SOUZA, H. D. S.; LIRA, B. F.; ATHAYDE-FILHO, P. F.; ARAÚJO, C. B. First Hyperpolarizability of 1,3‐Thiazolium-5-Thiolates Mesoionic Compounds. The Journal of Physical Chemistry, n°123, 677-683, 2019.
CANTILLO, D.; AVALOS, M.; BABIANO, R.; CINTAS P.; JIMÉNEZ, J.L.; LIGHT M.E.; PALACIOS, J.C.; RODRÍGUEZ, V.; RODRIGUEZ, V. Push-pull 1,3-thiazolium-5-thiolates. Formation via concerted and stepwise pathways, and theoretical evaluation of NLO properties. Organic and Biomolecular Chemistry, n°8, 5367–74, 2010.
FRISCH, M.J.; TRUCKS, H.B.; SCHLEGEL, G.E.; ROBB, M.A.; CHEESEMAN, J.R.; SCALMANI, G.; BARONE,V.; MENNUCCI, B.; PETERSSON, G.A.; NAKATSUJI, H.; CARICATO, M.; LI, X.; HRATCHIAN,H.P.; IZMAYLOV,A.F.; BLOINO, J.; ZHENG, G.; SONNENBERG, J. L.; HADA, M.; EHARA, TOYOTA, M.; FUKUDA, K. R.; HASEGAWA, J.; ISHIDA, M.; NAKAJIMA,T.; HONDA, Y.; KITAO,O.; NAKAI, H.; VREVEN, T.; Montgomery Jr., J.A.; PERALTA, J.E.; OGLIARO,F.; BEARPARK, M.; HEYD, J.; BROTHERS, E.; KUDIN, K.N.; STAROVEROV, V.N.; KOBAYASHI, R.; NORMAND, J.; RAGHAVACHARI, K.; RENDELL, A.; BURANT, J.C.; IYENGAR, S.S.; TOMASI, J.; KLENE, M.; KNOX, J.E.; CROSS, J.B.; BAKKEN, V.; ADAMO, C.; JARAMILLO, J.; GOMPERTS, R.; STRATMANN, R.E.; YAZYEV, O.; AUSTIN, A.J.; CAMMI, R.; POMELLI, C.; OCHTERSKI, J.W.; MARTIN, R. L.; MOROKUMA, K.; ZAKRZEWSKI,V.G.; VOTH, G.A.; SALVADOR, P.; DANNENBERG, J.J.; DAPPRICH, S.; DANIELS, A.D.; FARKAS, Ö.; FORESMAN, J.B.; ORTIZ, J.V.; CIOSLOWSKI, J.; FOX, D.J.; COSSI,M.; REGA, N.; MILLAM, N. Gaussian 09, Version c.01, Gaussian, Inc., Wallingford CT, USA, 2009, (n.d.)
LAURY, M.L.; CARLSON, M.J.; WILSON, A.K. Vibrational frequency scale factors for density functional theory and the polarization consistent basis sets. Journal of Computational. Chemistry, n° 33, 2380–2387, 2012.
LEE, W. C.; YANG, R.G. P. Development of the Colle-Salvetti correlation-energy formula into a functional of the electron density. Physical Review B, n° 37, 785–789, 1988.
LIRA, B.F.; Miller, J.; SIMAS, A.M.; ATHAYDE-FILHO, P.F.; Dias, A.F.; SILVA, R.O.; OLIVEIRA, V.C. Synthesis and complete assignments of 1H and 13C NMR spectra of mesoionic 2-(ptrifluoromethylphenyl)-3-methyl-4-(p-tolyl)-1,3-thiazolium-5-thiolate and 2-(p-chlorophenyl)-3-methyl–4-(p-isopropylphenyl)-1,3-thiazolium-5-thiolate. ARKIVOC, n° 6, 12–21, 2004.
PEIXOTO, I. /N.; SOUZA, H. D. S.; LIRA, B. F.; SILVA, D. F.; LIMA, E. O.; BARBOSA-FILHO, J. M.; ATHAYDE-FILHO, P. F. Synthesis and Antifungal Activity Against Candida Strains of Mesoionic System Derived From 1,3-Thyazolium-5-thiolate. Journal of the Brazilian Chemical Society, v.27, n° 10,1807-1813, 2016.
SANTOS, C. B. R.; LOBATO, C. C.; VIEIRA J. B.; BRASIL, D. S. B.; BRITO A. U.; MACÊDO, W. J. C.; CARVALHO, J. C. T.; PINHEIRO, J. C. Evaluation of Quantum Chemical Methods and Basis Sets Applied in the Molecular Modeling of Artemisinin. Wiley interdisciplinary reviews: Computational Molecular Science, v. 2013, 66–79, 2013.
SERT, Y.; BALAKIT, A. A.; ÖZTÜRK, N.; UCUN, F.; EL-HITI, G. A. Spectrochimica Acta Part A : Molecular and Biomolecular Spectroscopy Experimental ( FT-IR , NMR and UV ) and theoretical ( M06-2X and DFT ) investigation , and frequency estimation analyses on ( E ) -3- ( 4-bromo-5-methylthiophen-2-yl ) acrylonitrile. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, v. 131, 502–511, 2014.
ZHAO, Y.; TRUHLAR, D. G. Applications and validations of the Minnesota density functionals, Chemical Physical Letters, v. 502, 1–13, 2011.
ZHAO, Y.; TRUHLAR, D.G. The M06 suite of density functionals for main group thermochemistry, thermochemical kinetics, noncovalent interactions, excited states, and transition elements: two new functionals and systematic testing of four M06-class functionals and 12 other function. Theoretical Chemistry Accounts, n° 120, 215–241, 2007.









