Estudo DFT das propriedades eletrônicas e reatividade de neolignanas 8.O.4’ cetônicas
ISBN 978-85-85905-25-5
Área
Físico-Química
Autores
Carvalho Lobato, C. (UNIFAP/UFPA) ; Luis Belém dos Santos, K. (UNIFAP/UFPA) ; da Silva Freire, A.P. (SEED-AP) ; Patrícia Oliveira de Aguiar, C. (UFPA) ; Rodrigues dos Santos, C.B. (UNIFAP) ; dos Santos Borges, R. (UFPA)
Resumo
As neolignanas são um grande grupo de fenóis de ocorrência natural, resultantes acoplamento oxidativo de propenilfenóis e alilfenóis, e apresentam uma variedade de atividades biológicas, tais como antifúngica, leishmanicida, antioxidante e esquistossomicida. O objetivo deste trabalho foi realizar um estudo teórico, por DFT, das propriedades eletrônicas e reatividade de 7 neolignanas 8.O.4’ cetônicas. Os valores de HOMO, LUMO, potencial de ionização e contribuição de spin mostraram que a hidroxilação na posição orto do anel A da neolignana aumentou sua reatividade, melhorando a capacidade desta estrutura em doar elétrons.
Palavras chaves
Estudo DFT; Neolignanas; Reatividade Química
Introdução
As neolignanas são um grande grupo de fenóis de ocorrência natural que são amplamente difundidos no reino vegetal e derivam da via biossintética do ácido chiquímico. O termo neolignana designa derivados do acoplamento oxidativo de propenilfenóis e alilfenóis. Estes compostos mostram estruturas diméricas formadas por uma ligação β, β’ entre duas unidades de fenilpropano com um grau diferente de oxidação na cadeia lateral e um padrão de substituição diferente nas porções aromáticas (BERNINI et al., 2009). Semelhante às funções ecológicas de vários outros metabólitos secundários, as neolignanas representam um meio de proteção contra herbívoros e microorganismos para as plantas que os sintetizam. As neolignanas apresentam uma variedade de atividades biológicas, como antifúngica, leishmanicida, antioxidante e esquistossomicida (BARATA et al., 2000; SOUZA; NAKAMURA; CORRÊA, 2012). Pesquisadores, em especial os brasileiros, motivados pelas inúmeras potencialidades terapêuticas que as neolignanas apresentam, têm realizado uma série de sínteses de derivados e análogos de neolignanas naturais potencialmente ativas (BARATA et al., 2000; KÓNYA; VARGA; ANTUS, 2001; PINHEIRO et al., 2004). O objetivo deste trabalho foi realizar um estudo DFT de 7 neolignanas 8.O.4’ cetônicas e avaliar o papel das diferentes substituições nas posições orto, meta e para, do anel A, pelos grupos hidroxila e metila, na variação das energias dos orbitais de fronteira HOMO e LUMO, potencial de ionização e distribuição de spin.
Material e métodos
Neste estudo foram selecionadas 7 neolignanas 8.O.4” cetônicas (Tabela 1), sendo uma simples, e seis com substituições nas posições orto, meta e para do anel A pelos grupos elétron-doadores hidroxila e metila. Todos os cálculos computacionais foram realizados utilizando o conjunto de programas Gaussian 09 (FRISCH et al., 2016) e GaussView 6.1 (DENNINGTON; KEITH; MILLAM, 2016). O funcional híbrido B3LYP (BECKE, 1993) e o conjunto de base 6-31g(d,p) foram usados para otimizar a geometria de cada composto neutro e os radicais catiônicos relacionados. A partir dos cálculos foram obtidas algumas propriedades como: energia dos orbitais de fronteira HOMO e LUMO, GAP de energia (HOMO-LUMO). O potencial de ionização (PI) foi calculado a partir da diferença de energia entre uma molécula neutra e o radical catiônico (PI=Eneutro-Ecátion). Também realizou-se análise de distribuição de spin, que é outra propriedade importante para avaliação da nucleofilicidade e eletrofilicidade, a densidade de spin é gerada após a abstração do elétron formando um intermediário radicalar do tipo cátion, de modo que o elétron desemparelhado se distribui sobre toda molécula (GILLON et al., 1999).
Resultado e discussão
Os orbitais de fronteira HOMO e LUMO são muito úteis para predizer a posição
mais reativas em sistemas de elétrons-pi. O HOMO representa a capacidade de
doar elétron, enquanto o LUMO representa a capacidade de aceitar um elétron.
Assim, a energia do HOMO está diretamente relacionada ao potencial de
ionização, enquanto a energia LUMO está diretamente relacionada à afinidade
eletrônica, e o GAP está relacionado à estabilidade química. Uma molécula
com um menor GAP é mais polarizável e geralmente associada a alta
reatividade (GUNASEKARAN et al., 2008; KURT et al., 2011). Os valores HOMO,
LUMO e GAP são mostrados na Tabela 1. Os resultados mostraram que o composto
2 apresentou maior variação de HOMO, quando comparado com a neolignana mais
simples (composto 1), o composto 2 apresentou também, baixo valor de GAP. O
PI representa a facilidade de doação de elétrons. Portanto, moléculas com um
PI mais baixo são mais reativas. Os valores de PI são mostrados na Tabela 1.
O composto 2 apresentou o menor valor teórico para o potencial de ionização.
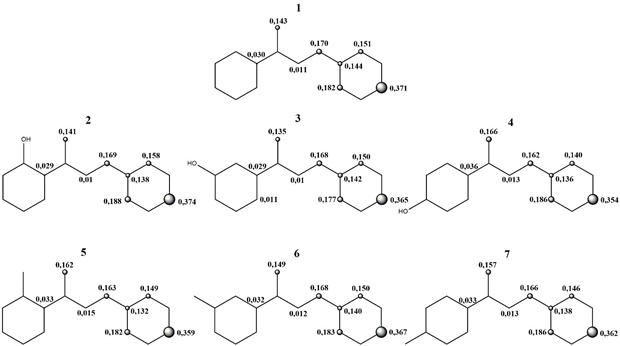
A Figura 1 mostra a distribuição das densidades de spin dos radicais das
neolignanas. As distribuições de densidade de spin para os cátions radicais
mostraram aumento das contribuições no anel B quando adicionados os
substituintes no anel A, sendo que o composto 2 apresentou maior aumento na
contribuição no anel B com valor global de 0,858. Nota-se então, que a
hidroxilação na posição orto do anel A provocou maior variação no valor de
HOMO e mostrou menor potencial de ionização, demostrando que este composto
apresenta maior facilidade em doar elétrons, sendo mais reativo. De acordo
com o padrão de estabilização pelo efeito eletrônico em todos os compostos,
o anel B pode ser substituído nas posições orto ou para em futuros
planejamentos.

Conclusões
Este estudo mostrou que entre as várias substituições no anel A de uma neolignana, a hidroxilação na posição orto provocou maior variação nos valores de HOMO e diminuição no potencial de ionização e, adicionados aos resultados de contribuição de densidade de spin demostrou-se, teoricamente, que esta estrutura possui maior facilidade em doar elétrons quando comparada com os demais compostos avaliados, possuindo maior reatividade.
Agradecimentos
Referências
BARATA, L. E. S. et al. Anti-leishmanial activity of neolignans from Virola species and synthetic analogues. Phytochemistry, v. 55, n. 6, p. 589-595, 2000.
BECKE, A. D. A new mixing of Hartree–Fock and local density‐functional theories. The Journal of Chemical Physics, v. 98, n. 2, p. 1372-1377, 1993.
BERNINI, R. et al. A novel and efficient synthesis of highly oxidized lignans by a methyltrioxorhenium/hydrogen peroxide catalytic system. Studies on their apoptogenic and antioxidant activity. Bioorganic & Medicinal Chemistry, v. 17, n. 15, p. 5676-5682, 2009.
DENNINGTON, R.; KEITH, T. A.; MILLAM, J. M. GaussView 6.1. Shawnee Mission, Kansas: Semichem Inc. 2016.
FRISCH, M. J. et al. Gaussian 09. Wallingford CT: Gaussian, Inc. 2016.
GILLON, B. et al. Spin density in a triazole-nitronyl-nitroxide radical presenting linear ferromagnetic interactions: role of hydrogen bonding. Chemical Physics, v. 250, n. 1, p. 23-34, 1999.
GUNASEKARAN, S. et al. Experimental and theoretical investigations of spectroscopic properties of N-acetyl-5-methoxytryptamine. Canadian Journal of Analytical Sciences and Spectroscopy, v. 53, 2008.
KÓNYA, K.; VARGA, Z.; ANTUS, S. Antioxidant properties of 8.O.4′-neolignans. Phytomedicine, v. 8, n. 6, p. 454-459, 2001.
KURT, M. et al. Molecular structure, vibrational, UV and NBO analysis of 4-chloro-7-nitrobenzofurazan by DFT calculations. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, v. 79, n. 5, p. 1162-1170, 2011.
PINHEIRO, A. A. C. et al. A QSAR study of 8.O.4′-neolignans with antifungal activity. Journal of Molecular Structure: THEOCHEM, v. 672, n. 1, p. 215-219, 2004.
SOUZA, V. A.; NAKAMURA, C. V.; CORRÊA, A. G. Atividade Antichagásica de Lignanas e Neolignanas. Revista Virtual de Química, v. 4, n. 3, p. 197-207, 2012.









