Síntese, Caracterização Espectroscópica, Teste de Toxicidade e Campo Aberto no Modelo do Zebrafish e Atividade Biológica na Inibição da Enzima Acetilcolinesterase do Complexo Inorgânico [Zn(AT)2](CH3COO)2, onde AT= Ácido Tânico.
ISBN 978-85-85905-25-5
Área
Iniciação Científica
Autores
Almeida, B.N. (UNIVERSIDADE ESTADUAL DO CEARÁ) ; Silva, F.C.O. (UNIVERSIDADE ESTADUAL DO CEARÁ) ; Silva, A.C.S. (UNIVERSIDADE ESTADUAL DO CEARÁ) ; Oliveira, M.D.L. (UNIVERSIDADE ESTADUAL DO CEARÁ) ; Silva, W.M.B. (UNIVERSIDADE ESTADUAL DO CEARÁ) ; Alves, D.R. (UNIVERSIDADE ESTADUAL DO CEARÁ) ; Menezes, J.E.S.A. (UNIVERSIDADE ESTADUAL DO CEARÁ) ; Magalhães, F.E.A. (UNIVERSIDADE ESTADUAL DO CEARÁ) ; Morais, S.M. (UNIVERSIDADE ESTADUAL DO CEARÁ) ; Pinheiro, S.O. (UNIVERSIDADE ESTADUAL DO CEARÁ)
Resumo
O Ácido Tânico (AT) é uma substância fenólica que apresenta inúmeras atividades farmacológicas. O zinco (Zn) é um dos íons mais importante e essenciais encontrado em todas formas de vida, pois o mesmo está envolvido em atividades regulatória dentro do corpo que inclui o crescimento e desenvolvimento no corpo, cérebro e expressões génicas. O complexo formado [Zn(AT)2](CH3COO)2 foi sintetizado utilizando uma proporção de 2:1 do ligante e sal Zn(CH3COO)2, respectivamente. A caracterização foi realizada por espectroscopia eletrônica na região do ultravioleta e visível (UV-Vis) e na região do infravermelho (IV). Realizou-se teste de toxidade e de campo aberto utilizado no modelo do Zebrafish e testes na inibição da enzina Acetilcolinesterase.
Palavras chaves
ÁCIDO TÂNICO.; COMPLEXOS INORGÂNICOS. ; ACETILCOLINESTERASE
Introdução
O íon zinco é muito utilizado em parâmetro para o diagnóstico de doenças neurodegenerativas como Alzheimer e Parkinson (LEAL et al., 2012). Estudos apontam que o zinco na sua forma de íon Zn2+ é empregado na adsorção de colóides minerais suspensos e complexação com os materiais orgânicos (SOUZA., 2003). O ácido tânico (AT) é um composto orgânico polifenólico encontrados em plantas, sendo esse integrante da classe dos taninos que são substâncias solúveis em água e solventes orgânicos polares que apresenta a capacidade de precipitar proteínas (HARTISH; KOLODZIEJ apud PANSERA et al., 2003; CUNHA, BIACHINI, SERRANO, 2002), utilizado como fonte de matéria prima de várias indústrias, como as de alimentos, bebidas e fármacos, sua aplicação mais antiga são em curtimento de couro, produção de borracha e tratamento de água em barragens (PANSERA et al., 2003). As classes dos taninos são classificadas como metabólicos secundários na qual são encontrados principalmente em folhas, galhos e em menores quantidades nas frutas, devido os taninos possuírem atividade antioxidante, que protege as plantas da radiação UV do sol (TIRELLI et al., 2010; ORLANDO, VALE, 2014). Possui uma vasta aplicação como ligante e capacidade de formar polímeros devido às ligações de hidrogênio, interações com cátion metálicos e proteínas por coordenação, tal fato decorre devido a múltiplos grupos de hidroxilas presentes na estrutura molecular do ácido tânico, além de atuar como base de Lewis (NABEL et al., 2013). O AT é capaz de produzir distintos efeitos farmacológico tanto em in vitro que possui atividade anticoagulante, como em in vivo que não modifica a fragilidade das hemácias ou na homeostase sanguínea (MEDEIROS et al., 1988).
Material e métodos
Para a elaboração deste trabalho, foram utilizados na síntese do complexo, o sal acetato de zinco (II) diidratado, Zn(CH3COO)2.2H2O (MERCK) e o ligante Ácido Tânico (VETEC), os solventes utilizados foram dimetilsulfóxido (DMSO), trietilamina (MERCK) e água destilada. Na preparação do complexo [Zn(AT)2] (CH3COO)2 foi dissolvido 0,03g de acetato de zinco (II) em 10mL de água e adicionado a uma solução de ácido tânico 0,464g dissolvido em água sob agitação por 15 minutos, após o tempo adicionou-se 3 gotas de trietilamina onde ficou sobre agitação por 3 horas. Ao fim da reação ocorreu a formação do sal complexo. O complexo [Zn(AT)2](CH3COO)2 foi filtrado, em seguida o precipitado foi coletado e estocado em dessecador. Foi realizado teste de solubilidade do composto em solventes diferentes (água destilada, metanol, diclorometano, etanol, éter e dimetilsulfóxido). Para a caracterização do complexo foi utilizado o espectrofotômetro (SHIMADZU UV-1800), em solução de concentração de 1x10-3 mol/L em uma faixa de 200 a 800 nm de comprimento de onda. A espectroscopia na região do infravermelho (FT-IR) foram obtidos utilizando um espectrofotômetro de modelo (NICOLET iS5) da Thermo Scientific. As amostras foram preparadas na forma de partilhas de KBr na proporção de 1:20 (m/m) (amostra: KBr) e os espectros registrados no intervalo de 4000 a 400 cm- 1, empregando-se 32 scans e resolução de 4cm-1. Foram utilizados zebrasfish (Danio rerio) adulto (ZFa), selvagens, ambos os sexos com idade de 60-90 dias, tamanhos de 3.5 ± 0.5 cm e peso 0.4 ± 0.1g, obtidos da Agroquímica: Comércio de Produtos Veterinários LTDA, um fornecedor de fortaleza (Ceará, Brasil). Todos os procedimentos experimentais foram aprovados pelo Comitê de Ética do Uso de Animais da Universidade Estadual do Ceará (CEUA-UECE), sob protocolo nº 3344801/2017. Os testes com zebrafish foram realizados baseando-se em metodologias propostas por Magalhães et al. (2017). No dia dos experimentos, os peixes foram selecionados randomicamente, transferidos para uma esponja úmida, tratados com as amostras teste ou controle (veículo; DMSO 3%), via oral (v.o.) (COLLYMORE, RASMUSSEN e TOLWANI, 2013), com pipeta automática variável de 20 µL com ponteiras estéreis. No Teste de Campo Aberto (n=6/grupo), os animais foram acondicionados individualmente em copos de vidro (250 mL) contendo 150 mL de água do aquário para repouso. Para a avaliação da toxicidade aguda 96 h, os animais (n=8/grupo) foram acondicionados individualmente em aquários de plástico (1,5 L) contendo 1 L de água do aquário para repouso. A atividade inibitória da enzima acetilcolinesterase (AChE) foi aferida em placas de 96 poços de fungo chato utilizando leitor Elisa BIOTEK, modelo ELX 800, software “Gen5 V2.04.11”, baseando-se na metodologia descrita por ELLMAN et al. (1961), com modificações.
Resultado e discussão
Durante os 15 minutos de síntese do composto [Zn(AT)2](CH3COO)2, a solução
apresentou uma coloração alaranjada devido à presença do ligante ácido tânico,
contudo, após a adição de trietilamina o composto passou a ter uma coloração
branca leitosa. O complexo formado não foi solúvel nos solventes como a água
destilada, metanol, diclorometano, etanol e éter, entretanto, completamente
solúvel em dimetilsufóxido (DMSO). Após o isolamento, o composto foi submetido
à análise de espectroscopia na região UV-Vis no solvente DMSO. A mudança de
cor durante a síntese do complexo demonstra que a coordenação se processou
após a adição da base trietilamina. De acordo com os dados da espectroscopia
eletrônica na região do UV-Vis, Tabela 01, observaram-se duas bandas no
espectro do ligante ácido tânico livre de coordenação, em 212 e 276 nm. No sal
Zn(CH3COO)2 observou-se apenas duas bandas 284 e 345 nm. Para o complexo as
bandas de absorção foram observadas nos comprimentos 245 e 284 nm o que
demostra uma alteração significativa em comparação com as amostras isoladas.
Os dados obtidos pela espectroscopia na região do infravermelho, Figura 01 e
Tabela 02, mostraram um deslocamento para uma região maior correspondente ao
O-H, de 3396 cm-1 observado no ligante livre de coordenação para 3403 cm-1 no
complexo, sugerindo a coordenação pelos grupamentos fenólicos, de forma
bidentanda. A coordenação também influenciou o deslocamento do C=O (carbonila)
de 1710 cm-1 no ligante AT para 1712 cm-1 no complexo, esses dados demostram a
coordenação do ligante ao centro metálico. Na região entre 1034 a 654 cm-1 do
ácido tânico livre de coordenação, observa-se os estiramentos das ligações C-
Csp2 dos anéis aromáticos, na mesma região para o complexo houve
deslocamentos para 1037 e 760 cm-1. Tomando-se por base estes resultados
sugeriu-se a estrutura do complexo conforme a Figura 02. Os testes com o
zebrafish de segurança clinica indicaram que o complexo sugere ter caráter
sedativo, e não tóxico, conforme a Figura 03 e Tabela 03. O teste de inibição
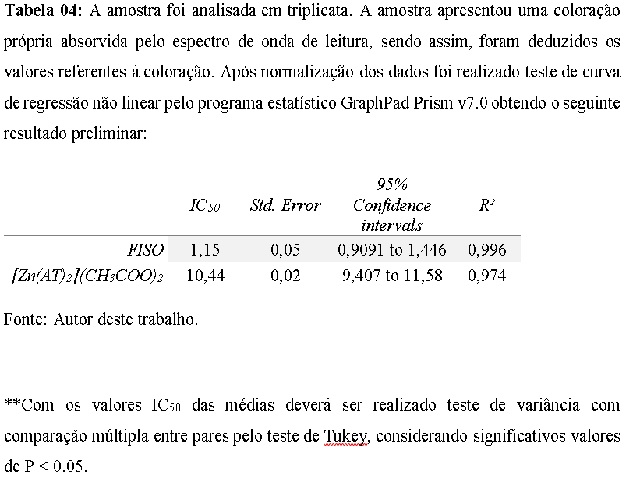
da enzima acetilcolinesterase demostra uma eficácia significativa, onde o
resultado para redução de 50% do teor da enzima foi necessário 10,44 µg/mL do
complexo, Tabela 04.

Tabela 01 - Espectro eletrônico na região UV-Vis no ligante AT, o sal Zn(CH3COO)2.2H2O e do complexo [Zn(AT)2](CH3COO)2 no solvente DMSO.

Tabel 2 Dados de Espectroscopia na Região do Infravermelho no ligante AT, do sal Zn(CH3COO)2.2H2O e do complexo [Zn(AT)2](CH3COO)2 em pastilha de KBr.
ACETILCOLINESTERASE.

Resultado do teste de toxicidade aguda de [Zn(AT)2](CH3COO)2 frente ao Zebrafish Adulto.
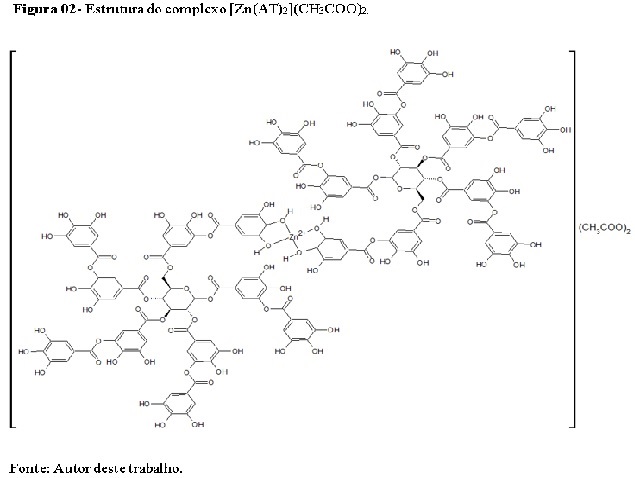
Estrutura do complexo [Zn(AT)2](CH3COO)2.
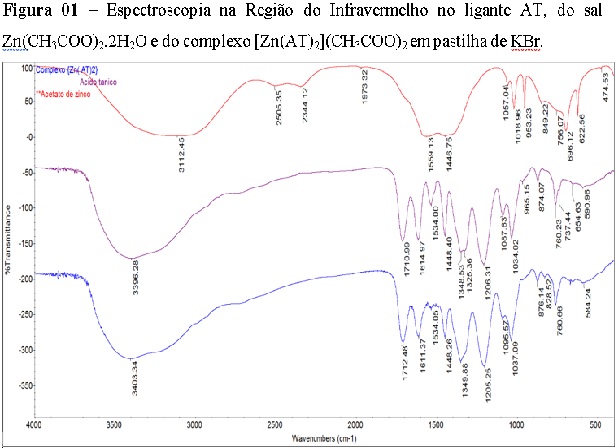
No ligante AT, do sal Zn(CH3COO)2.2H20 e do complexo [Zn(AT)2](CH3COO)2 em partilha de KBr.
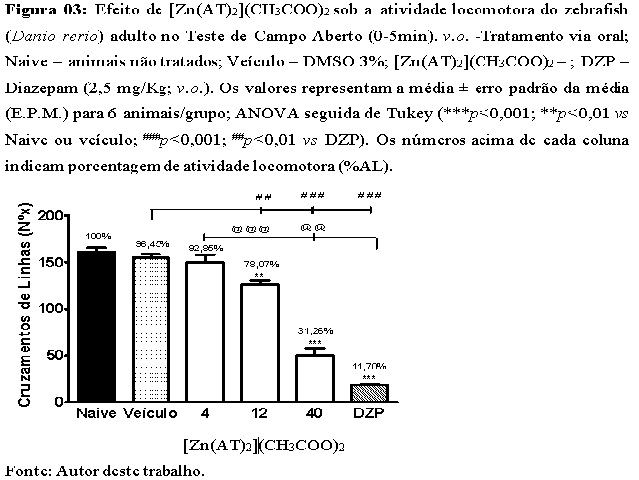
Efeito de [Zn(AT)2](CH3COO)2 sob atividade locomotora do zebrafish (Danio rerio) adulto no teste de campo aberto (0-5 min). v.o- Tratamento via Oral.
Conclusões
De acordo com os resultados descritos nesse trabalho, houve coordenação do ácido tânico ao centro metálico de Zn2+, sendo coordenado por grupamentos fenólicos de forma bidentada. No âmbito de segurança clínica os testes com o zebrafish indicam que o complexo não apresentou toxicidade e nos experimentos de campo aberto, observou-se um caráter sedativo. O teste com a inibição da enzima acetilcolinesterase demonstrou uma boa eficiência na capacidade do complexo de inibir a enzima em 50% de sua atividade.
Agradecimentos
À Universidade Estadual do Ceará (UECE), ao Laboratório de Química Inorgânica (LQUIN), ao Laboratório de Produtos Naturas (LQPN), pelo incentivo à pesquisa.
Referências
COLLYMORE, C., RASMUSSEN, S., TOLWANI, R.J. 2013. Gavaging adult zebrafish. J Vis Exp. 78(e50691), 1-5. CONCEA. Conselho Nacional de Controle de Experimentação Animal. Resolução Normativa Nº 37, de 15 de fevereiro de 2018. Diretrizes da Prática de Eutanásia. Disponível em www.mctic.gov.br/.../concea/...normativas/RN-37-Eutanasia-secao-1-22_02_18.pdf . Acesso em 22/4/18.
CUNHA, S, M, B.; BIANCHINI, JR, I.; SERRANO, L, E, F.; Aerobic and Anaerobic Degradation of Tannic Acid on Water. Braz. J, Biol, 62 (4A): p.585-590, 2002.
ELLMAN, G, L.; COURTNEY, K, D.; ANDRES, V, JR.; FEATHERSTONE, R, M.; A NEW AND RAPID COLORI METRIC DETERMINATION OF ACETYLCHOLINESTERASE ACTIVITY. Biochemical Pharmacology, 1961, v. 7, p. 88-95. Pergamon Ltd., Printed in Great Britain.
LEAL, M. F. C.; CATARINO, R. I. L.; PIMENTA, A. M. Especialização de cobre e zinco em urina- importância dos metais em doenças neurodegenerativas. Quim. Nova, v. 35, n. 10, 1985-1990, 2012.
MAGALHÃES, F.E.A., DE SOUSA, C.A.P.B., SANTOS, S.A.A.R., MENEZES, R.B., BATISTA, F.L.A., ABREU, A.O., DE OLIVEIRA, M.V., MOURA, L.F.W.G., RAPOSO, R.S., CAMPOS, A.R., 2017. Adult zebrafish: an alternative behavioral model of formalin-induced nociception. Zebrafish 4 (5), 422-429.
MEDEIROS, Y, S.; MORATO, G, S.; MOTATO, E, F.; VALLE, R, M, R.; LIMA, T, C, M.; RAE, G, A.; CALIXTO, J, B.; Ações Farmacológicas do Ácido Tânico. III. Análises em Outros Modelos Experimentais. P.157-170, 1988.
NABEL, A, N.; AHMED, F, E, F.; ISLAM, A, M.; MOHAMAD, F, Z.; MANAL, M, K.; Synthesis and inhibitory activity of schiff base surfactants derived from tannic acid and their cobalt (II), manganese (II) and iron (III) complexes against Bacteria and fungi. J Surfact Deterg 16:767–777. 24 january, 2013.
ORLANDO, J, F, F.; VALE, V, V.; Análise Fitoquímica e Atividade Fotoprotetora de Extrato Etanólico de Euphorbia Tirucalli Linneau (Euphosbiaceae). Ver. Bras. P.I. Med, v.17, n.4, p. 730- 736, 2015.
PANSERA, M, R.; SANTOS, A, C, A.; PAESE, K.; WASU, R.; ROSSATO, M.; ROTA, L, D.; PAULETTI, G, F.; SERAFINI, L, A.; Análise de Taninos Totais em Plantas Aromáticas e Medicinais Cultivadas no Rio Grande do Sul. Rev. Bras. Farmacogn, v.13, n.1, jan-jun, 2003.
SOUZA, E. S.; Método de escoamento superficial no solo: Quantificação e biodisponibilidade de metais no efluente, percolado, solo e planta. Campinas, SP, 2003.
TIRELLI, A, A.; ALVES, D, S.; CARVALHO, G, A.; SÂMIA, R, R.; BRUM, S, S.; GUERREIRO, M, C. EFEITO DE FRAÇÕES TÂNICAS SOBRE PARÂMETROS BIOLÓGICOS E NUTRICIONAIS DE Spodoptera frugiperda (LEPIDOPTERA: NOCTUIDAE). Ciênc. agrotec., Lavras, v. 34, n. 6, p. 1417-1424, nov./dez., 2010.









