SÍNTESE E CARACTERIZAÇÃO DE TITANATOS DE BÁRIO DOPADOS COM ÍONS LANTANÍDEOS
ISBN 978-85-85905-25-5
Área
Iniciação Científica
Autores
Silva, R.R. (UFT) ; Lemos, F.C.D. (UFT) ; Junior, S.A. (UFPE) ; Coelho, D.M.A. (UFPE)
Resumo
O objetivo deste trabalho foi sintetizar e caracterizar pós amorfos de titanato de bário, BaTiO3 (BT), por meio do método Pechini. Os pós de BT, puro e dopados com íons Samário (BTSm) e Európio (BTEu) a 1, 3 e 5%, foram caracterizados utilizando-se análise termogravimétrica (TG), difração de raios X (DRX), micrografia eletrônica de varredura (MEV) e espectroscopia de emissão. A análise de DRX revelou a presença de BaCO3, que por lixiviação ácida foi eliminado e a estrutura perovskita desejada foi obtida. Também se pôde observar, a partir das micrografias de MEV, que os pós apresentaram aspectos morfológicos similares e, pelos resultados de emissão, que esses materiais apresentam potencial aplicação em dispositivos fotônicos.
Palavras chaves
Titanato de bário; Perovskita; Método Pechini
Introdução
O BaTiO3 pertence à família da perovskita, do tipo ABO3 (SPORN, D. et al, 1995), sua estrutura tem ponto de Curie baixo, que atribui a este material uma constante dielétrica elevada a temperatura ambiente, permitindo seu uso em capacitores de armazenamento de alta capacidade (KISHI, H. et al, 2003). O desenvolvimento de compostos amorfos com dimensões nanométricas e com propriedades ópticas ativas, proporciona a fabricação de dispositivos eletroeletrônicos sofisticados, com desempenhos aprimorados e de dimensões extremamente pequenas (Leite, E.R. et al, 2002). Propriedades como polarização espontânea, alto valor de constante dielétrica e fotoluminescência são obtidas a partir da preparação das soluções, na estabilidade de fases, na sinterização do pó ou filme fino, bem como na própria estabilidade durante o crescimento das partículas (LEITE, E.R. et al, 2001). Uma das propriedades apresentadas por esses compostos amorfos, como o titanato de bário e de chumbo, é a fotoluminescência. Assim, esses materiais podem ser utilizados como dispositivos que funcionam à temperatura ambiente (MAMBRINI, G. P. et al, 2008). O estudo da produção e caracterização de materiais nanoestruturados tem sido um dos temas mais atraentes da pesquisa fundamental e tecnológica dos últimos anos devido as possibilidades de melhoria das diversas propriedades que esses materiais podem ter em comparação aos materiais obtidos por processos convencionais. Com o avanço tecnológico, novos métodos de preparação de materiais têm sido desenvolvidos e propriedades físicas de partículas nanocristalinas quando comparadas com as microcristalinas recebem mais e mais atenção (WEIRICH, TH. E. et. al., 2000). Técnicas modernas para a produção de materiais permitem controlar tanto a estequiometria como o tamanho dos cristalitos, em temperaturas relativamente baixas, simplicidade nos processos, os quais proporcionam melhores aplicações tecnológicas. Entretanto, métodos apropriados para a produção destes materiais são necessários de forma que venham a melhorar as rotas de síntese e possibilite o melhor conhecimento dos processos químicos e físicos que ocorrem em escala nanométrica. (MCKEE, R. A et. al., 2001; SIRENKO, A. A. et. al., 2000). Na estrutura perovskita do BT cada íon de Ba2+ e de Ti4+ está envolvido por 12 e seis íons oxigênios respectivamente (SADHANA, K. et. al., 2008). Os íons Ba2+ estão localizados nos vértices da célula unitária tanto na simetria tetragonal quanto na cubica e contribuem com 1/8 de seu volume. Os íos oxigênios são localizados no centro da face e contribuem para a formação dessas células com ½ de seu volume. Desta maneira a célula unitária do BT possui um íon bário, 3 oxigênios e um de titânio. Os íons Ti4+ podem ocupar duas posições acima ou abaixo do alinhamento com centro da célula unitária, não coplanares com os átomos de oxigênio e em nenhuma das posições está no centro da célula unitária (CALLISTER JR., W. D. 2002). A inserção de íons dopantes em uma rede cristalina poderá provocar dois tipos de defeitos pontuais, segundo o raio iônico do dopante: intersticial ou substitucional. Quando a dopagem é substitucional os íons podem ser do tipo isovalente, doador ou receptor (também chamado aceitador). O íon a ser substituído pelo dopante é comumente chamado íon hospedeiro (CALLISTER JR., W. D. 2002). Substituições isovalentes são feitas com íons que possuam tamanhos e carga similar ao Ba2+ e Ti4+ (SCHNEIDER JR., S. J, 1991). Quando o BT é dopado com íons receptores ou doadores, ele pode se comportar como um semicondutor tipo p ou n, que são portadores de carga positiva e negativa, respectivamente (DANIELS, J. et. al., 1978). Atualmente há um grande interesse em estudar as propriedades ópticas do BT, que pode atuar como um atraente hospedeiro na dopagem com íons de lantanídeos que têm aplicações em dispositivos de emissão de luz, displays de emissão de campo, lasers, etc. Neste aspecto muito trabalhos são relatados na literatura (MELÉNDEZA, J. J. et al et al, 2015. Neste trabalho apresentamos a produção e caracterização de pós cerâmicos puros e dopados, a partir de um método químico com a finalidade de entender a influência dos dopantes na formação de fase e propriedades desses materiais para possíveis aplicações.
Material e métodos
As técnicas mais utilizadas, para a obtenção de pós de BT são: reação no estado solido (processo convencional), sol-gel, coprecipitação (oxalato) e síntese hidrotérmica (MENDES FILHO, et al, 1998). Para obtenção dos óxidos ternários puros e dopados com íons lantanídeos utilizou-se o método dos precursores poliméricos, uma variação do método sol gel proposto por Pechini (PECHINI, M. P., 1967), por entender-se se tratar de um método que possibilitam um melhor entendimento dos processos químicos bem como um melhor controle da estequiometria da reação. Os reagentes de partida utilizados foram nitrato de bário (Vetec 99 %), isopropóxido de titânio (Sigma Aldrich 97%), acetato de európio (III) (Sigma Aldrich 99,9 %), óxido de samário (Merck 99,9 %), ácido cítrico (Merck 99,5%) e etileno glicol (Merck 99,5 %). Foram feitos cálculos estequiométricos de forma que os materiais obtidos obedeceram a relação ABO3 para o material puro e A2- 3x/2TRxBO3 para o material dopado. Inicialmente foram feitos ensaios para evitar que o isopropóxido de titânio sofresse hidrólise adicionando-se álcool isopropílico e a solução de ácido cítrico. Após a dissolução do isopropóxido, foram adicionadas soluções dos íons dopantes que foram, previamente, calculados obedecendo a uma relação molar de 1 mol de metal para 3 mols de ácido cítrico, de acordo com LEMOS, F. C. D et al, 2008. A mistura reacional foi mantida sob agitação e aquecimento com a temperatura aproximadamente 80 ºC. Nesta etapa, o meio reacional obtido apresentou pH ácido (~2), ao qual foi adicionado hidróxido de amônio, evitando-se a possível precipitação de citratos dos metais, controlando-se o pH para que fosse mantido em aproximadamente 4-5. A solução de citratos metálicos foi mantida sob agitação e quando atingiu a metade do volume inicial foi adicionado etileno glicol, em uma razão mássica de 60/40 em relação à quantidade total de ácido cítrico, para que ocorresse uma reação de esterificação. A polimerização promovida pelo aquecimento da mistura reacional, baseado no método aplicado, resultou em uma solução homogênea o que sugere que os cátions metálicos estão uniformemente distribuídos na matriz orgânica. As soluções poliméricas de titanatos de bário puro (BT) e dopados com samário (BTSm) e európio (BTEu) a 1, 3 e 5% foram posteriormente pré-calcinadas a 300 oC, para o início da pirólise do poliéster, por duas horas, obtendo-se materiais carbonizados. Estes materiais resultantes foram desagregados utilizando-se almofariz e armazenados para serem analisados utilizando-se métodos físicos químicos. Os materiais obtidos foram submetidos à análise termogravimétrica, inicialmente, seguindo-se de tratamentos térmicos a várias temperaturas por 2 horas e posterior análise por DRX, MEV e Espectroscopia de emissão.
Resultado e discussão
A partir das análises termogravimétricas (TG), pode-se inferir a respeito da
temperatura de tratamento térmico na obtenção da fase desejada. As análises
foram obtidas através do equipamento SDT Q600, da TA Instruments, utilizando
como gás de purga o ar sintético, razão de aquecimento 10 °C/min em cadinho
de alumina e temperatura final 1000 °C. Na figura 01 encontra-se o resultado
representativo da análise de TG.o comportamento das curvas
termogravimétricas é similar. Pode-se observar uma primeira região, em torno
de 200 ºC, onde existe uma perda de massa que pode ser associada à
eliminação da água existente na resina de BaTiO3. Também pode ser observada
uma perda intensa de massa, na faixa aproximadamente 400 a 650 °C, devido à
pirólise da substância com liberação de CO2. Esse processo de perda de massa
na amostra pode ser atribuído, principalmente, a reações de desidratação do
polímero. Na etapa seguinte ocorrem principalmente as reações de
combustão/oxidação seguidas por formação de fases intermediárias de
Carbonato de Bário (BaCO3) e no terceiro intervalo há principalmente a
quebra das últimas cadeias orgânicas e a formação da fase cristalina
(CERCONI, C. et. al, 2013). Também se pode observar uma pequena perda de
massa em torno de 800 a 900 oC, que pode ser observado pelas derivadas dos
três materiais. Ainda foi observado que os eventos por perda de massa na
faixa 500 a 600 oC foi mais acentuado para o BTSm1. Na figura o2pode-se
observar que os eventos térmicos relativos à perda de massa, foram
diferentes para os pós cerâmicos em estudo e que as curvas
termogravimétricas apresentaram um aspecto semelhante mostrando,
basicamente, três patamares de perdas de massa, com a primeira faixa
aproximadamente de 30 e 200 ºC. A temperatura final para os eventos
relativos à perda de massa ocorre na faixa, de aproximadamente, de 800 a 900
oC, mas acima de 900 oC ainda se percebe eventos de perda de massa através
das curvas de derivada.Os materiais tratados a 300, 500, 700 e 900 oC por 2
horas foram submetidos a análise de DRX utilizando o aparelho X-RAY
DIFFRACTOMETER, modelo XRD-7000, Shimadzu. A radiação usada foi Cu-kα com
faixa 2θ de varredura de 05 a 120 graus. Para os materiais tratados 1100 oC
por 2 horas foi utilizado o aparelho D8 ADVANCE da Bruker, radiação Cu-kα e
faixa de varredura de 10 a 90 graus. Os difratogramas de raios X para os
compostos BT puro e dopados foram padronizados na faixa, de 15 a 80 graus,
exceto a análise Rietveld. A partir dos difratogramas produzidos, pode-se
observar que, para o BT e BTEu, a 300 oC o material se apresentaram amorfos
e nas temperaturas de 500, 700 e 900 oC não se apresentaram monofásicos. No
nosso trabalho foi observado a fase cúbica majoritária e carbonato de bário
(24 graus) como fase secundária, tanto para o composto puro como para os
dopados. Na figura 10 é apresentado o resultado da análise Rietveld para o
BTSm1 tratado a 900 oC por 2 horas, que é representativa para todos os
compostos visto que são similares. A partir figura pode-se observar que
temos 86,1 % da fase cúbica tem e 13,9 % da fase secundária identificada
como BaCO3.A formação do BaCO3 é citada na literatura, como por exemplo o
BaCO3 de simetria ortorrômbica, foi observada em torno de 950 °C, onde este
sinal é praticamente nulo acima desta temperatura, seguido da formação da
estrutura cristalina do BaTiO3. Desta forma, os autores concluem que o
aumento da temperatura de tratamento térmico reduz a intensidade dos picos
do BaCO3, isto é, evidencia que o aumento da temperatura promove a
decomposição do carbonato de bário com formação do BT (BRITO, S. L. M. e
GOUVÊA, D., 2010).A análise por DRX pode-se comprovar que os compostos
dopados com samário apresentam comportamento similar daqueles obtidos com
európio. A partir dos dados de DRX para os compostos tratados termicamente a
1100 oC, se pode observar, ainda, a presença do BaCO3, embora o pico seja
menos intenso que a 900 oC. Em seu trabalho, BRITO, S. L. M. e GOUVÊA, D.,
2010, observou a formação de BaCO3 na obtenção do BT pelo método Pechini e
fez tratamento dos pós contendo BaCO3 por lixiviação ácida. No nosso
trabalho os pós obtidos a 1100 oC foram tratados com ácido acético PA,
aquecidos em chapa suportados em cadinho e posteriormente realizada a
análise por DRX que se pode verificar a que o pico em aproximadamente 24
graus, o qual foi identificado como BaCO3 por análise Rietveld, tem menor
intensidade que aqueles do material tratado termicamente a 900 oC, sugerindo
que o aumento da temperatura de tratamento térmico leva a formação da fase
perovskita desejada, no entanto observou-se que na temperatura de 1100 oC os
pós iniciam a sinterização. NOs pós que foram submetidos ao processo de
lixiviação ácida, o pico da fase carbonado não é observado, não há fases
secundárias, sugerindo a dissolução total do carbonato. Os pós obtidos a
1100 oC foram analisados por MEV e as micrografias estão dispostas nas
figuras de 18 a 22. Foram feitas micrografias do BT sem o tratamento com
ácido, onde se observou formações em forma de bastonetes que foi associado
ao carbonato de bário.
A partir das micrografias de MEV, pode-se observar que as amostras são
cristalinas, assim como foi confirmado pelas DRX anteriormente apresentadas.
Em todas as amostras observou-se que são formadas por partículas de dimensão
manométrica. Também se pode observar que as amostras são porosas e, de
maneira geral, apresentam uma morfologia uniforme, com sinais de início de
sinterização. As características da emissão de íons terras raras dependem da
matriz hospedeira na qual os íons são incorporados. O campo ligante em torno
do íon pode ter uma influência considerável sobre a absorção óptica, emissão
e nas taxas de decaimento fluorescentes, e os processos não radiativos
incluem características da matriz e da concentração de íons ativos. As
propriedades fotoluminescentes (FL) dos compostos com íons lantanídeos Eu3+
e Sm3+ inserido na matriz de BT obtido pelo método Pechini foi estudado em
função das diferentes concentrações de dopagem. Os espectros de emissão FL
das amostras de BT: Eu3+/Sm3+ (1,3 e 5%) foram obtidas com comprimento de
onda de excitação fixado em 398 e 409 nm, respectivamente.
Os espectros de emissões obtidos por excitação direta no íon Eu3+ em 398 nm
(5L6← 7F0), exibindo linhas finas correspondentes às transições 5D0 →7FJ
(onde, J = 0-4) típicas de compostos contendo íons Eu3+. A transição 5D0
→7F1 (mais intensa do espectro), sendo o 5D0 →7F2, a segunda transição mais
intensa e é hipersensível ao ambiente químico, podendo variar sua
intensidade de acordo com a simetria pontual do íon Eu3+ (ELISEEVA, S. V. e
BUNZLI, J. –C. G., 2010), assim sendo a principal responsável pela coloração
vermelha de fotoluminescência, que é observada para complexos de Eu3+. O
fato da intensidade da transição 5D0 → 7F1 ser mais intensa em relação ao
5D0 → 7F2, que indica uma alta simetria para o poliedro de coordenação do
íon Eu3+, tendo assim, mais de um sítio de coordenação com o íon Eu3+
(SHUVAEV et al., 2014), contudo presença da transição 5D0→7F0 neste perfil
espectral indica que o ambiente químico do íon Eu3+ está localizado em um
ambiente cuja simetria é do tipo Cn, Cnv ou Cs (TEOTONIO, E. E. S. et al,
2004). Foi observado, que com o aumento das dopagens os perfis espectrais
foram mantidos, o que corrobora com a alta estabilidade estrutural dos
compostos. As linhas de emissão mais intensas do íon Sm3+ ocorrem na faixa
de 550 a 720 nm, e seguem o mesmo perfil padrão de emissão para todas as
amostras. As transições principais correspondem às transições do nível 4G5/2
para os níveis 6H5/2, 6H7/2, 6H9/2 e 6H11/2, respectivamente, para todas as
amostras analisadas. Entre estes, a transição 4G5/2 → 6H7/2 em 595 nm, tendo
intensidade mais forte e pode ser aplicada para displays de materiais
emissores na região laranja-avermelhado ( GYU, M., 2012; PEKGÖZLU, I e
ÇAKAR, 2012)
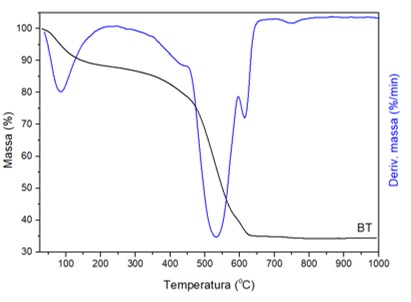
Curva termogravimétrica com derivada para o BT
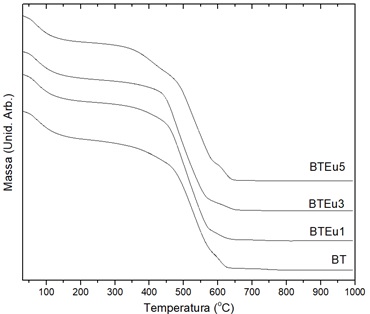
Curva termogravimétrica do BT puro e dopados com európio.
Conclusões
A parte experimental utilizando o método Pechini, possibilitou a obtenção de resinas com aspectos homogêneos sugerindo coerência na rota utilizada. A partir dos resultados de DRX podemos observar a estrutura perovskita obtida. Analisando os resultados do MEV, observamos que a morfologia dos materiais form semelhantes, com a superfície porosa. Também observamos, pelos resultados de emissão, que esses materiais apresentam potencial aplicação em dispositivos fotônicos. O presente trabalho foi desenvolvido na Universidade Federal do Tocantins (UFT) com o programa PIBIC/CNPq
Agradecimentos
Agradecemos a UFT, ao CNPq pela bolsa concedida, ao laboratório de cimentos da UFRN (NTCPP), ao laboratório de Terras Raras-BSTR da UFPE
Referências
BRITO, S. L. M.; GOUVÊA, D. Caracterização superficial de nanopartículas de BaTiO3 preparado pelo método dos precursores poliméricos, Cerâmica 56, 228-236 (2010).
BRITO, S. L. M.; GOUVÊA, D. Obtenção de BaTiO3 livre de resíduos de carbonato de bário pelo método dos precursores poliméricos, Cerâmica 57, 338-347(2011).
CALLISTER JR., W. D.; Ciência e Engenharia de Materiais: Uma introdução. Tradução de Sergio Murilo Stamile Soares. Rio de Janeiro: Livros Técnicos e Científicos. Editora S. A., p589 (2002).
CERCONI, C., PABLO, P., BORRERO, G.; Preparação e caracterização de pós e filmes finos de BaTiO3 sintetizados via método Pechini, Revista Matéria, v. 18, n. 04, pp. 1510 – 1524 (2013).
DANIELS, J.; HARDTL, K. H.; WERNICKE, R., The PTC Effect of Barium Titanate, Philips Technical Review, 38, 73-82 (1978).
ELISEEVA, S. V; BUNZLI, J.-C. G. Lanthanide luminescence for functional materials and bio-sciences. Chemical Society reviews, v. 39, n. 1, p. 189–227 (2010).
GYU, M. Sm 3 + -doped CaTiO3. phosphor : Synthesis , structure , and photoluminescent properties. Ceramics International, v. 38, n. 2, p. 1365–1370 (2012).
KISHI, H., MIZUNO, Y. e CHAZONO, H Base-metal electrode-multilayer ceramic capacitors: past, present and future perspectives, Jpn. J. Appl. Phys. 42, 1–15 (2003).
LEMOS, F. C. D.; Silva, J. E. C.; Melo, D. M. A.; Câmara, M. S. C.; Lima, P. S. e Carneiro, C. E. J.; Green and Red Upconversion Emissions of Er3+/Yb3+-Codoped SrTiO3 Powder Prepared by a Polymeric Precursor Method Inorg. Mater. 44, 866 (2008).
LEITE, E.R., CARREÑO, N.L.V., SANTOS, L.P.S., et al., “Photoluminescence in amorphous TiO2–PbO systems”. Applied physics A, v. 73, n.5, pp. 567-569 (2001).
LEITE, E.R. , PONTES, F.M., LEE, E.J.H., AGUIAR, R., LONGO, E.,. PONTES, D.S.L, NUNES, M.S.J. , MACEDO, H.R., PIZANI, P.S. , LANCIOTTI JR, F. , BOSCHI, T.M., VARELA, J.A. e PASKOCIMAS, C.A. “A novel approach for the development of photoluminescente material”. Applied physics A ((Appl. Phys. A ) 74, 529–532 (2002)
MAMBRINI, G. P., MOREIRA, M. L., GURGEL, M. F. C., et al., “Photoluminescence of Barium Titanate and Barium Zirconate in Multilayer Disordered Thin Films at Room temperature”. J. Phys. Chem. A, v. 112, n.38, pp. 8938–8942 (2008).
MCKEE, R. A.; WALKER, F. J. AND CHISHOLM, M. F. Physical structure and inversion charge at a semiconductor interface with a crystalline oxide. Science, 293, 486 (2001).
MELÉNDEZA, J. J., YOHANDYSA.ZULUETAC, YURIMILERLEYET, First-principles study of neutral defects in Fe-doped cubic barium titanate, Volume 41, Issue 1, Part B, January, 1647-1656 (2015).
MENDES FILHO, A. A; ARAUJO, FGS; PINTO, L C B M; SOUZA, V. F., Processamento Hidrotérmico de Pós de BaTi4O9 e Ba2Ti9O20, Congresso Brasileiro de Cerâmica, 45, 01-08 (1998).
PECHINI, M. P.; U. S. Patent No 3330697, July 11 (1967).
PEKGÖZLÜ, İ & ÇAKAR, S. Photoluminescence properties of Li6CaB3O8.5: M3+ (M3+: Dy and Sm). Journal of Luminescence. v. 132, p. 2312–2317 (2012).
SADHANA, K., KRISHNA VENI, T., PRAVEENA, K. “Microwave sintering of nanobarium titanate”, Scripta materialia, v. 59, n.5, pp. 495-498, April (2008).
SCHNEIDER JR., S. J., Engineered Materials Handbook: Ceramics And Glasses, vol.4, USA: ASM International, 1112-1118 (1991).
SHUVAEV, S. Lanthanide complexes with aromatic o-phosphorylated ligands: synthesis, structure elucidation and photophysical properties. apud Dalton transactions (Cambridge, England : 2003), v. 43, n. 8, p. 3121–36 (2014)
SIRENKO, A. A.; BERNHARD, C.; GOINIK, A.; CLARK, A. M.; HAO, J,; Si, W. Soft-mode hardening in SrTiO3 thin films, Nature,404, 373-376 (2000).
SPORN, D., MERKLEIN, S., GROND, W., “Sol-gel processing of peroviskita thin films”. Microelectronic engineering, v.29, n.1-4, pp. 161-168 (1995).
TEOTONIO, E. E. S. et al. Synthesis, crystalline structure and photoluminescence investigations of the new trivalent rare earth complexes (Sm3+, Eu3+ and Tb3+) containing 2-thiophenecarboxylate as sensitizer. Inorganica Chimica Acta, v. 357, n. 2, p. 451–460 (2004).
WEIRICH, TH. E.; WINTERER, M.; SEIFRIED, S.; HAHN, H. E FUESS, H. Rietveld analysis of electron powder diffraction data from nanocrystalline anatase, TiO2, Ultramicroscopy, 81, 263 (2000).
ZDOROVETSA, M.V. e KOZLOVSKIYA, A..L., Study of the effect of La3+doping on the properties of ceramics based onBaTiOx , Vacuum 168 (2019) 108838









