COMPLEXO [Fe(AT)2 (H2O)4](SO4)2, ONDE AT= ÁCIDO TARTÁRICO: ESTUDOS DE INIBIÇÃO DA ENZIMA ACETILCOLINESTERASE
ISBN 978-85-85905-25-5
Área
Iniciação Científica
Autores
Araújo, A.S. (UECE) ; Pinheiro, S.O. (UECE) ; Nascimento, M.C. (UECE) ; Silva, W.M.B. (UECE) ; Morais, S.M. (UECE) ; Alves, D.R. (UECE)
Resumo
A Química dos compostos de coordenação é um campo da Química Inorgânica que está inserido em diversos processos químicos, biológicos e industriais. O íon ferro tem grande importância biológica, está no transporte de elétrons em plantas e animais e no transporte e armazenamento de oxigênio em mamíferos. O Ácido Tartárico é encontrado quase exclusivamente na videira e é muito utilizado como antioxidante. O objetivo desse trabalho foi complexar ácido tartárico ao centro de Fe2+, a fim de unir as propriedades biológicas e químicas e formar um novo composto de coordenação. As caracterizações realizadas por espectroscopia na região do ultravioleta e visível e na região do infravermelho confirmam a coordenação. O teste de inibição da enzima acetilcolinesterase apresentou resultado satisfatório.
Palavras chaves
Síntese; Ácido Tartárico; Ferro
Introdução
Os complexos inorgânicos estão presentes na maioria dos processos químicos que envolvem espécies inorgânicas em temperaturas não muito elevadas. Estão presentes em fenômenos vitais como a respiração e a fotossíntese (FARIAS, 2019). O íon ferro é um micronutriente essencial e um componente intrínseco da hemoglobina, mioglobina e citocromos. Entre as funções do ferro, destacam-se a formação de hemácias, transporte de O2 e CO2, transferência de elétrons, reações redox e produção de energia celular (CAETANO-SILVA et al., 2017). A Química do ferro é enriquecida pelo número de estados de spin acessíveis, incluindo complexos de ferro de alto, intermediário e baixo spin (CHEN; BROWNE, 2018). Tendo em base essa diversidade de complexos de ferro, procurou-se sintetizar um complexo de ferro com o ácido tartárico. O ácido tartárico é um ácido orgânico com dois carbonos quirais (CHEN et al., 2018) e três estereoisômeros diferentes, ácido (R,R)-(+)-tartárico, ácido (S,S)- (-)-tartárico e ácido meso-tartárico (KHAN et al., 2006). Tem muitas aplicações, como um agente de acidificação, antioxidante, bem como uso nas indústrias de alimentos, panificação e farmacêutica (LOURENÇO et al., 2018). A fim de analisar suas especificidades quando complexado ao íon metálico faz-se necessária uma caracterização para compreender como essas interações sucederam e transformaram as propriedades atuais da molécula. Considerando- se todas as propriedades específicas do ácido tartárico, há uma tentativa por meio deste estudo complexá-lo ao íon metálico ferro, a fim de intensificar suas propriedades, principalmente a sua característica de inibição da enzima acetilcolinesterase, assim como, desenvolver novos atributos com a formação do complexo.
Material e métodos
A síntese do composto inorgânico foi realizada com adaptações da literatura seguindo a metodologia de CUIN (2004). Para a obtenção do complexo foram utilizados sulfato de ferro(II) heptahidratado (FeSO4.7H2O) e tartarato de sódio e potássio (KNaC4H4O6·4H2O). A água destilada foi o solvente utilizado na síntese. Inicialmente dissolveu-se 0,6 g do sal de ferro em 20 mL de água e 0,12 g do sal de tartarato em 20 mL de água, em um balão de fundo redondo adicionou-se a solução de FeSO4 e então a solução de KNaC4H4O6·4H2O e manteve-se sob agitação por 20 minutos. Passados 20 minutos adicionou-se 3 gotas de trietilamina e manteve-se em agitação por 2 horas. Após a síntese, o composto foi filtrado e mantido em dessecador sob vácuo. O espectro eletrônico na região do ultravioleta e visível (UV-Vis) foi obtido utilizando-se um equipamento de espectrofotômetro SHIMADZU UV-1800 e uma cubeta de quartzo, as soluções aquosas tinham 1x10-3 mol/L, em uma faixa de comprimento de onda de 200 nm a 800 nm. Os espectros vibracionais na região do infravermelho (IV) foram adquiridos utilizando um espectrofotômetro modelo Nicolet iS5 da Thermo Scientific. As amostras foram preparadas na forma de pastilhas de KBr, empregando-se 32 scans e resolução de 4 cm-1. A atividade inibitória da enzima acetilcolinesterase (AChE) foi aferida em placas de 96 poços de fundo chato utilizando leitor de absorbância de microplacas Elisa BIOTEK, modelo ELX 800, software “Gen5 V2.04.11”, baseando-se na metodologia descrita por ELLMAN et al. (1961). Em placas de 96 poços, foram utilizadas as seguintes soluções por poço: 25 µL de iodeto de acetiltiocolina (15 mM), 125 µL de 5,5’–ditiobis-[2-nitrobenzóico] na solução Tris/HCL (50nM, pH=8, com 0,1 M de NaCl e 0,02 M de MgCl2 .6H2O. (3 mM, DTNB (Ácido Ditionitrobenzoico) ou reagente de Ellman), 50 µL da solução Tris/HCL (50 nM, pH=8, com 0,1% de albumina sérica bovina (BSA)), 25 µL da amostra de extrato dissolvida em Metanol e diluída 10 vezes na solução Tris/HCL (50 mM, pH=8) para obter uma concentração final de 0,2 mg.mL-1 (Rhee et al. 2001, Trevisan et al. 2003). A absorbância foi aferida a 405 nm durante 30 segundos. Em seguida, foram adicionados 25 µL da enzima acetilcolinesterase (0,25 U.mL-1) e a absorbância foi aferida por minuto até o total de 25 minutos de incubação da enzima. A porcentagem de inibição da acetilcolinesterase foi calculada através da comparação das velocidades de reação (hidrólise do substrato) das amostras em relação ao branco (considerada atividade total da AChE, 100%). O padrão utilizado como controle positivo é a fisostigmina (eserina).
Resultado e discussão
A solução de sulfato de ferro(II) e de tartarato de sódio e potássio
apresentava cor translúcida, ao longo do processo de síntese a solução
apresentou mudança em sua coloração, passando por amarelo claro, verde musgo
e finalmente âmbar, essa mudança de coloração da reação é um indicativo de
que houve coordenação. Para realizar a análise espectroscópica, na região do
UV-Vis, dissolveu-se o sal do metal, (FeSO4), o ligante (KNaC4H4O6·4H2O) e o
complexo obtido, em água. De acordo com os dados obtidos, o ligante
tartarato de ferro e potássio apresentou uma única banda em 206 nm,
atribuída às transições intraligantes do tipo n→π* e também ao grupo
cromóforo do ácido tartárico (ARAÚJO, 2016), no sulfato de ferro observou-se
duas bandas em 238 nm e 312 nm. No espectro do complexo em estudo, são
observadas três bandas em valores de 207 nm, atribuída a transições
intraligantes, 306 nm e 352 nm, que são atribuídas à transições metal-
ligante (Figura 01). O espectro na região do infravermelho atribuído para o
ligante tartarato de sódio e potássio livre, apresenta os principais
alongamentos, estiramentos e deformações decorrentes das vibrações das
moléculas. Com os dados observados no espectro do ligante, observa-se o
estiramento assimétrico da carbonila (C=O) em 1610 cm-1, próximo ao valor
de referência (SHYJU; ANANDHI; GOPALAKRISHNAN, 2012). As bandas
características de grupamento (-OH) do ácido carboxílico podem ser
observadas nos valores de 3271 cm-1, 2981 cm-1, 2935 cm-1 (SHYJU; ANANDHI;
GOPALAKRISHNAN, 2012). A banda em 1247 cm-1 é referente ao estiramento (C-O)
de ácido carboxílico (ARAÚJO, 2016). Os valores de 3470 cm-1 e 3405 cm-1
estão relacionados ao ânion carboxilato (SHYJU; ANANDHI; GOPALAKRISHNAN,
2012). Já as bandas de 1117 cm-1 e 1070 cm-1 são referentes ao fraco
estiramento (C-C) (SHYJU; ANANDHI; GOPALAKRISHNAN, 2012). Para o complexo
obtido (Figura 02), houve um deslocamento para uma maior frequência na banda
referente ao grupamento carbonila (1635cm-1 no complexo) (MATHIVANAN et al.,
2014). Essa mudança pode indicar a coordenação do ligante ao metal pelo
oxigênio carbonílico do ligante. A banda em 1635 cm-1 pode ser atribuída ao
estiramento assimétrico do grupo carboxilato coordenado ao metal, já a banda
em 1399 cm-1, ao estiramento simétrico do grupo carboxilato. Essas bandas
não foram observadas no ligante livre confirmando a coordenação pelo
oxigênio carbonílico. Para identificar se o grupo carboxilato coordenou-se
ao íon metálico de modo monodentado, bidentado ou em ponte, realizou-se a
diferença dos modos vibracionais simétrico e assimétrico desse grupo [∆ν =
νass (COO-) - νs (COO-)] (LACHTER, 2009). Quando ∆ν > 200 cm-1, o grupo
carboxilato coordenou-se de forma monodentada. O valor de ∆ν é 236 cm-1,
sugerindo a coordenação de modo monodentado (MATHIVANAN et al., 2014). A
Figura 03 mostra a estrutura proposta para o complexo. Para o teste de
inibição da enzima acetilcolnesterase a amostra do complexo em estudo foi
analisada em triplicata. A amostra apresentou coloração própria absorvida
pelo espectro de onda de leitura, sendo assim, foram deduzidos os valores
referentes à coloração. Após normalização dos dados foi realizado teste de
curva de regressão não linear pelo programa estatístico GraphPad Prism v7.0
obtendo os seguintes resultados preliminares: FISO; IC50 (1,15), Std. Error
(0,05), 95% Confidence intervals (0,9091 to 1,446), R2 (0,996)
[Fe(AT)2(H2O)4](SO4)2; IC50 (8,80), Std Error (0,03), 95% Confidence
intervals (7,562 to 10,23), R2 (0,951). De acordo com o que pode ser
observado nos resultados obtidos, o complexo em estudo apresentou inibição
da enzima acetilcolinesterase com valor de IC50 em 8,80.
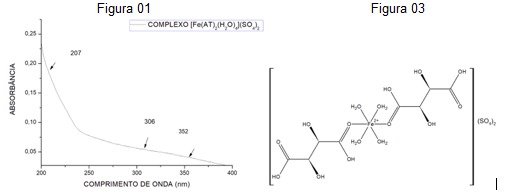
Figura 01 - Espectro eletrônico na região UV- Vis (concentração de 1x10-3 mol/L) e Figura 03 - Estrutura Proposta para complexo [Fe(AT)2(H2O)4](SO4)2
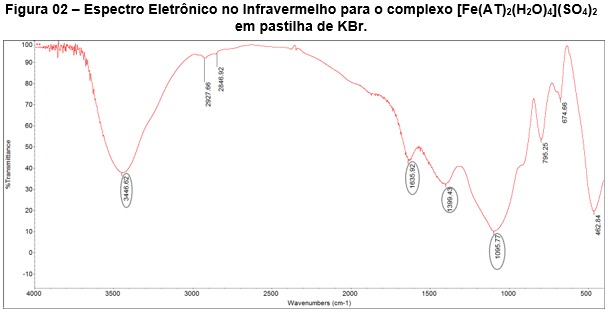
Figura 02 – Espectro Eletrônico no Infravermelho para o complexo [Fe(AT)2(H2O)4](SO4)2 em pastilha de KBr
Conclusões
De acordo com os resultados obtidos na síntese e no estudo espectroscópico do composto [Fe(AT)2(H2O)4](SO4)2 demonstrou-se que ocorreu a coordenação do ligante ao íon metálico. O complexo em estudo foi solúvel em água, isso se torna altamente adequado, uma vez que muitas reações biológicas acontecem em meio aquoso. A análise espectroscópica na região do ultravioleta e visível pôde confirmar a coordenação do ácido tartárico ao centro metálico através das mudanças de bandas. E a análise do espectro do infravermelho evidenciou que a coordenação se realizou pelo oxigênio carboxílico do metal de modo monodentado. A formação do complexo [Fe(AT)2(H2O)4](SO4)2 apresenta-se propícia para estudos biológicos posteriores, uma vez que, espera-se aumentar as propriedades do ácido tartárico após coordenação, unindo as características químicas e biológicas da molécula de ácido tartárico com propriedades inorgânicas com o centro do íon ferro.
Agradecimentos
À Universidade Estadual do Ceará, ao Laboratório de Química Inorgânica (LQUIN) – UECE, ao Laboratório de Química de Produtos Naturais (LQPN) – UECE
Referências
ARAÚJO, A. M. U. DE. Síntese e Caracterização de Complexos de Co(II) e Ni(II) com L-DOPA, CARBIDOPA E BENZIMIDAZOL. [s.l.] Universidade Federal do Rio Grande do Norte, 2016.
CAETANO-SILVA, M. E. et al. Synthesis of whey peptide-iron complexes: Influence of using different iron precursor compounds. Food Research International, v. 101, n. May, p. 73–81, 2017.
CHEN, J.; BROWNE, W. R. Photochemistry of iron complexes. Coordination Chemistry Reviews, v. 374, p. 15–35, 2018.
CHEN, T. et al. Experimental and theoretical investigations of tartaric acid isomers by terahertz spectroscopy and density functional theory. Spectrochimica Acta - Part A: Molecular and Biomolecular Spectroscopy, v. 205, p. 312–319, 2018.
CUIN, A. Síntese, Estrutura e Propriedades de Complexos de Molibdênio, Prata e Chumbo com Ácidos α-Hidrocarboxílicos. [s.l.] Universidade Estadual Paulista, 2004.
ELLMAN, G. L.; COURTNEY, K. D.; ANDRES JUNIOR, V.; FEATHERSTONE, R. M. A new and rapid calorimetric determination of acetylcholinesterase activity. Department of Pharmacology, University of California Medical Center. San Francisco. v.7, p. 88-95
FARIAS, R. F. DE. Química de coordenação fundamentos e atualidades. 2. ed. Campinas: Átomo, 2009.
KHAN, A. R. et al. Spectrometric and Electrochemical Investigation of Vanadium(V) and Vanadium(IV) Tartrate Complexes in Solution. v. 17, n. 5, p. 895–904, 2006.
LACHTER, D. R. NOVOS COMPLEXOS DE Mn (II), Co(II) e Au(III) COM LIGANTES DO GRUPO DAS FLUORQUINOLONAS: ESTUDOS ESPECTROSCÓPICOS, 2009.
LOURENÇO, A. S. et al. Voltammetric determination of tartaric acid in wines by electrocatalytic oxidation on a cobalt(II)-phthalocyanine-modified electrode associated with multiway calibration. Analytica Chimica Acta, n. Ii, p. 29–37, 2018.
MATHIVANAN, V. et al. Synthesis and characterization of gel-grown cobalt tartrate crystals. Pramana - Journal of Physics, v. 82, n. 3, p. 537–548, 2014.
SHYJU, T. S.; ANANDHI, S.; GOPALAKRISHNAN, R. Comparative studies on conventional solution and Sankaranarayanan-Ramasamy (SR) methods grown potassium sodium tartrate tetrahydrate single crystals. CrystEngComm, v. 14, n. 4, p. 1387–1396, 2012.









