Avaliação de síntese da zeólita ZSM-5 através dos métodos hidrotérmico, solvotermal e conversão de gel seco
ISBN 978-85-85905-25-5
Área
Materiais
Autores
Silva, D.P.S. (UFAL) ; Sarmento, L.R. (UFAL) ; Silva, D.C.M. (UFAL) ; Ribeiro, T.R.S. (UFBA) ; Silva, J.B.B. (UFAL) ; Peixoto, A.C.P. (UFAL) ; Silva, A.O.S. (UFAL)
Resumo
O presente trabalho apresenta a síntese da zeólita ZSM-5, através de três metodologias distintas, o método hidrotérmico, o método solvotermal e o método conversão de gel seco, a fim de analisar qual destes torna-se mais viável economicamente para obtenção do catalisador. As zeólitas foram caracterizadas por difratometria de raios X (DRX), análises térmicas (TG/DTG) e adsorção- dessorção de nitrogênio. Dessa forma, com base nos parâmetros discutidos nesse trabalho, a metodologia de síntese através do método hidrotérmico foi mais promissora em comparação com o método solvotermal e conversão de gel seco.
Palavras chaves
ZSM-5; método solvotermal; conversão de gel seco
Introdução
As zeólitas são polímeros inorgânicos complexos e cristalinos, de origem natural ou sintética, baseadas num arranjo tridimensional constituída por tetraedros TO4 (T= Si ou Al) interconectados através de um átomo de oxigênio em comum (ENGLERT; RUBIO, 2005). Nessa configuração, as cargas negativas dos tetraedros de AlO4 são compensadas por cátions alcalinos e/ou alcalinos terrosos, formando uma estrutura com canais, permitindo a troca iônica e uma hidratação reversível (SHINZATO, 2007). Devido às propriedades das zeólitas, como arranjo cristalino, elevada área superficial, acidez, capacidade de troca iônica e seletividade, estas são utilizadas em uma variedade de aplicações como: processos de separação de gás, catálise, adsorventes e trocadores iônicos de alta seletividade (CHEN et al., 2018). A zeólita ZSM-5 (Zeolite Socony Mobil - 5) foi desenvolvida pela Mobil Oil Corporation em 1975. É uma zeólita que se caracteriza pelo alto teor de silício na estrutura (relação Si/Al entre 11 e infinito) e possui estrutura tipo MFI (Mobil Five) de acordo com a classificação da International Zeolite Association (IZA). É utilizada como catalisador na indústria petroquímica em processos de isomerização, alquilação e aromatização (SANG et al., 2004). O método mais utilizado para a síntese de zeólitas e materiais microporosos é a cristalização hidrotérmica, que se refere à síntese por reações químicas de substâncias em uma solução aquosa aquecida acima da temperatura ambiente e pressão (XU et al., 2015). A água solubiliza os componentes da mistura reacional em vários graus, controla a concentração e o pH, onde cada estrutura é favorecida por uma característica específica, ajuda na estabilização final da microporosidade cristalina através da coordenação com cátions balanceadores de carga no produto final evitando o preenchimento parcial da microporosidade resultante (BAYATI; BABALUO; KARIMI, 2008). A adição de solventes orgânicos, através do método solvotermal, altera a viscosidade do meio reacional e, portanto, a capacidade de interação das espécies reagentes, levando a uma modificação no processo de cristalização e, possivelmente a formação de novas fases cristalinas ou a obtenção de fases já conhecidas com propriedades texturais diferentes das obtidas em meios aquosos. Este é o caso, por exemplo, da sodalita, silicalita-1, ZSM- 39, ZSM-48 e ZSM-5 (SUZUKI et al., 2009). Nos últimos anos pesquisadores vem estudando um novo método de síntese de zeólitas, denominado conversão de gel seco (Dry Gel Conversion, DGC). Xu e colaboradores (1990) foram os primeiros pesquisadores a abordarem a utilização deste novo método de síntese. Esses relataram que o gel seco de aluminosilicato pode ser transformado em MFI por contato com os vapores de água e de aminas voláteis. Desde então, tais métodos para sintetizar zeólitas têm sido amplamente desenvolvidos. Segundo Murrell e colaboradores (1999) esta nova metodologia de síntese, quando estiver completamente otimizada, poderá produzir zeólitas com diversas vantagens em relação aos métodos convencionais de síntese hidrotérmica, tais como redução do tempo total de síntese por batelada, eliminação da etapa de filtração, o que implica em uma economia considerável para o processo e substituição, no caso, de catalisadores industriais, da etapa de extrusão da zeólita pela extrusão da sílica-alumina que acarreta em menor perda de materiais. Dessa forma, o presente trabalho estudou a síntese da zeólita ZSM-5, através dos métodos hidrotérmico, solvotermal e conversão de gel seco analisando a velocidade de cristalização e propriedades texturais sobre o processo de cristalização dos materiais zeolíticos, com o objetivo de avaliar qual desses métodos melhor favorece na formação de um material cristalino. Os sólidos foram caracterizados por difratometria de raios X (DRX) para identificação das fases e o grau de cristalinidade e, as amostras isentas de fases concorrentes e mais cristalinas foram caracterizadas adicionalmente por análises térmicas (TG/DTG) e adsorção-dessorção de nitrogênio.
Material e métodos
Síntese das zeólitas A composição e o procedimento de preparo dos géis de síntese foram baseados nos métodos descritos por Szostak (1998) e Argauer e Landolt (1972). Os reagentes precursores foram misturados a partir das seguintes composições molares: 10,6 TPABr : 100 SiO2 : 1,0 Al2O3 : 14,3 Na2O : 2000 H2O (método hidrotérmico), 10 TPABr : 100 Etanol :1,0 SiO2 : 0,01 Al2O3 : 0,3 Na2O : 20 H2O (método solvotermal) e 10,6 TPABr : 14,3 Na2O: 1,0 Al2O3: 100 SiO2: 2000 H2O (método conversão de gel seco). O procedimento de mistura dos reagentes precursores para os métodos estudados foram realizados nas seguintes etapas: (i) Dissolução do silicato de sódio em 40% da água, logo após, adição do sulfato de alumínio octadecahidratado, sob agitação por 20 minutos (solução A), (ii) Diluição do ácido sulfúrico em 60% da água e a adição de brometo de tetrapropilamônio (TPABr), sob agitação por 20 minutos (solução B), (iii) Mistura das soluções A e B, sob agitação por 30 minutos. No método solvotermal, na última etapa houve também a adição do etanol. Para os métodos solvotermal e hidrotérmico, após o preparo do gel, este foi transferido para vasos de teflon, revestido em autoclaves de aço inoxidável e aquecido em estufas a 170 °C, de 5 a 96 horas. As autoclaves foram resfriadas a temperatura ambiente, e o sólido resultante foi separado do líquido sobrenadante por filtração à vácuo, sendo lavado com água destilada até atingir pH neutro, por fim, seco em estufa a 120 °C por 12 horas. No método de conversão de gel seco, após o preparo do gel de síntese este foi transferido para a estufa para evaporação de toda a água, a temperatura de 60 °C durante 48 horas. O material sólido obtido foi triturado e transferido para um suporte de teflon. No fundo da autoclave foi colocado 40 mL de água destilada. A cristalização das amostras foi realizada a uma temperatura de 170 °C, de 5 a 96 horas. Após a cristalização, a autoclave foi removida da estufa e resfriada a temperatura ambiente. O material sólido obtido foi seco a 100 °C por 24 horas. Todos os catalisadores sintetizados foram calcinados sob fluxo de ar de 100 mL.min-1 com uma rampa de aquecimento de 2 oC.min-1 até 550 oC por 6 horas. Caracterizações As análises de DRX foram realizadas utilizando um difratômetro da Shimadzu XRD-6000, com radiação CuKα (λ = 0,1542 nm), filtro de Ni, voltagem de 40 kV e corrente de 30 mA. A aquisição dos dados foi realizada no intervalo de 2θ entre 3 e 40º, com velocidade de varredura de 2°.min-1 e passo de 0,02°. As análises térmicas (TG/DTG) foram realizadas em uma termobalança da Shimadzu DTG-60H, com taxa de aquecimento 10 °C.min-1, sob atmosfera de ar sintético de 100 mL.min-1, de temperatura ambiente à 800 ºC. As medidas de adsorção- dessorção de nitrogênio foram realizadas em um equipamento Micromeritics ASAP 2020, a 196 °C, no qual as amostras foram previamente desgaseificadas por 12 horas, sob vácuo (2 μmHg) à 200 °C.
Resultado e discussão
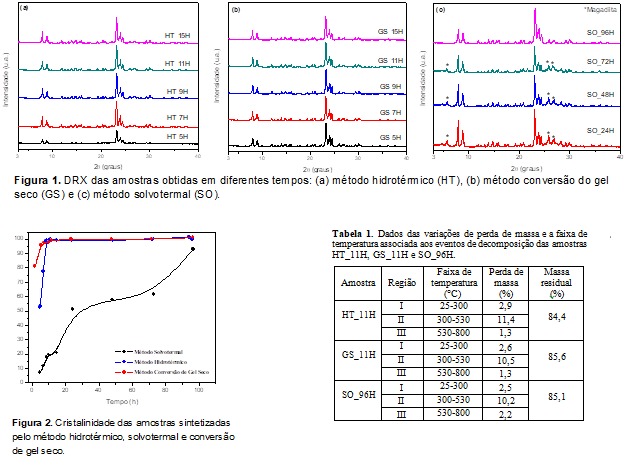
Os difratogramas das amostras sintetizadas pelo método hidrotérmico estão
apresentados na Figura 1(a), os quais demonstram que em todos os períodos
são apresentados os picos característicos referentes à estrutura MFI (JCPDS
Nº 42-0023) (RAZAVIAN; FATEMI, 2015), confirmando a eficácia da obtenção da
zeólita ZSM-5 pura e altamente cristalina através do método hidrotérmico.
A Figura 1(b) exibe os espectros das amostras sintetizadas pelo método
conversão de gel seco, os quais demonstram que em todos os períodos
estudados apresentaram os picos característicos referentes à estrutura MFI,
confirmando a aplicabilidade do método conversão de gel seco na obtenção da
zeólita ZSM-5 sem a presença de fases concorrentes e altamente cristalinas.
A Figura 1(c) apresenta os difratogramas das amostras sintetizadas pelo
método solvotermal, os quais demonstraram que entre 24 e 72 horas houve o
intercrescimento da fase lamelar Magadiita (JCPDS Nº 42-1350) em conjunto
com a ZSM-5. Estudos relatam a síntese da magadiita, com a proporção
SiO2:NaOH na faixa de 1,0 : 0,2 a 1,0 : 9,0, onde proporção SiO2:NaOH
utilizada neste trabalho foi de 1,0 : 0,3, podendo então a quantidade de
NaOH utilizada ter favorecido a formação da magadiita, levando à formação de
várias áreas segregadas classificadas em regiões zeolíticas e lamelares
(OZAWA et al., 2010; YILMAZ; MULLER, 2009). A zeólita ZSM-5 isenta de fases
concorrentes foi obtida somente com 96 horas de cristalização. Tempos de
cristalização inferiores a 24 horas foram obtidos materiais amorfos.
A Figura 2 apresenta a cristalinidade das amostras sintetizadas
através dos métodos hidrotérmico, conversão de gel seco e solvotermal. A
amostra obtida com 11 horas de cristalização, pelo método hidrotérmico, se
apresentou como a mais cristalina, havendo a manutenção da integralidade na
intensidade dos picos para tempos superiores. Para o método conversão de gel
seco, percebeu-se um aumento da cristalinidade com o passar do tempo,
comportamento similar às amostras sintetizadas pelo método hidrotérmico,
onde a cristalinidade do material aumentou até 11 horas, após esse período
havendo a manutenção do grau de cristalinidade do material, assim como o
método hidrotérmico. Para o método solvotermal, se percebeu um aumento da
cristalinidade com o passar do tempo, devido à conversão da magadiita em
ZSM-5, obtendo-se uma cristalinidade de 93% em 96 horas de cristalização.
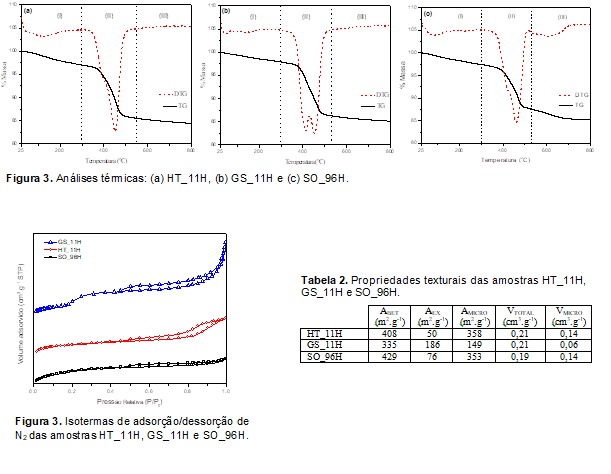
A Figura 3 (a), (b) e (c) exibem os resultados das análises de TG/DTG
realizadas nas amostras HT_11H, GS_11H e SO_96H, respectivamente. As curvas
de percentual de perda de massa e DTG apresentam perfis com comportamento
bastante semelhantes, apresentando, basicamente, três eventos de perdas de
massa. Podendo-se atribuí-los a: (I) de 25 °C – 300 °C, compreende a perda
de massa relacionada à eliminação da água fisissorvida (evaporação de grupos
hidroxilas ligadas fracamente às superfície); (II) a região entre 300 °C –
530 °C, corresponde a decomposição oxidativa de íons amônio provenientes do
agente direcionador de estrutura (ZANG et al., 2012); (III) acima de 530 °C
a perda de massa é decorrente do coque depositado sobre o catalisador gerado
durante a queima do direcionador.
A temperatura final da etapa de remoção do direcionador orgânico confirma
que a temperatura necessária para o tratamento térmico de calcinação
utilizada na metodologia desse trabalho está correta, pois a 550 °C
certamente todo o direcionador orgânico foi removido.
As variações de perda de massa e a faixa de temperatura associada aos
diversos eventos de decomposição das amostras HT_11H, GS_11H e SO_96H estão
indicadas na Tabela 1. Os resultados obtidos indicam que os índices de massa
residual apresentam similaridade entre os três métodos de síntese estudados
neste trabalho, corroborando que as zeólitas sintetizadas demonstram
estrutura de rede cristalina semelhante, corroborando os resultados obtidos
pelas as análises de DRX.
A Figura 4 apresenta as isotermas de adsorção- dessorção de nitrogênio sobre
as amostras HT_11H, GS_11H e SO_96H. De acordo com a classificação da
International Union of Pure and Applied Chemistry (IUPAC), essa medida
mostra que os materiais obtidos adsorvem o nitrogênio com uma combinação de
isoterma do tipo I, característico de adsorventes microporosos, com a do
tipo IV, característicos de sólidos mesoporosos com a presença de um loop de
histerese, que está relacionado com a formação de poros em formas de fenda
(SENAPATI, 2014).
A Tabela 2 apresenta os dados das propriedades texturais das amostras
HT_11H, GS_11H e SO_96H. Para todos os sólidos sintetizadas os valores da
área específica calculada pelo método BET foram elevadas, característicos
dos sólidos microporosos, o que está de acordo com valores relatados na
literatura para zeólitas do tipo ZSM-5 (CHENG et al., 2008) que comprovam a
eficiência dos métodos de síntese empregados neste trabalho. Em todas as
zeólitas, a presença de mesoporos caracterizados pelo loop de histerese nas
isotermas de adsorção-dessorção foi comprovada pelo pertinente volume de
mesoporos, o que concorda com a classificação da histerese observada na
Figura 3 (SILVA, 2004). Verifica-se que os materiais sintetizados pelos
métodos hidrotémico e solvotermal, apresentaram valores similares de áreas
externa, microporosa e volume microporoso, indicando que ambos possibilitam
a obtenção de sólidos com características de porosidade e, tão como,
possivelmente de tamanhos de cristais semelhantes, em contrapartida, o
método de gel seco proporcionou a obtenção de materiais com valores de área
e volume de microporos inferior e área externa superior, indicando a
formação de sólidos de cristais menores em relação aos outros métodos.
Conclusões
As amostras sintetizadas pelo método hidrotérmico e conversão de gel seco apresentaram tempos de cristalização mais curtos em comparação com o método solvotermal. Isto é, com apenas 11 horas de síntese as amostras já estavam aproximadamente 100% cristalinas, sem a presença de fases concorrentes. Enquanto, o método solvotermal só foi possível observar material sem a presença de fases contaminantes com 96 horas. As análises térmicas evidenciaram que os índices de massa residual apresentam-se próximos aos diferentes métodos de síntese estudados neste trabalho, corroborando que as zeólitas sintetizadas demonstram estrutura de rede cristalina semelhante confirmando com as análises de DRX. Para todos os métodos estudados, as isotermas de adsorção-dessorção de nitrogênio indicaram a obtenção de materiais com elevado valor de área superficial e volume de mesoporos, o que está de acordo com valores relatados na literatura para zeólitas do tipo ZSM-5 que comprovam a eficiência dos métodos de síntese empregados neste trabalho. Dessa forma, com base nos parâmetros discutidos nesse trabalho, a metodologia de síntese através do método hidrotérmico foi mais promissora em comparação com o método solvotermal e conversão de gel seco, apesar todos os métodos obterem a zeólita ZSM-5.
Agradecimentos
CNPq, UFAL, LSCat, ANP e FAPEAL.
Referências
ARGAUER, R. J.; LANDOLT, G. R. Characterization and environmental application of a Chilean natural zeólita. US Patent 3.702.886, 1972.
BAYATI, B.; BABALUO, A. A.; KARIMI, R. Hydrothermal synthesis of nanostructure NaA zeolite: The effect of synthesis parameters on zeolite seed size and crystallinity. Journal of the European Ceramic Society, v. 28, n. 14, p. 2653-2657, 2008.
CHEN, Yujing et al. Synthesis of ZSM-23 zeolite with dual structure directing agents for hydroisomerization of n-hexadecane. Microporous and Mesoporous Materials, v. 268, p. 216-224, 2018.
CHENG, Y. et al. Synthesis research of nanosized ZSM-5 zeolites in the absence of organic template. Journal of materials processing technology, v. 206, n. 1-3, p. 445-452, 2008.
ENGLERT, A. H.; RUBIO, J. Characterization and environmental application of a Chilean natural zeolite. International Journal of Mineral Processing, v. 75, n. 1-2, p. 21-29, 2005.
MURRELL, Lawrence L. et al. Method for making molecular sieves and novel molecular sieve compositions. U.S. Patent n. 6.004.527.21, 1999.
OZAWA, Kiyoshi et al. Hydrothermal Synthesis of Magadiite/Si‐ZSM‐11 Composites. Journal of the American Ceramic Society, v. 93, n. 12, p. 4022-4025, 2010.
RAZAVIAN, Marjan; FATEMI, Shohreh. Synthesis and application of ZSM-5/SAPO-34 and SAPO-34/ZSM-5 composite systems for propylene yield enhancement in propane dehydrogenation process. Microporous and Mesoporous Materials, v. 201, p. 176-189, 2015.
SANG, Shiyun et al. Difference of ZSM-5 zeolites synthesized with various templates. Catalysis Today, v. 93, p. 729-734, 2004.
SENAPATI, Soumya et al. Post-synthetic modifications of as-made zeolite frameworks near the structure-directing agents. Journal of Materials Chemistry A, v. 2, n. 27, p. 10470-10484, 2014.
SHINZATO, Mirian Chieko. Remoção de metais pesados em solução por zeólitas naturais: revisão crítica. Revista do Instituto Geológico, v. 27, n. 1-2, p. 65-78, 2007.
SILVA, A. O. S.. Síntese e Caracterização de Catalisadores de Ferro e Cobalto Suportados nas Zeólitas HZSM-12 e HZSM-5 para a Conversão de Gás de Síntese em Hidrocarbonetos. 2004. 229 f. Tese (Doutorado em Engenharia Química) – Centro de Tecnologia. Universidade Federal do Rio Grande do Norte, Natal.
SUZUKI, Yasuhiro et al. Cooperative effect of sodium and potassium cations on synthesis of ferrierite. Topics in Catalysis, v. 52, n. 1-2, p. 67, 2009.
SZOSTAK, Rosemarie. Molecular sieves. New York: Van Nostrand Reihold, 1998.
XU, Bing et al. Catalytic oxidative dehydrogenation of n-butane over V2O5/MO-Al2O3 (M= Mg, Ca, Sr, Ba) catalysts. Chinese Journal of Catalysis, v. 36, n. 7, p. 1060-1067, 2015.
XU, W.; DONG, J.; LI, J.; WU, F. J. Dry-gel conversion synthesis of Cr-MIL-101 aided by grinding: high surface area and high yield synthesis with minimum purification. Chemical Communications, v. 755, n. 225-242, 1990.
YILMAZ, Bilge; MÜLLER, Ulrich. Catalytic applications of zeolites in chemical industry. Topics in Catalysis, v. 52, n. 6-7, p. 888-895, 2009.
ZHANG, Ling et al. Organic template-free synthesis of ZSM-5/ZSM-11 co-crystalline zeolite. Microporous and Mesoporous Materials, v. 147, n. 1, p. 117-126, 2012.









