Atividade catalítica de líquidos iônicos anfifílicos derivados de surfactante na fixação química de CO[sub]2[/sub]
ISBN 978-85-85905-25-5
Área
Materiais
Autores
Vieira, M.O. (PUCRS) ; Monteiro, W.F. (PUCRS) ; Ligabue, R. (PUCRS) ; Einloft, S. (PUCRS)
Resumo
O CO2 é o gás de efeito estufa de maior impacto ambiental em termos de quantidades emitidas. A fixação do CO2 é um processo para agregar valor comercial a um gás residual. Líquidos iônicos podem ser utilizados de forma satisfatória na formação de ciclocarbonatos a partir de epóxidos e CO2. Baseado nisso, foram sintetizados dois líquidos iônicos anfifílicos derivado de surfactante: [bmim][C12ESO4] e [TBA][C12ESO4] para serem empregados na síntese do carbonato de propileno, carbonato de estireno, carbonato de glicidil isopropil éter e carbonato de epicloridrina. Em todos os casos, o cátion [TBA+] se mostrou mais eficiente em termos de conversão e seletividade. Para o carbonato de epicloridrina a conversão chegou a 79,5% com seletividade acima de 90% quando utilizado o [TBA][C12ESO4].
Palavras chaves
líquido iônico; ciclocarbonato; dióxido de carbono
Introdução
O CO2 é o gás de efeito estufa de maior impacto ambiental em termos de quantidades emitidas. Significativa parte desta contribuição vem de fontes antropogênicas causando inúmeras alterações climáticas (NOAA, 2019; IPCC, 2014). A conversão do CO2 é um processo atraente pois visa agregar valor comercial a um gás residual. Vários estudos de conversão de CO2 em ciclocarbonatos orgânicos usando líquidos iônicos (LIs) como catalisadores foram recentemente reportados na literatura (Vieira, et al., 2018; Vieira, et al., 2019). LIs são materiais versáteis pois além de serem considerados solventes verdes por substituem de maneira eficaz alguns solventes orgânicos tóxicos, despertam interesse para aplicações em diversos campos da Química, principalmente na área da catálise. Possuem propriedades particulares e projetáveis como estabilidade química e térmica, baixa pressão de vapor e alta condutividade iônica (Anthony, et al., 2005). O emprego comercial de LIs ainda é bastante limitado em função do alto custo para síntese destes materiais, por este motivo é fundamental o aprimoramento de estruturas de menores custos. Uma alternativa para isso é o emprego de surfactantes comerciais no ânion, diminuindo o valor do material e proporcionando propriedades anfifílicas. Ciclocarbonatos orgânicos podem ser obtidos a partir do CO2 com uma perfeita economia molecular. São materiais bastante utilizados industrialmente pois além de serem ótimos solventes polares, são precursores de diversos outros produtos. Neste contexto, o presente trabalho demonstra a atividade catalítica de dois líquidos iônicos, baseados em cátions já bastante conhecidos e ânion derivado de surfactante, ou seja, líquidos iônicos anfifílicos, como potenciais catalisadores na síntese do carbonato de propileno, carbonato de estireno, carbonato de glicidil isopropil éter e carbonato de epicloridrina a partir de seus respectivos epóxidos e CO2. Os líquidos iônicos utilizados neste trabalho foram: dodecil éter sulfato de butil metil imidazólio ([bmim][C12ESO4]) e dodecil éter sulfato de tetrabutilamônio ([TBA][C12ESO4]).
Material e métodos
A síntese dos líquidos iônicos dodecil éter sulfato de butil metil imidazólio ([bmim][C12ESO4]) e dodecil éter sulfato de tetrabutilamônio ([TBA][C12ESO4]), foi realizada segundo procedimento descrito na literatura (Bharmoria, et al., 2014; Vieira, et al., 2017). Os LIs foram caracterizados por FTIR, 1H-RMN, TGA e DSC. [bmim][C12ESO4]: FTIR (cm-1): 3158-3120, 2966, 2882, 1628, 1568-1459, 1282, 1215, 1170, 1019. 1H-NMR (600 MHz, DMSO-d6) δ (ppm): 9,11 [s, 1H]; 7,77 [d, 1H]; 7,70 [d, 1H]; 4,17 [t, 2H, J=6,8 Hz]; 3,78 [s, 3H]; 3,86 [t, 2H, J=15,7 Hz]; 3,54-3,41 [dt, 4H]; 1,82-1,70 [m, 2H, J=13,4; 7,5 Hz]; 1,47 [dt, 2H, J=12,8; 6,8 Hz]; 1,24 [s, 24H]; 0,93-0,79 [m, 6H]. TGA: 188 – 287 °C (perda de 8,6%), 293 – 435 °C (perda de 85,3%). DSC: TG = -70,0 °C; fusão = 4,1 °C; cristalização = 1,2 °C. [TBA][C12ESO4]: FTIR (cm-1): 2962, 2877 1280; 1216, 1023. 1H-NMR (600 MHz, DMSO-d6) δ (ppm): 3,79 [t, 2H]; 3,67 [t, 2H, J=6,0 Hz]; 3,49 [t, 2H, J=17,2 Hz]; 3,23-3,11 [m, 8H]; 1,58 [m, 8H]; 1,36-1,19 [m, 8H, J=5,8 Hz]; 0,94 [s, 26H]; 0,85 [t, 12H, J=6,1 Hz]. TGA: 223 – 376 °C (perda de 99,4%). DSC: TG = ND; fusão = -5,0 °C; cristalização = -12,2 °C. As carbonatações foram realizadas em um reator de aço de 120 cm3 equipado com agitação magnética e temperatura controlada. Para preparo dos ciclocarbonatos orgânicos foi utilizado 50 mmol de epóxido, 0,5 mmol de LI e 0,125 mmol de ZnBr2 como cocatalisador numa temperatura de 120 °C por 2 horas. As sínteses foram realizadas sem utilização de qualquer solvente adicional. Ao reator foi introduzido CO2 (30 bar) e aquecido. No término de cada reação, o reator foi resfriado e o gás remanescente removido lentamente. A separação do catalisador e produtos foi realizada por destilação simples. O carbonato final foi analisado utilizando um cromatógrafo gasoso Shimadzu GC - 14B equipado com um detector de ionização de chama (FID) e uma coluna DB - 5HT (15 m x 0,32 mm x 0,10 mm), utilizando acetofenona como padrão externo e éter dietílico como solvente.
Resultado e discussão
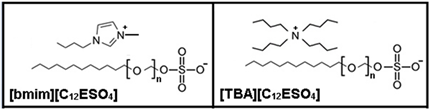
A estrutura dos líquidos iônicos sintetizados é mostrado na Figura 1.
A atividade catalítica do líquido iônico depende do cátion e do ânion
utilizado. No caso deste estudo, utilizou-se o mesmo ânion
([C12ESO4-]) nos dois LIs testados, alterando
somente o cátion ([bmim+] ou [TBA+]).
Avaliando o ânion escolhido, deve-se levar em consideração o grande volume que
ele ocupa, pois possui uma cadeia C12, além de uma série de
repetições do grupo (-O-CH2-). Além disso, grupo sulfato é uma base
fraca, o que beneficia este tipo de reação que requerem sítios básicos no
catalisador (Du, et al., 2005).
Na Tabela 1 é apresentado os resultados da influência do catalisador para a
síntese dos ciclocarbonatos orgânicos.
Não houve conversão sem a utilização de catalisador, assim como a utilização
de um cocatalisador é fundamental para obtenção de produto, pois ele atua como
ácido de Lewis. O cátion [TBA+] mostrou-se mais eficiente em todos
os diferentes carbonatos, apresentando resultados de conversão e seletividade
mais elevados quando comparada ao [bmim+]. O volume molecular do [TBA+
] leva ao afastamento do ânion, aumentando a distância entre eles. Como
consequência, uma menor interação eletrostática pode tornar o ânion mais
nucleófilo (Ju, et al., 2008), aumentando a atividade catalítica dele. Um
estudo
realizado por North e Pasquale, 2009, indica que o [TBA+] em alta
temperatura gera um produto de degradação, a trialquilamônia, que seria um
componente chave para o favorecimento de catálises que requerem sítios básicos
no catalisador, tornando assim, o [TBA+] mais eficiente que o
[bmim+].
Os melhores resultados de conversão e seletividade foram obtidos utilizando
glicidil isopropil éter e a epicloridrina. Estes epóxidos em geral, são mais
reativos que os contenho somente cadeia alquilíca. Além do mais, para melhores
resultados com óxido propileno, é necessário mais tempo reacional e o óxido de
estireno fornece um grande impedimento estéreo por conter um anel aromático,
dificultando as interações.
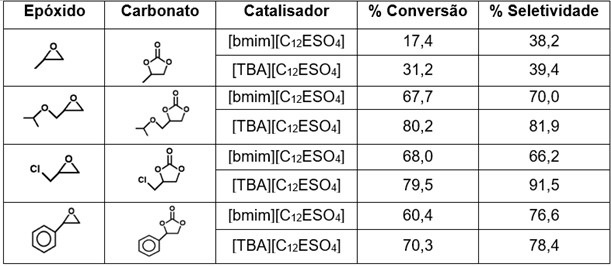
Condições reacionais: 50 mmol epóxido; 0,5 mmol LI; 0,125 mmol ZnBr2; T = 120 °C; P = 30 bar; t = 2 h.
Conclusões
A caracterização confirma a estrutura dos líquidos iônicos anfifílicos propostos e os resultados de conversão confirmam que eles podem ser utilizados como catalisadores na síntese de ciclocarbonatos. O ânion [TBA+] se mostrou mais eficiente todos testes. Para o carbonato de epicloridrina a conversão chegou a 79,5% com seletividade acima de 90% quando utilizado o [TBA][C12ESO4]. Este resultado é muito vantajoso, já que é proposto a síntese de um LI de ânion surfactante, cujo custo é significantemente menor, e nestas condições ele apresenta bons resultados catalíticos, havendo ainda possibilidade de melhora de resultados com a busca das melhores condições ideais de reação.
Agradecimentos
A CAPES pelas bolsas concedidas e a PUCRS pela infraestrutura.
Referências
ANTHONY, J.L.; ANDERSON, J.L.; MAGINN, E.J.; BRENNECKE, J.F. The Journal of Physical Chemistry B, v. 109, p. 6366-6374, 2005.
BHARMORIA, P.; MEHTA, M.J.; PANCHA, I.; KUMAR, A. The Journal of Physical Chemistry B, v. 118, p. 9890−9899, 2014.
DU, Y.; CAI, F.; KONG, D.L.; HE, L.N. Green Chemistry, v. 7, p. 518–523, 2005.
IPCC – Intergovernmental Panel on Climate Change. Mitigation of Climate Change, 2014.
JU, H.Y.; MANJU, M.D.; KIM, K.H.; PARK, S.W.; PARK, D.W. Journal of Industrial and Engineering Chemistry, v. 14, p. 157-160, 2008.
NOAA – National Organic & Atmospheric Administration. Trend in Atmospheric Carbon Dioxide – Mauna Loa, 2019.
NORTH, M.; PASQUALE, R. Angewandte Chemie, v. 121, p. 2990-2992, 2009.
VIEIRA, M.O.; MONTEIRO, W.F.; LIGABUE, R.; SEFERIN, M.; CHABAN, V.V.; ANDREEVA, N.A.; NASCIMENTO, J.F.; EINLOFT, S. Journal of Molecular Liquids, v. 241, p. 64-73, 2017.
VIEIRA, M.O.; MONTEIRO, W.F.; NETO, B.S.; CHABAN, V.V.; LIGABUE, R.; EINLOFT, S. Reaction Kinetics, Mechanisms and Catalysis, v. 126, p. 987–1001, 2019.
VIEIRA, M.O.; MONTEIRO, W.F.; NETO, B.S.; LIGABUE, R.; CHABAN, V.V.; EINLOFT, S. Catalysis Letters, v. 148, p. 108-118, 2018.









