ANÁLISE MORFOLÓGICA E MICROESTRUTURAL DE CRISTAIS FORMADOS NA SUPERFÍCIE DE ÁGUA SALINA DE DIFERENTES DENSIDADES TRATADAS POR DESCARGA DE PLASMA ATMOSFÉRICO
ISBN 978-85-85905-25-5
Área
Materiais
Autores
Almada, L.F.A. (UNIVERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO) ; Melo, V.R.M. (UNIVERSIDADE FEDERAL DO RIO GRANDE DO NORTE) ; Vitoriano, J.O. (UNIVERSIDADE FEDERAL DO RIO GRANDE DO NORTE) ; Fontes, K.E.S. (UNIVERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO) ; Fraga, F.E.N. (UNIVERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO) ; Junior, C.A. (UNIVERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO)
Resumo
Sob condições ainda desconhecidas, partículas de sais, chamadas Fleur del sel (flor de sal), podem se formar na superfície da água salina. A fim de estudar a morfologia e a microestrutura desses cristais em diferentes condições de densidade e sob influência de uma descarga de plasma atmosférico, amostras de água salina foram inseridas em recipientes plásticos e aquecidas a 40°C. A superfície foi exposta à temperatura ambiente, 25°C, e dividida em dois lados. Um lado foi submetido a uma descarga de plasma atmosférico. Os cristais formados foram coletados e estudados por MEV, DRX e análises químicas. O plasma atmosférico, além de promover a nucleação gerando uma maior massa e maior número de cristais menores, também provocou aumento na cristalinidade do material.
Palavras chaves
flor de sal; microestrutura; plasma atmosférico
Introdução
A cristalização de NaCl é bastante complexa, e tem sido estudada desde muitos anos atrás sob diferentes condições. Muitas pesquisas tem sido desenvolvidas a fim de identificar as formas de crescimento desses cristais, como a coexistência de crescimento nas formas {100} e {111} a partir de uma solução líquida, a cristalização a partir do resfriamento de uma solução saturada com diferentes gradientes de temperatura, em gotas e em diferentes substratos sujeito a agentes cristalizadores (DINO et al., 2009; CARLOS et al.,2002; SONIA et al., 2014; NOUSHINE et al, 2015). O método mais simples de obtenção de do sal é por meio da evaporação natural, em que à medida que a água circula por tanques, a salinidade aumenta até atingir 26°Bé (1,21g/cm³) e então é bombeada para os tanques cristalizadores. Nessa densidade inicia-se a precipitação do cloreto de sódio até atingir entre 28 a 29° Bé (1,23 a 1,24g/cm³), estágio em que a salmoura residual é descartada. Durante o aumento da densidade diferentes sais precipitam ao longo dos tanques, de modo que esses são misturas dos diferentes íons que compõe a água do mar (ROB, 2000; RENATO et al.,2012). Em condições ambientais bastante específicas e ainda desconhecidas dentro da cadeia produtiva do sal, ocorre o fenômeno de cristalização na superfície das águas presentes nos cristalizadores. Nas salinas os cristais formados na superfície dessas águas são chamados de flor de sal, são coletados e comercializados sem processamento. Além disso, possuem elevado custo (NOA, 2017; BHARAT et al.,2018). A nucleação, etapa inicial para formação de cristais, pode ser influenciada por diversos fatores, entre eles, uma solução saturada pode iniciar uma cristalização sob diferença de temperatura, presença de impurezas, choques mecânicos, diferenças de pressão etc (JOHN, 2001). Nesse aspecto, o plasma atmosférico tem sido estudado como um potencial agente sintetizador de nanopartículas através de interações plasma-líquido, em virtude das reações físicas e químicas envolvidas no processo (JAIRO et al.,2017; AKOLKAR et al., 2013; KURAKE et al., 2016). Neste trabalho, buscou-se estudar a morfologia, microestrutura e composição química dos cristais formados na superfície de salmoura sob condições controladas de temperatura e umidade sujeita a uma descarga de plasma atmosférico.
Material e métodos
Sugerindo que a principal causa da formação da flor de sal é a existência de um gradiente térmico associado às condições climáticas do ambiente, amostras de água salina foram coletadas na Salina Maranhão, pertencente ao grupo F.Souto Ind, Grossos-RN, e submetidas a uma diferença de temperatura e umidade média do ar de 50%. Enquanto a temperatura ambiente foi mantida a 25°C, a temperatura de uma chapa, Hotplate DB-IVAC, sob a qual foi posto um recipiente contendo a amostra da solução salina foi mantida a 40°C. Para realização do experimento foi utilizado um recipiente com dimensões 285 mm x 176 mm x 97 mm, material polietileno, contendo 2000mL de solução salina com densidade de 1,215g/cm³ e 1,232g/cm³. A superfície da solução foi dividida ao meio através de um cano de PVC, de 176 mm de comprimento, 15 mm de diâmetro e 1 mm de espessura. Um dos lados da superfície foi submetido a uma descarga de plasma atmosférico cuja configuração de tensão, 7kV, e frequência, 602 Hz, utilizada foi controlada por meio de um osciloscópio. A descarga foi gerada entre a ponta de uma agulha, utilizada como cátodo, e a superfície da solução com função de ânodo, sendo a distância entre eles de 1mm. Os cristais formados na superfície em cada lado foram coletados com o auxílio de uma peneira de material polimérico e postos para secar em filtros de papel qualitativo por 3 horas. Na etapa seguinte os cristais foram pesados e secos em uma estufa até que não houvesse mais variações na massa. Após secos, parte dos cristais foram diluídos em água deionizada e submetidos a análises químicas fotométricas, titulações e espectroscopia de absorção. Outra parte foi analisada por microscopia eletrônica de varredura, e difração de raios x. Os tamanhos dos cristais foram determinados por meio de do Software de tratamento de imagens, Image J. A análise de difração foi realizada em um foram realizadas em um difratômetro Shimadzu modelo XRD 6000, utilizando um tubo de radiação Cu - kα1, (20 kV, 30 mA). As amostras foram analisadas em ângulos de varredura de 20 – 80°, com passo de 0,02° e intensidades registradas por 0,6 s em cada passo. Os difratogramas foram caracterizados por meio do software Xpert HighScore Plus, e as fases foram quantificadas através de refinamento utilizando o método Rietveld por meio do software Maud - Materials analysis using difracction.
Resultado e discussão
Os cristais se formaram em ambos os lados da superfície, cresceram por cerca
de 6 horas e apresentaram diferenças significativas no tamanho e
aglomeração. A Figura 1 mostra imagens da microscopia eletrônica de
varredura e dados referente a densidade da solução no instante da coleta,
massa dos cristais, tamanho médio e composição química. As amostras a) e c)
apresentaram maior tamanho médio das partículas em relação às amostras
obtidas sem tratamento b) e d). O plasma atua como agente nucleador,
promovendo mudanças no processo de cristalização. Sua atuação gerou a
formação de um grande número de núcleos em comparação a superfície não
tratada e reduziu o crescimento dos cristais, de modo a gerar um maior
número cristais de tamanho menor. A diversificação dos tamanhos dos cristais
observada através dos desvios pode estar relacionada com a densidade e com o
plasma, em que para densidade maior o desvio foi menor em relação aos
cristais formados quando a solução possuía menor densidade. Enquanto isso as
soluções tratadas apresentaram maior desvio no tamanho médios dos cristais
em relação a não tratada. Ao aplicar uma descarga atmosférica sobre a
superfície de uma solução saturada, imediatamente cristais se formavam na
região próxima ao local da interação, por tanto a quantidade de núcleos
formados no local da descarga são bem maiores do que os formados na
periferia (JAIRO et al.,2017). Com relação a massa total de material obtido
nas duas condições, nota-se o aumento da massa tanto com o aumento da
densidade como em relação ao tratamento. Sendo importante observar que o
aumento percentual de massa para a densidade de 1,216g/cm³ foi de 16,28% com
o tratamento e para a solução de densidade de 1,232g/cm³ foi de 8,81%. A
composição química das amostras indicou uma maior mobilidade íons sódio,
cloro e potássio durante o experimento, tendo em vista a presença dessas
espécies em todas as amostras e considerando a presença dos outros íons na
solução utilizada. Tanto a atuação do plasma como o aumento da densidade
resultaram no aumento de sódio nas amostras, cerca de 13,82% para a amostra
A1 com o tratamento, 6,15 % para a amostra A2 com tratamento, e considerando
somete o aumento da densidade, 26,22%. Já o percentual de cloro reduz com o
tratamento e com a densidade, sendo a queda com o aumento da densidade mais
significativa, 41,79%. Os difratogramas das amostras apesentaram picos
correspondentes as fases de NaCl em sua grande maioria, com percentual acima
de 98%, tabela presente na Figura 2. As amostras A1T e A2NT apresentaram
pouca contaminação pela presença de K2SO3 desencadeada
tanto pela alteração da densidade da amostra como pela descarga de plasma
para formação da amostra A1. Percebe-se que nas amostras obtidas com o
tratamento houve aumento da cristalinidade pelo aumento na intensidade dos
picos observadas na Figura 2 a) e b). Na Figura 2 c) a amostra de menor
densidade apresenta maior cristalinidade, indicando redução desta com o
aumento da densidade. Além disso, nota-se a inversão do plano preferencial
de crescimento quando a densidade é maior, no entanto com a descarga de
plasma a microestrutura é orientada para o mesmo plano preferencial que as
demais amostras, Figura 2 d).

MEV (ampliação 30X, SE), dos cristais obtidos sem tratamento, NT, e com tratamento, T, para diferente densidades, A1 e A2 e análises físico-químicas.
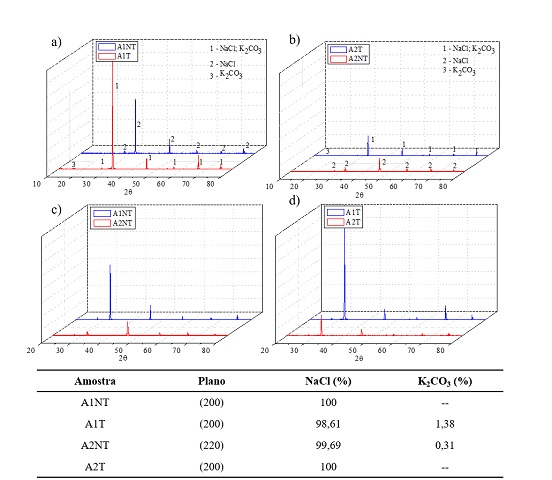
Comparativo do DRX das amostras e tabela contendo a quantificação das fases pelo método Rietiveld e planos preferenciais de crescimento dos cristais
Conclusões
A metodologia utilizada permitiu obter cristais de flor de sal a partir da superfície da solução, bem como observar que a descarga de plasma e a densidade são fatores que reduzem o tamanho do cristal e aumentam a massa de flor de sal. A composição química das amostras indicou o plasma e a densidade da solução como fatores influenciadores na redução de íons cloro e aumento de sódio. Além disso foi possível notar que o plasma promove orientação no crescimento dos cristais e aumento da cristalinidade. A flor de sal se mostrou um material de elevada pureza, até mesmo para aquela cuja água já se encontra nas condições de descarte. O plasma se mostrou um mecanismo imediato de nucleação de cristais para uma salmoura, sugerindo seu uso para estudo em aplicações mais especificas de cristalização.
Agradecimentos
Os autores agradecem ao Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPQ-430863 / 2016-0) e ao Instituto Nacional de Engenharia de Superfícies (CNPq-465423 / 2014-0).
Referências
AKOLKAR R, SANKARAN RM. Charge transfer processes at the interface between plasmas and liquids. Journal of Vacuum Science & Technology A: Vacuum, Surfaces, and Films. 2013.
BHARAT H, TEJASWINI D, ABHISHEK D, RHEA B, PUSHPITO K.G. Channelizing the osmotic energy of proximate sea bittern for concentration of seawater by forward osmosis under realistic conditions to conserve land requirement for solar sea salt production. Journal of Membrane Science, Vol. 567 n°1, December 2018, pp 329-338.
CARLOS R.N, LUCIA L.F, ERIC D, EDUARDO S. Effects of ferrocyanide ions on NaCl crystallization in porous stone. Journal of Crystal Growth, Vol.243, n° 3–4, September 2002, pp 503-516.
DINO A, LINDA P, MARCO B, MARCO R.{1 0 0} and {1 1 1} forms of the NaCl crystals coexisting in growth from pure aqueous solutiom. Journal of Crystal Growth, Vol.311,n° 2, January 2009, pp 399-403.
JAIRO B.F.O.B, CAMILA S.P, INGRID A.G, JUSSIER O.V, CLODOMIRO A.J. Sodium Chloride Crystallization by Electric Discharge in Brine. Materials Research, Vol.20, supl.2, São Carlos, 2017.
JOHN W.M.Crystallization, 4ºed. Butterworth-Heinemann, May 2001, pp 181. ISBN: 9780080530116.
KURAKE N, TANAKA H, ISHIKAWA K, NAKAMURA K, KAJIYAMA H, KIKKAWA F. Synthesis of calcium oxalate crystals in culture medium irradiated with non-equilibrium atmospheric-pressure plasma. Applied Physics. Express. 2016.
NOA S.L. Comparative analysis of traditional solar saltworks and other economic activities in a portuguese protected estuary. Bol. Investig. Mar. Costeras, 2017, Vol.46 n°1.
NOUSHINE S, MARTHE F.L.S, JULIE D, MARC P, DANIEL B. Salt stains from evaporating droplets. Nature - Scientific Reports, Vol.5, May 2015.
RENATO M.R, DIÓGENES F.S.C, MILTON A.L.F, RODOLFO M.B, DAVID H.M.M, ANTÔNIO M.A.S, CRISTIAN N.A, LAURO X.F. Brazilian solar saltworks - ancient uses and future possibilities. Aquatic Biosystems, April 2012.
ROB M.G. Sodium Chloride Crystallization, first ed. Encyclopedia of Separation Science, 2000, EUA, pp 4127-4134.
SONIA G, LEO P, KLAAS K. Crystallization behavior of NaCl droplet during repeated crystallization and dissolution cycles: An NMR study. Journal of Crystal Growth, Vol.391, n°1, April 2014, pp 64-71.









