Síntese, elucidação estrutural e avaliação da atividade hemolítica e bactericida de um novo derivado da amsacrina.
ISBN 978-85-85905-25-5
Área
Química Orgânica
Autores
Linhares de Locio, L. (UEPB) ; Suelleny de Caldas Nobre, M. (UEPB) ; Pamela Simoes do Nascimento, A. (UEPB) ; Leonel Silva Sousa, G. (UFRRJ) ; Albino Lima, S. (UEPB) ; Olimpio de Moura, R. (UEPB) ; Muriel da Silva, J. (UEPE) ; Barbosa Santos, M. (UEPB) ; Maria Sales de Medeiros e Silva, Y. (UEPB) ; Melo, C.O. (UFPB)
Resumo
Cerca de 10 milhões de pessoas morrem por doenças infeciosas. Este estudo tem o intuito de sintetizar, avaliar a atividade antimicrobiana e hemolítica de um derivado da ansacrina. Inicialmente foi sintetizado N-(acridin-9- l)tiazol-2-amina através da condensação do 2-amino-1,3,4-tiazol com a 9- dicloro-acridina. Foram realizados ensaios in vitro para avaliação antimicrobiana (por microdiluição em caldo) e ensaio de hemolise. Os resultados mostram que os compostos apresentam rota sintética viável, já que o compostos tiveram rendimentos satisfatórios (maior que 50%). Elucidação da molécula através de espectroscopia de infravermelho e RMN de 1H e 13C. Portanto, nessa pesquisa foi possível sintetizar uma molécula inédita e avaliar sua atividade hemolítica e atividade antibacteriana.
Palavras chaves
hibridação molecular; atividade antibacteriana; atividade hemolitica
Introdução
Desde que Wohler sintetizou a ureia em 1828, a síntese orgânica teve grande evolução permitindo, assim, a síntese de compostos completos de forma mais eficiente. Nesse sentido, a síntese de análogos, isômeros, isósteros ou outros processos de modificação molecular, como a simplificação molecular, a latenciação, bioisosterismo, hibridização molecular, entre outros, qualificam a química medicinal como ferramenta para o desenvolvimento de estruturas cada vez mais ativas em sistemas biológicos (CERA; PANCOTE, 2012).Uma das estratégias de síntese de novas estruturas químicas usadas pela indústria farmacêutica é a hibridação molecular. Essa estratégia clássica é a conjugação de duas entidades químicas distintas a fim de se obter uma molécula nova com dois grupos farmacofóricos com atividades biológicas e, assim, ter uma eficácia maior em relação aos seus compostos de origem (ARAÚJO et al., 2015). As acridinas são conhecidas como compostos versáteis que possuem ampla variedade de atividade biológica, sendo usado como anticonvulsivantes, anti-hipertensivo, anti-inflamatório, antimaláricos, antileishmania e principalmente como antimicrobiano e antitumoral. (MAKHAEVA et al., 2017). Os derivados do tiazol, que apresentam amplo emprego na farmacologia sendo usado como antiviral, antitumoral, anti- hipertensiva, anticonvulsivante, anti-inflamatória, antioxidante, analgésica e com maior relevância como antibacteriano. (EL‐BEHAIRY, et al., 2014; DAS; SIKDAR; BAIRAGI, 2016). Nesse sentido este trabalho tem o intuito de sintetizar, avaliar a atividade antimicrobiana e hemolítica de um derivado da ansacrina.
Material e métodos
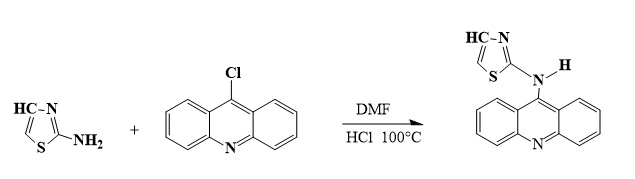
Para obtenção N-(acridin-9-il)tiazol-2-amina foi pela condensação do 2- aminotiazol com 9-cloroacridina na equivalência molar de 1:1, juntamente com ácido clorídrico (1 gota), usando como solvente o Dimetilformamida em 100°C. A reação foi acompanhada por cromatografia em camada delgada, usando hexano/acetato de etila (1:1) como a fase móvel. Após notar que os reagentes de partida não apareceram na placa cromatográfica decretou o fim da reação. Em seguida o precipitado formado foi filtrado, secado em temperatura ambiente, calculado o rendimento, ponto de fusão e elucidação estrutural através da espectrometria de infravermelha e ressonância magnética nuclear de carbono e hidrogênio. A atividade hemolítica dos compostos foi realizada em eritrócitos humanos frescos (tipo O-). As células foram lavadas três vezes em solução salina tamponada com fosfato e 100µl desta suspensão (1% hematócrito) e foi distribuído em cada cavidade de uma placa de 96 poços. Depois, com 100µl do composto sintetizado previamente dissolvido em uma solução tampão fosfato salino com 1% de DMSO. Foram testados em triplicata, adicionados à placa e incubadas durante 1 h. O ácido acético a 5% LT foi utilizado como droga hemolítica padrão. Após a incubação, as amostras foram centrifugadas (1500 rpm durante 10 min.), 100µl de cada sobrenadante será transferido para outra placa de microtítulo. A hemoglobina libertada foi monitorizada através da medição da absorbância a 540 nm num espectrofotómetro. A avaliação da ação bactericida do composto, foi testata frente as cepas das bactérias Staphylococcus aureus (ATCC25923) e Escherichia coli (ATCC25922) da Coleção pertencentes ao LaRMiCC da Universidade Estadual da Paraíba, determinando-se as concentrações inibitórias mínimas pelo método de microdiluição em caldo.
Resultado e discussão
O composto teve um rendimento satisfatório de 57,78%, o ponto de fusão não
foi identificado pois provavelmente é maior que 340ºC, o log P teórico foi
de 5,58. Sobre a solubilidade do teve boa solubilidade nos solventes:
dimetilformamida, dimetilsulfóxido, etanol e não foi solúvel
em água destilada, acetato de etila e hexano. Através da análise de
espectro de infravermelho do LLAC02 foi possível associar que a estrutura
sintetizada é a requerida, pois apresenta bandas características dos grupos
funcionais esperados. Primeiramente, observou-se uma banda de pequena
intensidade na região de 3200 cm-1 sugestiva de amina secundária. Foram
observados também bandas sugestivas de deformações axiais de C-H de
aromático entre 3092 e 3000 cm-1, assim como a presença de bandas C=C de
aromático nas regiões de 1590 a 1462 cm-1. Em 1626 cm-1 foi observado uma
banda sugestiva de grupo imina, além de bandas em 1348 cm-1 e 700 cm-
1sugestivas de ligações C-N e C-S, respectivamente. O espectro da RMN de 1H
(DMSO-d6, 400 MHZ) mostrou picos em δH 11,74 (s,1H) e 11,70 (s,1H) que
representam o hidrogênio da amina secundária e multipletos em δH 8,24 (m,
1H), δH 8,02 (m, 1H), δH 7,72 (m, 1H), 7,63 (m, 1H), δH 7,55 (m, 1H), δH
7,50 (m, 1H), δH 7,26 (m, 1H) 7,15 (m, 1H), referentes aos oitos hidrogênios
das posições 8,7,6,5,4,3,2,1 do núcleo acridínico, respectivamente. Na
análise do espectro de RMN 13C na técnica APT do N-(acridin-9-il)tiazol-2-
amina da observou a presença de todos carbonos da estrutura esperada,
destacando-se o sinal em δC 163,81, referente ao carbono amínico da posição.
No ensaio hemolítico observou que a composto teve 15,85% de hemólise na
concentração de 1000 µg mL-1 e a atividade bacteriana teve concentração
inbitoria mínima superior.

Conclusões
Nessa pesquisa conseguiu de sintetizar o N-(acridin-9-il)tiazol-2. Tendo o composto um rendimento satisfatório o que viabiliza a síntese. Determinou-se suas características físico-químicas. Como também foi possível elucidação completa da molécula através de espectroscopia de infravermelho e ressonância magnética de carbono e hidrogênio. O ensaio de hemólise sugeriu que o composto pode não ter toxicidade, porém é necessário outros tipos de ensaios para ter uma resposta final. O ensaio antimicrobiano mostrou que não teve atividade, provavelmente devido à dificuldade de solubilização da molécula.
Agradecimentos
Referências
ARAÚJO, C. R. M. et al. Desenvolvimento de fármacos por hibridação molecular: uma aula prática de química medicinal usando comprimidos de paracetamol e sulfadiazina e a ferramenta virtual Scifinder®. Química Nova, v. 38, n. 6, p. S1-S9, 2015.
CERA, T. P; PANCOTE, C.G. Planejamento de Fármacos. Revista Científica Unilago, p. 137-148, 2012.
DAS, D; SIKDAR, P; BAIRAGI, Mo. Recent developments of 2-aminothiazoles in medicinal chemistry. European journal of medicinal chemistry, v. 109, p. 89-98, 2016.
MAKHAEVA, G. F. et al. 9-Substituted acridinederivatives as acetylcholinesterase and butyrylcholinesterase inhibitors possessing antioxidant activity for Alzheimer's disease treatment. Bioorganic & Medicinal Chemistry, 2017.









