Planejamento, Síntese e Avaliação Biológica de Ftalimido-Tiossemicarbazonas com Atividade Anti-T.cruzi
ISBN 978-85-85905-25-5
Área
Química Orgânica
Autores
Santos, I.R. (UFRPE) ; Freitas, L.A.B. (UFPE) ; Gomes, P.A.T.M. (UFPE) ; Silva, V.G.M. (UFPE) ; Souza, F.A. (UFPE) ; Silva, G.C. (UFPE) ; Conceição, J.M. (UFPE) ; Santos, A.C.S. (FIOCRUZ-CPQAM) ; Pereira, V.R.A. (FIOCRUZ-CPQAM) ; Leite, A.C.L. (UFPE)
Resumo
A doença de Chagas é causada pelo protozoário Trypanosoma cruzi, na maioria das vezes é transmitida por picada do inseto triatomíneo. Tem grande incidência na América Latina. O fármaco atualmente utilizado não é eficaz nas fases mais agudas da doença. Diante da problemática, foi planejada, sintetizada e avaliada atividade anti-Tcruzi frente a forma tripomastigota do parasita uma série de 8 compostos. Foram identificados os produtos a1, a2, b2, c2 e d2 com promissores valores de IC50 em unidade micromolar, entre 3,60 e 22,44. Sendo estes menores que o apresentado pelo fármaco de referência benzonidazol. Foram encontrados altos valores de IS, em destaque d2 (IS=62,22). Os resultados foram promissores tendo em vista a potencial atividade tripanocida dos compostos.
Palavras chaves
Ftalimida; Tiossemicarbazonas; Doença de Chagas
Introdução
A doença de Chagas, causada pelo protozoário Trypanosoma cruzi, destaca-se entre o conjunto das doenças negligenciadas. No mundo é estimado que cerca de 6 a 7 milhões de pessoas estejam infectadas com T.cruzi. A maior incidência desta doença se dá na América Latina (WHO, 2019). É transmitida ao humano através de ingestão de alimentos contaminados, ou picada do inseto triatomíneo (barbeiro), quando este está infectado. No Brasil, de 2000 e 2013, as maiores incidências da doença na fase aguda se apresentaram na região Norte, ocorrendo surtos (BRASIL, 2015). O contágio pode se dar através de contato das fezes do inseto com a corrente sanguínea ao coçar o local da picada, contato das mãos infectadas com olhos ou boca, ou ingestão de alimentos contaminados. O controle de vetores é necessário para prevenção (WHO, 2019). O tratamento é feito através da ministração do medicamento benzonidazol. Porém, a eficácia do fármaco é diminuída nos casos mais graves (BRASIL, 2015). Tendo em vista a necessidade de desenvolvimento de novos medicamentos para o tratamento a sua terapêutica, objetivamos a produção de moléculas promissoras com potencial atividade anti-T.cruzi frente a forma tripomastigota do parasita. Ftalimidas e tiossemicarbazonas são grandes alvos de estudo, por serem reconhecidas na literatura como estruturas privilegiadas. Nosso grupo de pesquisa tem desenvolvido uma série de compostos ftalimido-tiazois que apresentaram efeitos potenciais contra o T. cruzi (GOMES et al., 2016). Há registros na literatura de tiossemicarbazonas com atividade Anti-T.cruzi (AGUIRRE et al., 2004). Séries de tiossemicarbazonas anteriormente desenvolvidas por nosso grupo de pesquisa, também apresentaram promissora atividade anti-T.cruzi(ESPÍNDOLA et al.,2015).
Material e métodos
A síntese dos compostos foi realizada em três etapas. Na primeira foi a síntese da ftalimida, esta foi obtida como primeiro intermediário. Na segunda etapa raegiu-se o primeiro intermediário com quatro diferentes acetofenonas alfa-halogenadas, obtendo-se quatro segundos intermediários (ftalimido-acetofenonas) com distintos substituintes no anel. Na terceira etapa reacional reagiu-se cada um dos intermediários dois com duas diferentes tiossemicarbaziadas, que variaram na substituição do nitrogênio da amina final, com H e Ph. Obtendo-se como produtos finais 8 ftalimido-tiossemicarbazonas distintas. A avaliação anti-T.cruzi foi realizada frente a forma tripomastigota do parasita, obtendo-se os valores de concentração de inibição (IC50). As formas tripomastigotas (cepa Y) foram semeadas em condições pré estabelecidas a placas de 96 poços, juntamente com diferentes concentrações dos compostos por 24h. O controle negativo foi obtido em poços sem tratamento e a droga de referência foi utilizada como controle positovo. Contados os parasitas em câmara de Neubauer, os valores obtidos foram submetidos a regressão linear simples utilizando o “softwere” Prisma 5.0 Graphpad, através do qual obteve-se os valores de IC50. Foram realizados também ensaios de citotoxicidade CC50 frente a células de linhagem macrofágica J774. Os macrófagos foram semeados em placas de 96 poços em meio condicional e atmosfera pré estabelecidos, incubados por 24h, e adicionados os compostos em diferentes concentrações para nova incubação por mais 48h. Também foi avaliada a atividade do benzonidazol. Após lida a absorbância, a partir da inibição da cultura, foi obtida a CC50 por meio de uma regressão linear simples utilizando o “softwere” Prisma 5.0 Graphpad.
Resultado e discussão
A estrutura química dos compostos sintetizados foi confirmada através de dados obtidos por espectroscopia de Ressonância Magnética Nuclear de Hidrogênio 1 (RMN 1H), espectroscopia de Ressonância Magnética Nuclear de Carbono 13 (RMN 13C ), e espectrometria de massas de alta resolução (EMAR). Os valores obtidos de Coeficiente de Inibição (IC50), Citotoxicidade (CC50) e Índice de Seletividade (IS), para os 8 produtos finais (Figura 1), estão descritos na Tabela 1. Todos em unidade micromolar. Foram de destaque os compostos que apresentaram valores de IC50 menores que o do fármaco de referência (14.60). Se mostraram promissores no grupo das ftalimido-tiossemicarbazonas do grupo 1 (a1,b1,c1 e d1) o composto a1, com valor de IC50 de 8,65. Para o grupo 2 (a2, b2, c2 e d2), se destacam todos os compostos em relação aos seus valores de IC50 , sendo 4,90, 3,75, 11,51 e 3,60 respectivamente. O composto d2 apresentou o maior índice de seletividade da série, se mostrando 68,22 vezes mais seletivo para o parasita na forma tripomastigota do que para células de mamíferos, sendo assim o mais promissor. Enquanto que o benzonidazol, nos ensaios apresentou um menor IS (6,58). De forma geral, frente ao tipo de células com as quais foram realizados os testes de CC50, a maioria apresentou índices maiores que o do fármaco de referência utilizado como controle, benzonidazol Tabela 1. Além disso, os baixos valores de IC50 obtidos, mostram que uma concentração menor dos compostos é necessária para inibição de 50% das cepas, e um maior IS com relação ao benzonidazol. Identificando nossos compostos como promissores em seletividade para os tripomastigotas na presença das células.
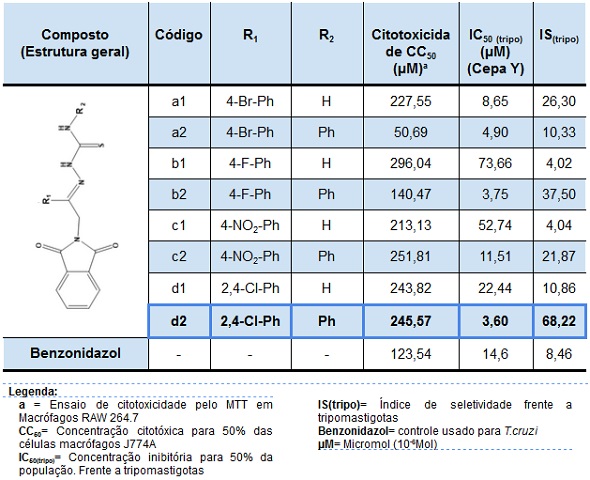
Resultados obtidos para atividade anti-T.cruzi das ftalimido-tiossemicarbazonas.
Conclusões
Após planejamento e síntese, comprovadas as estruturas, todos os compostos da série foram testados quanto sua atividade anti-Tcruzi. Os produtos a2, b2, c2, d2, a1, d1, apresentaram promisores valores de IC50 em unidade micromolar entre 3,60 e 11,51, menores que o do bezonidazol. Os altos valores de IS, em destaque o d2 (IS=62,22), encontrados na maioria dos compostos sintetizados, mostram que nossos compostos oferecem um direcionamento mais eficiente para o parasito do que para as células de mamíferos, o que os torna bastante promissores tendo em vista sua propriedade tripanocida.
Agradecimentos
A UFPE,em especial o laboratório LpQM e a Central Analítica do DQF. A Fiocruz-CPqAM. Ao CETENE. Ao CNPq. A CAPES pelo financiamento através de bolsa de mestrado.
Referências
AGUIRRE, G.; BOIANI, L.; CERECETTO, H.; FERNÁNDEZ, M.; GONZÁLEZ, M.; DENICOLA, A.; OTERO, L.;GAMBINO, D.; RIGOL, C.; OLEA-AZAR, C.; FAUNDEZ, M.; In vitro Activity and Mechanism of Action Against the Protozoan Parasite Trypanosoma cruzi of 5-nitrofuryl Containing Thiosemicarbazones; Bioorganic & Medicinal Chemistry; v.12, 4885–4893, 2004.
BRASIL, Ministério da Saúde - Secretaria de Vigilancia e Saúde. Doença de Chagas aguda no Brasil: série histórica de 2000 a 2013; Boletim Epideiológio, vol 46,nº 21, 2015.
ESPÍNDOLA, J. W. P.; CARDOSO, M. V. O.; OLIVEIRA FILHO, G. B.; SILVA, D. A. O.; MOREIRA, D. R. M.; BASTOS, T. M.; SIMONE, C. A.; SOARES, M. B. P.; VILLELA, F. S.; FERREIRA R. S.; CASTRO, M. C. A. B.; PEREIRA, V. R.; MURTA, S. M. F.; SALES, J. P. A.; ROMANHA, A. J.; LEITE, A. C. L.; Synthesis and structure-activity relationship study of a new series of antiparasitic aryloxyl thiosemicarbazones inhibiting Trypanosoma cruzi cruzain; European Journal of Medicinal Chemistry , nº 101, 818- 835, 2015.
GOMES, P. A. T. M. OLIVEIRA, A. R.; CARDOSO, M. V. O.; SANTIAGO, E. F.; BARBOSA, M. O.; SIQUEIRA, L. R. P.; MOREIRA, D. R. M.; BASTOS, T. M.; BRAYNER, F. A.; SOARES, M. B. P.; OLIVEIRA, M. A. P.; CASTRO, M. C. A. B.; PEREIRA, V. R. A.; LEITE, A, C, L. Phthalimido-thiazoles as building blocks and their effects on the growth andmorphology of Trypanosoma cruzi; European Journal of Medicinal Chemistry, nº 111, 46-57, 2016.
WHO - World Health Organization; Chagas Disease (American trypanosomiasis); Disponível em:
http://www.who.int/mediacentre/factsheets/fs340/en/.; Acesso em: 16.08.2019









