SÍNTESE DE DERIVADOS DE CUMARINAS VIA REAÇÃO DE MANNICH E ATIVIDADE ANTIMICROBIANA COM BASE NA ANÁLISE POR COMPONENTES PRINCIPAIS
ISBN 978-85-85905-25-5
Área
Química Orgânica
Autores
da Silva, J.F. (UEG) ; Billegas, T.B. (UEG) ; Ribeiro, L. (UEG) ; Ramos, L.M. (UEG)
Resumo
As cumarinas podem ser obtidas por extração em plantas ou obtidas por síntese orgânica. Uma vasta gama de atividades biológicas, estão relacionadas às cumarina. Esses compostos, podem ser empregados como reagente de partida em reações de Mannich para formação de compostos β-aminocarbonílicos. Síntetizou- se a cumarina acetilada, que foi usada como reagente de partida na reação de Mannich. Diferentes catalisadores e quantidades (ácidos e bases de Lewis e Bronsted-Lowry) foram avaliados e o melhor rendimento foi usando 10 mol% de p- TsOH (84%). Usando solventes polares próticos e apróticos, o emprego do THF apresentou o rendimento mais satisfatório (84%). Foram avaliados a atividade antimicrobiana, confirmando a SAR dos compostos usando análise de PCA que justificaram a atividade biológica.
Palavras chaves
cumarinas; Mannich; PCA
Introdução
A síntese orgânica têm objetivado práticas cada vez mais sustentáveis com a adoção de medidas que se adequam dentro dos princípios da Química Verde. Destaca-se nesse contexto as reações multicomponentes (RMCs) que são reações em que três ou mais reagentes se combinam para obtenção um único produto final, o qual contém todos, ou grande parte dos átomos de carbono (MARQUES; BISOL; SÁ, 2012; ROGERIO et al., 2016). Dentre as RMCs, destaca-se as reações de Mannich (ALLOCHIO et al., 2013), em que os produtos apresentam amplas aplicações biológicas (SANKAPPA RAI et al., 2010). O emprego de cumarinas como reagente de partida em reações de Mannich é uma alternativa sintética. As cumarinas são heterocíclicos podem ser obtidas na sua forma natural, extraída de plantas, ou ainda serem obtidas por síntese. Inúmeras aplicações terapêuticas são atribuidas à essa classe, tais como: estimulante do sistema nervoso central, anti-inflamatória, antibacteriana, anticoagulante, dentre outros (MARQUES; SALLES; MAISTRO, 2015). Visto a importância dos derivados cumáricos e sabendo-se que alteração de grupos na estrutura de composto podem alterar sua atividade biológica, o presente estudo teve como objetivo sintetizar diferentes derivados por meio de uma otimização das condições de reação. Os derivados cumáricos foram submetidos à avaliação antimicrobiana para Staphylococcus aureus e a Escherichia coli. Utilizando estatística multivariada permitiu avaliar a qualitativamente a relação estrutura-atividade desses derivados, separando-as em dois grupos distintos, os derivados ativos e inativos frente às bactérias Staphylococcus aureus e Escherichia coli.
Material e métodos
Inicialmente foi sintetizado a 3-Acetil-2H-1-benzopiran-2-ona e após recristalização,foi utilizada como reagente de partida nas reações de Mannich. Iniciou-se então, a análise das melhores condições reacionais. Em um balão de fundo redondo foram adicionados: 3-Acetil-2H-1benzopiran-2-ona (1mmol), anilina (1mmol) e benzaldeído (1mmol), por rotação em 24 horas. Foram testados: i) Catalisadores: Diácido Imidazol, Nitrato de Cerium amoniacal, MAI.Cl-, p-TSOH, MSI e PEI+LI. ii) Solventes: apolares, polares proticos e apróticos. iii) quantidade de catalisador. iv) excesso de reagente. Todas as reações foram mantidas a temperatura ambiente. Os produtos foram filtrados, recristalizados e elucidados por técnicas espectroscopica.
Resultado e discussão
A otimização das condições reacionais ocorreram conforme o Esquema 01:
Utilizando variados catalisadores na síntese: sem catalisador (27%), MAI.Cl-
(34%), Diácido Imidazol (54%), (NH₄)₂[Ce(NO₃)₆](17%), p-TSOH (66%), MSI (27%) e
PEI+LI (57%). Observou-se que a catálise ácida usando o p-TSOH como catalisador
e na quantidade de 10 mol% p-TSOH (78%). No efeito do solvente, notou-se que o
THF (78%) e BMI.BF4 (75%) foram satisfatórios. Ao utilizar THF e BMI.BF4, o
excesso de cumarina favoreceu obtenção de quantidades estequiométricas. Essas
condições foram empregadas na sintese de derivados: aldeídos aromáticos,
cumarinas (acetilcumarina e N,N-4-dietilamino-acetilcumarina) e amina (anilina
e 4-nitroanilina). Os derivados foram submetidos à avaliação antimicrobiana.
Seis produtos apresentaram valores de CMI igual a 62,5 µg/mL para S. aureus
ATCC 29213 e sete produtos apresentaram valores de CMI igual a 62,5 µg/mL para
a E. coli ATCC 25312.
A obtenção da otimização da geometria desses derivados foram realizadas através
do programa Gaussian 09 com o nível M062XD/6-311++G9(d,p). Em termos dos
valores de CMI 50% foi feita uma análise de principal componente (PCA)
empregando a função prcomp do pacote stats no ambiente computacional R.
Os resultados de estatística multivariada são apresentados através de gráficos
de PCA.A Figura 1a mostra o gráfico das duas primeiras componentes principais,
em destaque uma linha contínua vertical traçada, a partir da origem separa os
compostos azuis (ativos) dos vermelhos (inativos). A primeira PC (52,97%) os
ativos apresentaram valores positivos, contrastando com os inativos que
apresentam valores negativos, na mesma PC1. A Figura 1b mostra a separação em
ativas e inativas para a E. coli e o PC foi o responsável por 59,58% das
separações.
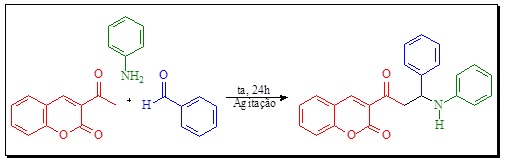
Representação da reação de Mannich usando acetil cumarina
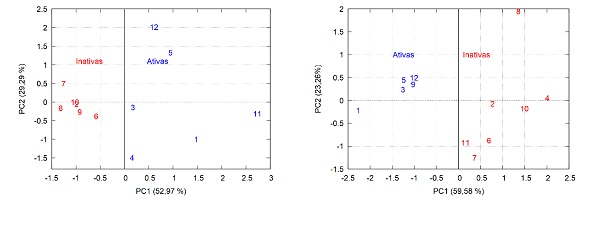
a) gráfico de escores para moléculas ativas e inativas para S. aureos; b) para E. coli.
Conclusões
Estabelecido as melhores condições, observou-se que o uso de p-TSOH 10mol% foi satisfatório, além do uso maiores quantidades de cumarina acetilada. Os derivados cumáricos apresentaram bons rendimentos e potenciais atividades biológicas frente à bactérias (CMI e CMB), o que permitiu determinar a atividade antibacteriana de sete produtos permitindo dizer que os produtos que apresentaram CMI dentro das concentrações testadas tem ação bacteriostática. A análise de componentes principais (PCA) dos produtos os separou em ativos e inativos frente as bactérias S. aureus e a E. coli
Agradecimentos
CNPq, FAPEG e UEG.
Referências
ALLOCHIO J. F. F.; FIOROT, R. G; DELARMELINA, M.; LACERDA, V. Jr.; dos SANTOS, R. B.; GRECO, S. J. Review Reação de Mannich: Metodologia Clássica na Formação de L. Carbono-carbono. Orbital: The Electronic Journal of Chemistry, v. 5, n. 2, p. 96–142, 2013.
MARQUES, E. DE S.; SALLES, D. B.; MAISTRO, E. L. Assessment of the genotoxic/clastogenic potential of coumarin derivative 6,7-dihydroxycoumarin (aesculetin) in multiple mouse organs. Toxicology Reports, v. 2, p. 268–274, 2015.
MARQUES, M. V.; BISOL, T. B.; SÁ, M. M. Reações multicomponentes de biginelli e de mannich nas aulas de química orgânica experimental. Uma abordagem didática de conceitos da química verde. Quimica Nova, v. 35, n. 8, p. 1696–1699, 2012.
ROGERIO, K. R.; KUMMERLE, F.; GRAEBIN, A. E.; STEPHAN, C. Multicomponent reactions: A brief history and their versatility for the synthesis of biologically active molecules. Revista Virtual de Quimica, v. 8, n. 6, p. 1934–1962, 2016.
SANKAPPA RAI, U.; SHETTY, A. M. I. P.; ISLOOR, N.; MALLADI, S.; FUN, H. K. Synthesis and biological evaluation of aminoketones. European Journal of Medicinal Chemistry, v. 45, n. 12, p. 6090–6094, dez. 2010.









