Síntese e avaliação da atividade antibacteriana e moduladora de chalconas nitro substituídas derivadas do produto natural 2-hidroxi-3,4,6-trimetoxiacetofenona
ISBN 978-85-85905-25-5
Área
Química Orgânica
Autores
Gomes Araújo, D.N. (UVA) ; Teixeira da Silva, P. (URCA) ; Sampaio de Freitas, T. (URCA) ; Esmeraldo Rocha, J. (URCA) ; da Cunha Xavier, J. (URCA) ; Ferreira Campina, F. (URCA) ; Douglas Melo Coutinho, H. (URCA) ; Magno Rodrigues Teixeira, A. (URCA) ; Nogueira Bandeira, P. (UVA) ; Silva dos Santos, H. (UVA)
Resumo
Foi realizado a avaliação da atividade antibacteriana e modulatória de duas novas chalconas obtidas a partir da 2-hidroxi-3,4,6-trimetoxiacetofenona com nitrobenzaldeídos, m- e p- substituídos. Elas foram sintetizadas por reações de condensação aldólica de Claisen-Schmidt em meio básico e caracterizadas por RMN de 1H, 13C e infravermelho. O potencial antibacteriano e modulador foi determinado a partir da concentração inibitória mínima frente as linhagens de Staphylococcus aureus (ATCC 25923; S.A.10) e Escherichia coli (ATCC 25992; E.C.06). As chalconas apresentaram valores de CIM≥1024 μg/mL. Os resultados da modulação com as cepas multiresistentes S.A.10 e E.C.06 indicam sinergismo da chalcona 2 associada a gentamicina e um efeito antagônico da chalcona 1 quando associada ao mesmo fármaco.
Palavras chaves
Chalconas; síntese; atividade antibacteriana
Introdução
A descoberta dos antibióticos, permitiu um grande avanço da medicina nos últimos oitenta anos (LAXMINARAYAN et al., 2015). Seu uso contribuiu para a redução da mortalidade infantil e aumento na expectativa de vida (BLAIR et al., 2014). No entanto, devido ao uso descontrolado de antibióticos e a evolução natural, muitos microrganismos patógenos têm adquirido resistência aos fármacos atualmente disponíveis, aumentado assim o número de infecções causadas por esses microrganismos (HOLMES et al., 2015). Nesse sentido, as chalconas e seus derivados tem sido alvo de inúmeros estudos com o intuito de descobrir novas substâncias que possam servir como alternativa no tratamento dessas enfermidades, seja substituindo os fármacos atualmente disponíveis ou como adjuvantes ao tratamento medicamentoso. Chalconas são compostos que possuem em sua estrutura fundamental os dois anéis aromáticos interligados por um sistema carbonílico α, β-insaturado de três carbonos conjugados (ROZMER, PERJÉSI, 2016). Seu vasto espectro de atividades está relacionado a reatividade da subunidade prop-2-em-1-ona α, β-insaturada e a infinidade de possibilidades de substituições nos anéis aromáticos A e B desses metabólitos, pela adição de diferentes grupos funcionais (ORLIKOVA et al., 2011; GUPTA, SINGH, GUPTA, 2017). O objetivo desse trabalho foi realizar a síntese de duas novas chalconas obtidas a partir da reação de condensação aldólica, em meio básico, entre o produto natural 2-hidroxi- 3,4,6-trimetoxiacetofenona com nitrobenzaldeídos, meta e para substituídos, e avaliar o potencial antibacteriano e modulador da resistência aos antibióticos ciprofloxacina, gentamicina e cefalexina, frente as linhagens padrão e resistentes das bactérias Staphylococcus aureus e Escherichia coli.
Material e métodos
As chalconas foram sintetizadas por reações de condensaçõa aldólica de Claisen-Schmidt, em meio básico, utilizando o produto natural 2-hidroxi- 3,4,6-trimetoxiacetofenona e os nitrobenzaldeídos. A acetofenona (0,88 mmol) foi solubilizada em etanol (10 mL) e, em seguida, acrescentou-se 10 gotas de hidróxido de sódio 50% deixando-se sob agitação por 2 minutos. Acrescentou- se a essa mistura 0.88 mmol dos nitrobenzaldeídos previamente dissolvidos em etanol. A reação foi mantida sob agitação magnética durante 24 - 72 horas, à temperatura ambiente e monitorada por cromatografia em camada delgada (CCD). Após o término da reação, a solução foi neutralizada e o precipitado formado foi filtrado e lavado com água destilada gelada. O produto formado foi avalidao por CCD e purificado por recristalização em etanol. Os espectros de RMN foram obtidos utilizando-se Espectrômetros de Bruker, modelo, Avance DPX – 300 e DRX-500 que operam na frequência de 300 MHz e 500 MHz para 1H, 75 MHz e 125 MHz para 13C. Os espectros de infravermelho foram obtidos no espectrômetro Perkin-Elmer, modelo 1000-FT. Os testes de atividade foram realizados no Laboratório de Microbiologia e Biologia Molecular (LMBM) da Universidade Regional do Cariri (URCA). Foram utilizadas linhagens padrão e resistentes das bactérias: Staphylococcus aureus ATCC 25923 e Staphylococcus aureus 10, Escherichia coli ATCC 25922, Escherichia coli 06. A concentração inibitória mínima (CIM) foi determinada pelo método de microdiluição em caldo. Para verificar a modulação do efeito antibacteriano dos antibióticos frente às cepas testadas, foi utilizado o método proposto por Coutinho et al. (2008), onde os antibióticos utilizados no teste foram ciprofloxacina, gentamicina e cefalexina, preparados na concentração inicial de 1024 μg/mL.
Resultado e discussão
As chalconas (E)-1-(2-hidroxi-3,4,6-trimetoxifenil)-3-(3-nitrofenil)prop-2-
en-1-ona (1) e (E)-1-(2-hidroxi-3,4,6-trimetoxifenil)-3-(4-nitrofenil)prop-
2-en-1-ona (2) foram sintetizadas por meio de reações de condensação de
Claisen Schmidt em meio básico (figura 1). Os rendimentos obtidos foram ≥
70% sendo considerados satisfatórios. As estruturas químicas dessas
substâncias foram elucidadas através da interpretação dos espectros de RMN
1H e 13C e infravermelho.
Ambas as chalconas apresentaram os valores de concentração inibitória mínima
CIM ≥ 1024 µg/mL para as linhagens bacterianas Staphylococcus aureus ATCC
25923 e Staphylococcus aureus 10, Escherichia coli ATCC 25992, Escherichia
coli 06, mostrando um valor de CIM clinicamente irrelevante frete as
linhagens estudadas.A figura 2 , mostra os resultados da avaliação da
atividade moduladora das chalconas 1 e 2 frente as cepas multirresistentes
S.A.10 e E.C.06. A concentração subinibitória CIM/8 dos antibióticos
associados ou não com as chalconas, frente ambas as bactérias apresentaram
um efeito inibidor significativo no crescimento das bactérias quando
comparadas com a gentamicina. Onde foi possível observar um sinergismo da
chalcona 2 associada a gentamicina e um efeito antagônico da chalcona 1
quando associada a este mesmo antibiótico.
Estudos com derivados de chalconas mostram que as mesmas apresentaram forte
atividade antibacteriana contra cepas Gram-positivas e Gram-negativas, onde,
a eficiência dessa atividade muda de acordo com os diferentes tipos de
substituintes e a localização em diferentes posições nos anéis aromáticos
(CHU et al., 2018). Além disso quando associadas a antibacterianos de uso
clinico a posição dessas estruturas também influencia na atividade (MORA;
CASTANO; JARAMILLO, 2014).
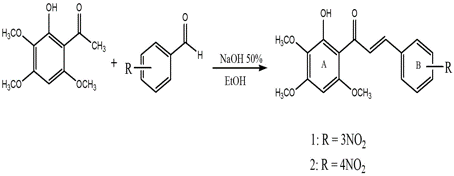
Reação de obtenção das chalconas

Concentração Inibitória Mínima (CIM) de antibióticos na presença e na ausência de chalconas 3-Nitro e 4-Nitro Staphylococcus aureus e Escherichia coli
Conclusões
As chalconas (E)-1-(2-hidroxi-3,4,6-trimetoxifenil)-3-(3-nitrofenil)prop-2-en- 1-ona (1) e (E)-1-(2-hidroxi-3,4,6-trimetoxifenil)-3-(4-nitrofenil)prop-2-en- 1-ona (2) foram obtidas com bons rendimentos por meio de reações de condensação aldólica. Com base na sensibilidade antibacteriana, as chalconas sintetizadas apresentaram valores de CIM ≥ 1024 µg mL-1. Para os testes de modulação, os resultados demostraram que a chalcona 2 apresentou efeitos sinérgicos quando associada ao aminoglicosídeo gentamicina, já a chalcona 1 quando associado ao mesmo antibiótico apresentou efeito antagônico.
Agradecimentos
Os autores agradecem a CAPES, CNPq e FUNCAP pelo apoio financeiro.
Referências
BLAIR, J. M. A.; WEBBER, M. A.; BAYLAY, A. J.; OGBOLU, D. O.; & PIDDOCK, L. J. V. Molecular mechanisms of antibiotic resistance. Nature Reviews Microbiology, v.13, p.42-51, 2014.
CHU, Wen-Chao et al. Synthesis and antibacterial evaluation of novel cationic chalcone derivatives possessing broad spectrum antibacterial activity. European journal of medicinal chemistry, v. 143, p. 905-921, 2018.
COUTINHO, H. D. M. et al. In vitro anti-staphylococcal activity of Hyptis martiusii Benth against methicillin-resistant Staphylococcus aureus: MRSA strains. Rev. bras. farmacogn. João Pessoa, v. 18, supl. p. 670-675, 2008.
GUPTA, J. K.; SINGH, S. V.; GUPTA, K. R. Chalcones: a review on synthesis, chemical properties and biological activities. Research Pharmaceutica, v.1, n. 2, p. 1-10, 2017.
HOLMES, A. H.; MOORE, L. S. P.; SUNDSFJORD, A.; STEINBAKK, M.; REGMI, S.; KARKEY, A.; GUERIN, P. J.; PIDDOCK, L. J. V. Understanding the mechanisms and drivers of antimicrobial resistance. The Lancet, v.387(10014), p.176-187, 2015.
LAXMINARAYAN, R.; MATSOSO, P.; PANT, S.; BROWER, C.; ROTTINGEN, J.-A.; KLUGMAN, K.; & DAVIES, S. Access to effective antimicrobials: a worldwide challenge. The Lancet, v.387(10014), 168-175, 2015.
MORA, C. L.; CASTANO, Julian; JARAMILLO, M. C. Inhibitory activity of dihydroxy-phenyl-propenone on betalactamase of Enterobacter cloacae: preliminary study for drug development to overcome bacterial resistance. Biomedica: revista del Instituto Nacional de Salud, v. 34, p. 114-123, 2014.
ORLIKOVA, B.; TASDEMIR, D.; GOLAIS, F.; DICATO, M.; DIEDERICH, M. Dietary chalcones with chemopreventive and chemotherapeutic potential. Genes & Nutrition, v. 6(2), p. 125-147, 2011.
ROZMER, Z.; PERJÉSI, P. Naturally occurring chalcones and their biological activities. Phytochemistry Reviews, v.15, n.1, p. 87-120, 2014.









