Comparação entre óxidos de zircônia magnéticos obtidos por duas rotas de síntese diferentes e sua aplicação na esterificação do ácido acético
ISBN 978-85-85905-21-7
Área
Química Verde
Autores
Duarte Mendes, M. (UNIVERSIDADE FEDERAL DE LAVRAS) ; Carolina Souza Andrada Anconi, A. (UNIVERSIDADE FEDERAL DE LAVRAS) ; Vilela Miranda, E. (UNIVERSIDADE FEDERAL DE LAVRAS) ; Lima Vieira, S. (UNIVERSIDADE FEDERAL DE LAVRAS) ; Ferreira Trindade, B. (UNIVERSIDADE FEDERAL DE LAVRAS) ; César Guerreiro, M. (UNIVERSIDADE FEDERAL DE LAVRAS)
Resumo
Entre os óxidos mais estudados como catalisadores heterogêneos destaca-se o óxido de zircônia. Este é o único óxido de metal que tem quatro propriedades químicas em sua superfície: propriedades ácidas, básicas, oxidantes e redutoras. O trabalho teve como objetivo a comparação entre dois materiais de óxido de zircônia magnética obtidos a partir de duas sínteses diferentes. Os materiais foram obtidos pela síntese de refluxo e sol-gel e foram caracterizados por análise de Espectroscopia vibracional na região do infravermelho. O teste catalítico foi feito no Cromatógrafo gasoso BID Tracera 2010, Coluna RTX-Wax,50 °C. Foi possível observar que os dois materiais apresentam espectros semelhantes e que o material produzido por sol-gel obteve uma maior conversão de reagentes em produto.
Palavras chaves
Catalisador heterogêneo; Òxido de Zircônia; Óxido de ferro
Introdução
Catalisadores podem ser divididos em catalisadores homogêneos e catalisadores heterogêneos. A diferença entre eles está na fase em que se encontram no meio reacional. Catalisadores homogêneos estão na mesma fase em que os reagentes, já os catalisadores heterogêneos estão em uma fase diferente dos reagentes. Quando o catalisador se encontra na mesma fase dos produtos, no caso os catalisadores homogêneos, são necessários custos extras com a sua recuperação e também para o tratamento dos efluentes gerados. Neste contexto, catalisadores heterogêneos podem ser promissores e ajudar nessas limitações da catálise homogênea (VYAS; VERMA; SUBRHAMANYAM,2010). Grandes esperanças são depositadas na aplicabilidade de catalisadores heterogêneos, porém para que eles sejam competitivos algumas características são desejáveis: (DABDOUB; BRONZEL, 2009): - Devem atuar em temperaturas moderadas e pressões baixas; - Devem ser 100% insolúvel no meio reacional e atuar de forma 100% heterogênea; - Devem ser reutilizáveis e de fácil separação; - Devem apresentar alta eficiência e atividade; - De preferência devem ser produto de fácil obtenção comercial Dentre os catalisadores heterogêneos, os óxidos metálicos apresentam grande potencial para catalisar diversas reações, uma vez que estes óxidos apresentam grande versatilidade, sendo fácil alterar a força dos sítios ácidos e básicos dos mesmos a fim de melhorar o desempenho nas reações, principalmente nas reações de esterificação (TEO,2016). Estes óxidos podem ser sintetizados a partir de alguns métodos como: co-precitação, sol-gel, combustão, refluxo. Mas para alguns desses tipos de síntese podem existir algumas desvantagens: necessidade constante de controle de pH, longo período de síntese e o uso de reagentes caros (HASHEMZEHI; SAGHATOLESLAMI; NAYEBZADEH, 2016). Entre os óxidos metálicos mais utilizados destaca-se a zircônia. O óxido de zircônia é o único óxido de metal que tem quatro propriedades químicas em sua superfície: propriedades ácidas e básicas e as propriedades oxidantes e redutoras. Além de ter alta estabilidade térmica e alta resistência a corrosão. Essas vantagens tornam materiais feitos a partir de zircônia, adequados para aplicações em materiais estruturais, células de combustíveis e catalisadores, sendo que sua grande aplicação é como catalisador ácido, podendo ser utilizado em reações de isomerização de isobuteno, craqueamento catalítico, alquilação e esterificação de ácidos graxos (TANABE; YAMAGUCHI, 1994; RUIZ-ROSAS,2011; GANAPATI, 1999; REDDY, 2009; VARTULI, 1999). O óxido de zircônia apresenta uma maior seletividade em relação a outros catalisadores ácidos, como a alumina, por exemplo. O que torna esse catalisador mais interessante para catalisar reações de esterificação. Além de catalisador, os materias de zircônia também podem ser utilizados como suporte catalítico (DENG; et al, 2008). A magnetização dos óxidos é uma alternativa interessante, já que facilita a separação do catalisador do meio reacional ao final da reação, fazendo com que o mesmo possa atuar em vários ciclos catalíticos.
Material e métodos
Na síntese por refluxo, o material foi produzido a partir da reação entre ZrOCl2.8H2O em solução (10 % m/m) e solução de NaOH 5 molL-1. A solução de oxicloreto de zircônia foi adicionada lentamente à solução de base, contendo 10% de óxido de ferro (Fe3O4) em relação à zircônia e etilenoglicol como dispersante, sob agitação constante a 100°C. A solução restante foi deixada em refluxo por 18 horas. Após as 18 horas, a suspensão resultando foi lavada com NH4NO3 até neutralização e calcinada em forno mufla a temperatura de 500°C por uma hora. O material foi nomeado ZMR. Na síntese por sol-gel foram adicionados acetilacetonato de zircônio e ácido cítrico nas proporções molares de 1:2 em um bécker contendo 50 mL de água deionizada. A temperatura foi elevada até 50°C para a dissolução do precursor de zircônia no ácido cítrico. Após a total dissolução, foi adicionada à mistura etilenoglicol na proporção molar de 1:2 em relação ao ácido cítrico e 10% de óxido de ferro em relação a zircônia. Elevou-se a temperatura até atingir 130°C para favorecer a esterificação. Houve a formação de uma resina. Na resina foram feitos dois tratamentos térmicos com atmosfera oxidante. No primeiro a resina foi calcinada até 300°C com taxa de aquecimento de 1°C/min, para favorecer a reação de pirólise, ficando nessa temperatura por duas horas. Depois o material foi calcinado até 500°C com taxa de aquecimento de 5°C/min, para o término da pirólise e cristalização dos sólidos, ficando nessa temperatura por 15 horas. O material foi nomeado ZMS. Os materiais foram caracterizados por análise de Espectroscopia vibracional na região do infravermelho. Os espectros foram obtidos em um espectrômetro Digilab Excalibur série FTS 3000, com faixa espectral de 400 a 4.000 cm-1 e resolução de 4 cm-1. As amostras foram preparadas em forma de pastilha de KBr. Foram feitos testes catalíticos no Cromatógrafo gasoso BID Tracera 2010, Coluna RTX-Wax, com temperatura 50 °C. Foi pesado 30 mg de cada material e inserido em um tubo de quartzo de 1/4 de polegada, acomodado em lã de vidro. O tudo com o material foi inserido em um reator de fluxo continuo com controlador de temperatura, sendo estas temperaturas de 60° a 150°C. Pelo material passou gás de arraste (He) em um fluxo de 40 mL/min e a mistura reacional de ácido acético e etanol 2:1, que é o reagente a ser convertido, com um fluxo de 1uL/min. Os possíveis produtos formados eram direcionados diretamente ao cromatógrafo gasoso acoplado ao reator realizando a separação e análise dos compostos formados no momento em que ocorre a reação, ou não, entre o material e o reagente.
Resultado e discussão
Pelos espectros de infravermelho obtidos foi possível observar que os
materiais apresentaram espectros de infravermelho semelhantes, com bandas
características de OH de hidratação na região de 3400 cm-1 e 1600 cm-1. Esta
última refere-se à deformação HOH coordenada ao material (PEREIRA, et al.,
2008). Em aproximadamente 1000 cm-1 há a formação de uma banda larga e
nítida devido a vibrações tridimensionais provavelmente Zr-O-Zr de
alongamento assimétrico (WANG, et al., 2014). No material sintetizado por
sol-gel a deformação dessa banda, pode significar que apesar da mesma
quantidade de óxido de ferro ser adicionada aos dois materiais, houve uma
maior incorporação de ferro nesse material do que no material produzido por
refluxo. O que pode significar que além da formação do núcleo magnético,
ainda houve uma dopagem do material com o ferro, maior no material
sintetizado por sol-gel do que o outro material (MARQUES,2015). Na região
entre 626 cm-1 e 400 cm-1 revela a presença de bandas de Zr-O. Mas a banda
correspondente ao estiramento Fe-O encontra-se perto de 480 cm-1. Como o
espectro do material produzido por refluxo mostra apenas uma banda larga
nessa região, pode ser devido à sobreposição das bandas de Zr-O e Fe-O. Esse
comportamento pode ser indício que não há fase segregada de ferro. Já o
espectro do material produzido por sol gel, há uma banda pequena perto de
500cm-1, o que pode significar que há fase segregada de ferro nesse
material. No cromatógrafo foi feita a curva analítica para o acetato de etila e
para o etanol nas mesmas condições apresentadas na metodologia para a mistura
reacional ácido acético e etanol 2:1. O valor do tempo retenção de cada um dele
é 3,7 min e 4,2 min. Esses picos podem ser observados nos cromatogramas obtidos
(gráfico 2) para os dois materiais sintetizados que atuaram como catalisadores
da reação entre ácido acético e etanol 2:1 no cromatógrafo. É possível observar
que a intensidade do pico do acetato de etila para os materiais MZS é maior do
que a intensidade do pico do acetato de etila para os materiais MZR. Isso
sugere que há uma maior conversão de ácido acético e etanol em acetato de etila
para os materiais sintetizados pelo método sol-gel. Para determinação dos
outros dois picos que aparecem no cromatograma seria necessária uma análise com
detector de massas.
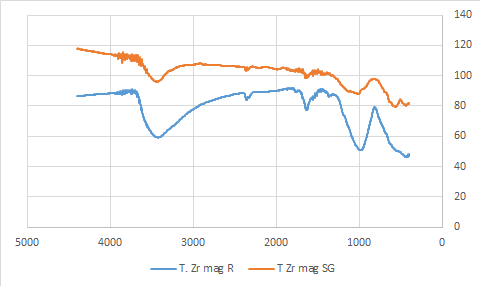
Espectro de infravermelho dos materiais obtidos pelo método de síntese de refluxo e pelo método de síntese sol-gel.
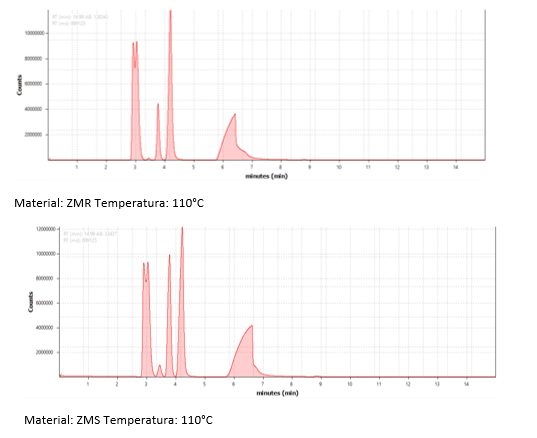
Cromatogramas obtidos para os materiais produzidos por síntese de refluxo e síntese sol-gel.
Conclusões
É possível concluir que os materiais de óxidos de zircônia magnéticos obtidos por duas rotas de síntese diferentes podem ser catalisadores da reação de esterificação do ácido acético e etanol em acetato de etila. É possível concluir também que o material produzido por sol-gel converteu uma maior quantidade de reagentes em produto.
Agradecimentos
FAPEMIG UNIVERSIDADE FEDERAL DE LAVRAS CAPQ
Referências
DABDOUB, J. M.; BRONZEL, L. J. Biodiesel: visão crítica do status atual e perspectivas na academia e na indústria. Química Nova, São Paulo, v. 32, n.3, p. 776-792, 2009.
DENG, X. Steam reforming of ethanol for hydrogen production over NiO/ZnO/ZrO2 catalysts. International Journal of Hydrogen Energy, vol. 33, pp. 1008-1013, 2008.
GANAPATI, D. Y.; YADAV, G.; NAIR, J. J. Sulfated zirconia and its modified versions as promising catalysts for industrial processes. Microporous and Mesoporous Materials, Amsterdam, v. 33, n. 1, p. 1-48, Dec, 1999.
HASHEMZEHI, M.; SAGHATOLESLAMI, N.; NAYEBZADEH, H. A study on the structure and catalytic performance of Zn x Cu 1− x Al 2 O 4 catalysts synthesized by the solution combustion method for the esterification reaction. Comptes Rendus Chimie, Iran, p. 1-8, 2016.
MARQUES, R. N. Zircônia modificada com ferro: caracterização e testes catalíticos.
P, A. L. C., et al. Effect of iron on the properties of sulfated zirconia. Applied Catalysis A: General, 334(1), 187-198, 2008.
REDDY, B. M.; PATIL, M. K. Organic Syntheses and Transformations Catalyzed by Sulfated Zirconia. Chemical Rewies. 109, 2185, 2009.
RUIZ-ROSAS, R. et al. Methanol decompostion on electrospun zircônia nanofibers. Catalysis Today, New York, 2011. In press.
TANABE, K., YAMAGUCHI, T. Acid-base bifunctional catalysis by ZrO2 and its mixed oxides. Catalysis Today, 20(2), 185-197, 1994
TEO, H. S. et al. Heterogeneous calcium-based bimetallic oxide catalyzed transesterification of Elaeis guineensis derived triglycerides for biodiesel production. Energy Conversion and Management, Malaysia, 2016.
VARTULI, J. C. et al. Characterization of the properties of tungsten/zirconia catalysts using adsorption microcalorimetry and n-pentane isomerization activity. Journal of catalysis, New York, v. 187, n. 1, p. 131- 138, Oct. 1999.
VYAS, A. P.; VERMA, J. L.; SUBRAHMANYAM, N. A review on FAME production processes. Fuel, London, v.89, n. 11, p. 1-9, Nov, 2010.
WANG, Q. et al. Synthesis of crack-free monolithic ZrO2 aerogel modified by SiO2. Journal of porous materials, v. 21, n. 2, p. 127-130, 2014.
































