Isolamento de triterpenos pentacíclicos em folhas de Jacaranda caroba
ISBN 978-85-85905-21-7
Área
Produtos Naturais
Autores
Pereira, N.R. (UFVJM) ; Silva, R.R. (UFVJM) ; Silva, I.M. (UFVJM) ; Bento, C.S.O. (UFMG) ; Oliveira, P.M. (UFVJM)
Resumo
As espécies do gênero Jacaranda apresentam uma vasta fonte de metabólitos secundários importantes, tendo em vista sua utilização como protótipos para o desenvolvimento de fármacos. A ausência de um amplo estudo químico da espécie Jacaranda caroba, direciona o presente trabalho a um estudo fitoquímico e taxônomico das folhas da espécie bem como o isolamento e elucidação estrutural dos seus constituintes. Foram isolados e identificados dois triterpenos com grande potencial farmacológico: ácido ursólico e ácido oleanólico.
Palavras chaves
Jacaranda caroba; triterpenos pentacíclicos; RMN
Introdução
O estudo no âmbito de produtos naturais tem um papel fundamental no Brasil. Sua vasta biodiversidade necessita de pesquisas científicas para seu melhor aproveitamento. Estudos que caracterizem e viabilizem a obtenção de novos fármacos são imprescindíveis já que segundo os dados da OMS, atualmente cerca de 80% da população mundial utiliza extratos de plantas ou de seus princípios ativos para promoção ou recuperação da saúde. A partir dessas considerações, dados etnobotânicos de espécies do cerrado brasileiro acompanhados de testes de prospecção fotoquímica, revelaram várias famílias com uma vasta fonte de metabólitos secundários bioativos, em particular, a espécie Bignoniaceae. Essa família constitui-se por aproximadamente 800 espécies de árvores lenhosas e arbustos, que podem ser agrupadas em 120 gêneros. Dentre os gêneros se destaca o Jacaranda. As espécies do gênero Jacaranda são nativas do continente americano e estão presentes, principalmente, na América do Sul e na América Central. São conhecidas 49 espécies desse gênero, constituindo principalmente de arbustos e árvores (MOSTAFA et al., 2014). As espécies dessa família apresentam atividades farmacológicas, tais como anti-inflamatória, antimicrobiana, antitumoral dentre outras (GACHET E SCHUHLY et al.; 2009; CHECKER et al.; 2012; FERRERES et al., 2013; RAJENDRAN et al., 2014). Assim, com base no êxito alcançado envolvendo estudos com plantas do gênero Jacaranda, e a ausência de estudos com Jacaranda caroba direcionou este trabalho para investigar fitoquimicamente e biologicamente as folhas desta espécie.
Material e métodos
O material botânico foi coletado na cidade de Diamantina- MG. Depositado no herbário da UFVJM (com exsicata ainda a ser catalogada). As folhas e caule foram secos em temperatura ambiente ao abrigo da luz solar. Em seguida, somente as folhas foram reduzidas a pó e submetidos à prospecção fitoquímica para identificação dos triterpenos. O material vegetal (folhas) da espécie em estudo foi submetido à extração a frio por maceração, com solventes de polaridade crescente, utilizando-se para isso hexano, clorofórmio e etanol, em média, 72 horas (REF), a amostra foi concentrada em rotaevaporador e secos até peso constante. A extração foi realizada em triplicata. O extrato clorofórmico foi submetido à cromatografia em coluna por via úmida, com solventes em ordem crescente de polaridade. Foram obtidas 172 frações que foram analisadas por cromatografia de camada delgada comparativa e as que apresentaram um perfil cromatográfico semelhante foram agrupadas. O sólido do grupo EC (47 mg) foi analisado por experimento de RMN1H e 13C.
Resultado e discussão
O processo de fracionamento empregado permitiu isolar a mistura de dois
triterpenos pentacíclicos. Do total da massa obtida para o extrato
clorofórmico bruto (149,2 g), obteve 28,4 g da mistura de natureza
triterpênica, sendo que estes se apresentam como sólidos cristalinos na cor
branca. A análise por CCD de sílica gel, utilizando vanilina perclórica como
revelador, evidenciou a existência de uma única mancha rosa, mesmo quando
testados em diferentes sistemas eluentes de mistura. O espectro de RMN de
13C é uma ferramenta bastante útil para distinguir triterpenos das séries
oleanano e ursano. Um dos fatores a serem considerados é o número de
carbonos não hidrogenados, seis nos ursanos e sete nos oleananos; nos urs-
12-enos o valor do deslocamento químico de C-12 encontra-se geralmente 2 ppm
mais afastado do TMS, e o de C-13 cerca de 5 ppm mais próximo do TMS, em
comparação com os sinais correspondentes em olean-12-enos. Portanto, nos
urs-12-enos os deslocamentos químicos de C-12 e C-13 encontram-se em torno
de δ 125 e δ 140, enquanto nos olean-12-enos estes deslocamentos encontram-
se em torno de δ 123 e δ 145, respectivamente (MAHATO; SEN, et al.; 1997).
Esta diferença se deve ao fato de que, na série ursano, o grupo metila em C-
19 está espacialmente próximo à dupla ligação, o que afeta os deslocamentos
químicos dos carbonos olefínicos, em relação àqueles da série oleanano, que
não apresentam o grupo metila em C-19 (VALADARES et al., 2009). Esta
variação nos deslocamentos químicos aparece como uma proteção γ em C-13 e
uma desproteção α em C-12 (DODRELL et al., 1974). Na série ursano, ocorre
efeito de desproteção β do grupo metila equatorial do C-19 sobre C-18. Nos
olean-12-enos, o sinal de C-18 encontra-se em torno de 11,5 ppm mais próximo
do TMS (valores em torno de δ 41,3 nos oleananos e δ 52,8 nos ursanos)
(MAHATO; KUNDU et al.; 1994). Com base nas atribuições anteriormente
discutidas, e comparação com dados da literatura, o ácido ursólico (3β-
hidróxi-urs-12-en-28-óico) foi identificado na mistura, mas em contrapartida
os demais deslocamentos observados não foram identificados como sendo o
ácido oleanólico. Contraditoriamente, nos estudos de VALADARES et al. (2009)
foram observados os sinais dos deslocamentos químicos de 13C, referente as
moléculas de ácido ursólico e oleanólico para a Jacaranda caroba.
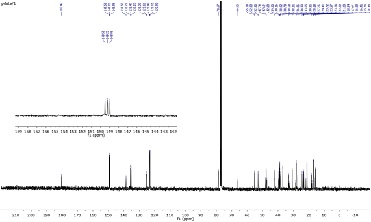
Espectro de RMN de 13C da mistura dos triterpenos pentacíclicos isolado da planta Jacaranda caroba em aparelho de 400 MHz, (CDCl3) e (C5D5N).

Foto da planta Jacaranda caroba.
Conclusões
O estudo inicial com as folhas da Jacaranda caroba evidenciou a partir de ensaios fitoquímicos a presença de triterpenos pentacíclicos, dos quais constituem 18,8% do extrato bruto clorofórmico. Outro aspecto positivo é a diferenciação da constituição química, onde foi possível constatar que indivíduos da mesma espécie, coletados em locais diferentes, produzem metabólitos diferentes. O novo composto já está sendo elucidado estruturalmente e será submetido a bioensaios para verificarmos se o mesmo trata-se ou não de um composto farmacologicamente ativo.
Agradecimentos
Os autores agradecem ao CNPq, à CAPES e à FAPEMIG.
Referências
DODRELL, D. M.; KHONG, P. W.; LEWIS, K. G. The stereochemical dependence of 13C chemical shifts in olean-12-enes and urs-12-enes as aid to structural assignment. Tetrahedron Letters, v. 27, p. 2381-2384, 1974.
FERRERES, F.; GROSSO, C.; GIL-IZQUIERDO, A.; VALENTÃO, P.; ANDRADE, P. B. Phenolic compounds from Jacaranda caroba (Vell) A. D. C.; Approaches to neurdegenerative disorders. Food Chem. Toxicol., 57, 91-98, 2013.
GACHET, M. S.; SCHÜHLY, W. Jacaranda – An ethnopharmacological and phytochemical review. J. Ethnopharmacol., 121 (1), 14-27, 2009.
GENTRY, A. H. Bignoniaceae – part II. (tribe Tecomeae). Flora Neotropica, 25 (2), 1992, 370p
MAHATO, S. B.; KUNDU, A. P. 13C NMR spectra of pentacyclic triterpenoids – acompilation and some salient features. Phytochemistry, v. 37, n. 6, p. 1517-1575,1994.
MAHATO, S. B.; SEN, S. Advances in triterpenoids research. Phytochemistry, v.44, n. 7, p. 1185-1236, 1997.
MOSTAFA, N. M.; ELDAHSHAN, O. A.; SINGAB, A. N. B.; The Genus Jacaranda (Bignoniaceae): An Updated Review. Phcog Commn., 4 (3) 31-39, 2014.
VALADARES, Y. M. Remijia ferruginea D.C., Jacaranda caroba D.C. e Solanum paniculatum L: fitoquímica, atividades biológicas e síntese de derivados dos ácidos ursólico e oleanólico. Tese (Doutorado em Ciências Farmacêuticas) – Faculdade de Farmácia, Universidade Federal de Minas Gerais, Belo Horizonte, 2009.
































