Óleo essencial de Backousia citriodora: influência na biossíntese de micotoxinas produzidas por Aspergillus flavus
ISBN 978-85-85905-21-7
Área
Produtos Naturais
Autores
Brandão, R.M. (UNIVERSIDADE FEDERAL DE LAVRAS) ; Cardoso, M.G. (UNIVERSIDADE FEDERAL DE LAVRAS) ; Batista, L.R. (UNIVERSIDADE FEDERAL DE LAVRAS) ; Camargo, K.C. (UNIVERSIDADE FEDERAL DE LAVRAS) ; Soares, L.I. (UNIVERSIDADE FEDERAL DE LAVRAS) ; Nogueira, J.O. (UNIVERSIDADE FEDERAL DE LAVRAS) ; Tourino, E.L.O. (UNIVERSIDADE FEDERAL DE LAVRAS) ; Lira, N.A. (UNIVERSIDADE FEDERAL DE LAVRAS)
Resumo
Os objetivos desta pesquisa foram caracterizar os constituintes químicos do óleo essencial de Backousia citriodora, avaliar a atividade antifúngica e aflatoxigênica sobre o Aspergillus flavus. A extração do óleo essencial foi realizada pelo método de hidrodestilação, sendo posteriormente analisados por GC/MS e GC/DIC. A atividade antiaflatoxigênica dos óleos (15,62; 7,81 e 3,90 µL mL-1) foi identificada por cromatografia em camada delgada. O constituinte majoritário encontrado no óleo essencial de Backousia citriodora foi o citral (100%). O óleo essencial inibiu 100% da produção de aflatoxinas B1 e B2 produzidas pelo fungo Aspergillus flavus na concentração de 15,62 µL mL-1, podendo ser considerado como promissor conservante de alimento e eficaz contra infecções de fungos e micotoxinas.
Palavras chaves
Aflatoxina B1; Aflatoxina B2; Produtos Naturais
Introdução
Os produtos naturais são utilizados pela humanidade desde a antiguidade, buscando alívio e ou cura de doenças, no controle de pragas e em mecanismos de defesa. Assim, os óleos essenciais, metabólitos secundários de plantas, possuem uma aplicabilidade em perfumaria, cosméticos e na conservação de alimentos, pois seus constituintes possuem diversas propriedades biológicas como antifúngica, antioxidante, antisséptica, antimicrobiana, anti- inflamatória, entre outras (SIMÕES et al., 2007). A espécie Backhousia citriodora, conhecida como murtão-limão, apresenta importantes constituintes biologicamente ativos que estão presentes em seu óleo essencial. Seu constituinte majoritário, citral, pode ser responsável em apresentar propriedades antifúngicas (LAZAR-BAKER et al., 2011). O controle da contaminação microbiológica é necessário, pois os fungos proporcionam risco à saúde humana por ter capacidade de produzir substâncias tóxicas denominadas micotoxinas. As micotoxinas são moléculas orgânicas produzidas como metabólitos secundários dos fungos. (RUYCK et al., 2015). As espécies do gênero Aspergillus, são as principais produtoras de micotoxinas. Esses fungos, geralmente, podem contaminar os produtos agrícolas no campo, durante o transporte e armazenamento. As toxinas produzidas por esses fungos entram na cadeia alimentar humana pela contaminação direta ou indireta de alimentos, podendo resultar em doenças crônicas e agudas (MILICEVIC; SKRINJAR; BALTIC, 2010). As aflatoxinas B1 e B2 são produzidas principalmente pela espécie Aspergillus flavus (ROCHA et al., 2014). Essas toxinas apresentam propriedades tóxicas, carcinogênicas e imunossupressoras, induzindo infecções nas pessoas que são contaminadas. O fígado é o principal órgão- alvo, causando danos hepáticos, quando aves, peixes e roedores ingerem alimentos contaminados por AFB1. Sendo essa a mais tóxica entre elas, causando efeitos diversos e, em alguns casos, podem ser letais para seres humanos e animais (FOOD INGREDIENTS BRASIL, 2009). Os objetivos deste trabalho foram caracterizar os constituintes químicos do óleo essencial de Backousia citriodora, avaliar a atividade antifúngica e o efeito do óleo essencial na biossíntese de aflatoxinas B1 e B2.
Material e métodos
Extração e composição química do óleo essencial: A extração do óleo essencial (OE) de folhas de B. citriodora foi realizada utilizando o método de hidrodestilação com aparelho de Clevenger modificado, acoplado a um balão de fundo redondo de 5 litros por um período de 2 horas (BRASIL, 2010). A identificação dos constituintes do OE foi realizada utilizando-se um cromatógrafo gasoso acoplado a um espectrômetro de massa. E a quantificação dos constituintes foi realizada por meio de normalização de áreas (%) utilizando-se um cromatógrafo gasoso com detector por ionização de chamas. Os constituintes foram identificados com base na comparação dos índices de retenção da literatura (ADAMS, 2007). Também foram utilizadas duas bibliotecas NIST107 e NIST21 do aparelho para comparação dos espectros. Efeito inibitório do óleo essencial sobre as espécies fúngicas: A análise do efeito inibitório do OE sobre o fungo A. flavus (CCDCA 10508) foi realizada utilizando o teste de difusão em disco aceito pelo Food and Drug Administration (FDA) e estabelecido pelo National Committe for Clinical Laboratory Standards (NCCLS). O inóculo (106 esporos mL-1) foi transferido para a placa contendo meio de Agar Extract Malt (MEA), pela técnica de espalhamento em superfície. Discos de papel-filtro de 5 mm de diâmetro embebidos com 10 μL do OE diluídos em dimetilsulfóxido (DMSO) nas concentrações de 500; 250; 125; 62,5; 31,25; 15,63; 7,81 e 3,91 µL mL-1 foram colocados sobre o meio de cultura, como sugerido por Karaman et al. (2003). O controle negativo foi o DMSO, e o controle positivo foi o fluodioxonil (2μL mL-1). As placas foram incubadas em BOD, a 25 °C, por um período de 72 horas e foram realizadas medições diametralmente opostas dos halos de inibição formados. A concentração inibitória mínima (CMI) é a menor concentração de OE em que ocorre a presença do halo de inibição. Influência do óleo essencial sobre a síntese de aflatoxinas B1 e B2: O efeito antiaflatoxigênico do OE foi avaliado por meio da inibição da produção de aflatoxinas B1 e B2 pelo fungo A. flavus (CCDCA 10508) em meio de cultura Yeast Extract Sucrose Agar (YES). O plaqueamento foi realizado inoculando-se 10 μL da suspensão de esporos (106 esporos mL-1) no centro da placa contendo 20 mL do meio YES adicionado do OE diluído em DMSO para obter as três concentrações abaixo da CMI, determinada em teste preliminar. Como padrão de comparação, 10 μL da suspensão de esporos foram adicionados à placa contendo apenas o meio. Todas as placas foram incubadas em BOD a 25°C, no escuro por um período de 10 dias. As Aflatoxinas B1 e B2 foram extraídas de acordo com o método de Passamani et al. (2014) e foram analisados por cromatografia em camada delgada (CCD). A fase estacionária utilizada foi uma placa metálica com cobertura de sílica em uma das fases, de dimensão 20 x 20 cm, e a fase móvel foi composta por tolueno: acetato de etila: ácido fórmico (60:30:10).
Resultado e discussão
A caracterização química dos constituintes do óleo essencial de
Backousia citriodora está apresentada na Tabela 1. Foram identificados dois
constituintes químicos no óleo essencial pertencentes à classe de
monoterpenos oxigenados.
Hayes e Markovic (2002), estudando o óleo essencial de Backousia
observaram que dentre os 9 constituintes presentes, o neral (40,9%) e o
geranial (51,4%) foram os de maior proporção. Observa-se que apesar do óleo
essencial obtido pelos autores citados apresentaram um número maior de
compostos que o presente trabalho, os constituintes majoritários foram os
mesmos apresentando porcentagens semelhantes.
A concentração mínima inibitória do óleo essencial de Backousia
citriodora foi de 31,25 µL mL-1 sobre o fungo A. flavus. Essa concentração é
aquela necessária para causar 100% de inibição do crescimento do micro-
organismo.
Pesquisas realizadas por Stévic et al. (2014) e Tian et al. (2012)
mostraram que as classes de compostos terpenos (monoterpenos e
sesquiterpenos) apresentam propriedades antimicrobianas contra vários micro-
organismos, dentre eles, os fungos. Essas substâncias proporcionam uma
toxicidade na estrutura e nas membranas celulares dos fungos, podendo
alterar a fluidez e a permeabilidade, interagindo com os componentes
internos das células. Essas ações contra os micro-organismos podem ser
explicadas a partir da característica lipofílica que os óleos essenciais
apresentam.
O efeito do óleo essencial sobre a inibição da produção de
aflatoxinas B1 e B2 por Aspergillus flavus estão representados na Figura 1.
Comparando-se o tratamento utilizado com o inóculo do fungo e com os padrões
de aflatoxinas B1 e B2.
Observando a Figura 1, que compara os padrões de AFB1 e AFB2 percebe-
se que há a presença das micotoxinas no inóculo do fungo A. flavus sem o
tratamento. Utilizando-se o tratamento com o óleo essencial de Backousia
citriodora, foi possível visualizar qualitativamente que apenas a
concentração de 15,62 µL mL-1 foi eficiente na inibição total da síntese
dessas toxinas. Visivelmente pode-se dizer que as concentrações abaixo
inibiram um pouco da produção de aflatoxinas B1 e B2.
Pandey, Sonker e Singh et al. (2016) observaram que o óleo essencial
de Lippia alba, apresentando como composto majoritário o citral (66,26%),
atua também na inibição total do crescimento micelial do Aspergillus flavus
a 0,28 µL mL-1 e na produção de aflatoxina B1 a 2 µL mL-1. Assim, sugere-se
que o composto citral pode ser o responsável pela atividade
antiaflatoxigênica do óleo essencial de Backousia citriodora.
Jerseck et al. (2014) as classes de terpenos encontrados nos óleos
essenciais proporcionam a inibição do crescimento e das micotoxinas
produzidas por fungos filamentosos. Por apresentarem vários compostos
bioativos, a atividade do óleo essencial não é atribuída apenas a um
mecanismo específico, mas a existência de vários alvos que podem atacar a
célula do fungo, podendo atribuir aplicação prática como inibidor da
produção de micotoxinas.
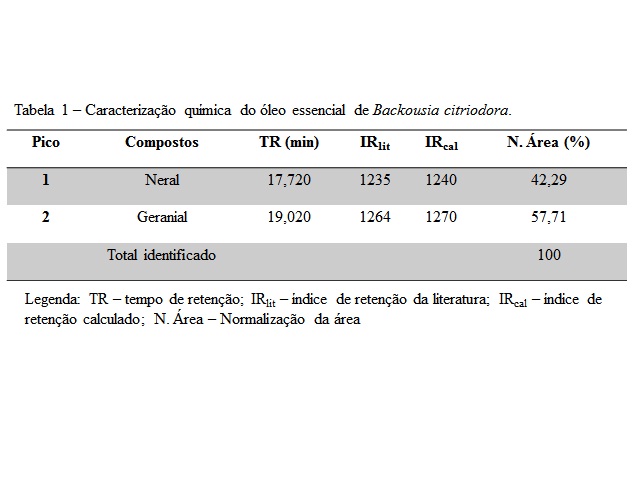
Tabela 1 – Caracterização química do óleo essencial de Backousia citriodora.
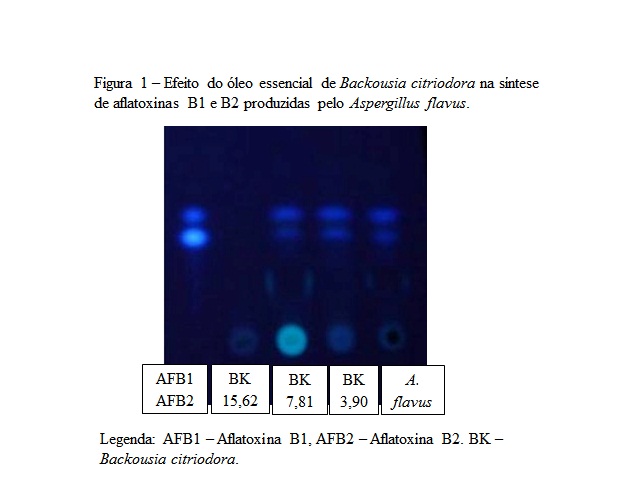
Figura 1 – Efeito do óleo essencial de Backousia citriodora na síntese de aflatoxinas B1 e B2 produzidas pelo Aspergillus flavus.
Conclusões
O óleo essencial de Backousia citriodora influenciou na síntese de aflatoxinas B1 e B2 porduzidas pelo fungo Aspergillus flavus, proporcionando inibição total da toxina na concentração de 15,62 µL mL-1.
Agradecimentos
Fapemig, CNPq, Capes e UFLA.
Referências
ADAMS, R. P. Identification of essential oils componentes by gas chromatography/ mass spectroscopy. 4th ed. Carol Stream: Allured, 2007. 804p.
Brasil. Agência Nacional de Vigilância Sanitária (ANVISA). In: Farmacopeia Brasileira, 1. (5th ed.). Brasília, 198-199, 2010.
FOOD INGREDIENTS BRASIL. As micotoxinas. Revista Oficial da Food Ingredients South America, n 7, p. 32-40, 2009.
HAYES, A. J.; MARKOVIC, B. Toxicity of Australian essential oil Backousia citriodora (Lemon myrtle). Part 1. Antimicrobial activity and in vitro cytotoxicity. Food and Chemical Toxicology, v. 40, n. 4, p. 535-543, 2002.
JERSEK, B.; ULRIH, N. P.; SKRT, M.; GAVARIC, N.; BOZIN, B.; MOZINA, S. S. Effects of selected essential oils on the growth and production of ochratoxin A by Penicillium verrucosum. Archives of Industrial Hygiene and Toxicology, Zagreb, v. 65, n. 2, p. 199–208, June 2014.
KARAMAN, I., SAHIN, F., GULLUCE, M., OGUTÇU, H., SENGUL, M., & ANDIGUZEL, A. Antimicrobial activity of aqueous and methanol extracts of Juniperus oxycedrus L. Journal of Ethnopharmacology, 85, 231-235, 2003.
LAZAR-BAKER, E. E. et al. Evaluation of commercial essential oil samples on the growth of postharvest pathogen Monilinia fructicola (G. Winter) honey. Letters in Applied Microbiology, Oxford, v. 52, n. 3, p. 227-232, Mar. 2011.
MILICEVIC, D. R.; SKRINJAR, M.; BALTIC, T. Real and perceived risks for mycotoxin contamination in foods and feeds: challenges for food safety control. Toxins, Basel, v. 2, n. 4, p. 572-592, Apr. 2010.
PANDEY, A. K.; SONKER, N.; SINGH, P. Efficacy of some essential oils against Aspergillus flavus with special reference to Lippia alba oil an inhibitor of fungal proliferation and aflatoxin B1 production in green gram seeds during storage. Journal of Food Science, v. 81, n. 4, p. M928-M934, 2016.
PASSAMANI, F. R.; HERNANDES, T.; LOPES, N. A.; BASTOS, S. C.; SANTIAGO, W. D.; CARDOSO, M. G.; BATISTA, L. R. Effect of temperature, water activity, and pH on growth and production of ochratoxin A by Aspergillus niger and Aspergillus carbonarius from Brazilian grapes. Journal of Food Protection, Des Moines, v. 77, n. 11, p. 1947–1952, Nov. 2014.
ROCHA, M. E. B.; FREIRE, F. C. O.; MAIA, F. E. F.; GUEDES, M. I. F.; RONDINA, D. Mycotoxins and their effects on human and animal health. Food Control, v. 36, n.1, p. 159-165, Feb. 2014.
RUYCK, K. D.; BOEVRE, M. HUYBRECHTS, I.; SAEGER, S. Dietary mycotoxins, co-exposure, and carcinogenesis in humans: Short review. Mutation Research, v. 766, p. 32-41, Oct./Dec. 2015.
SIMÕES, C. M. O., SCHENKEL, E. P., GOSMANN, G., MELLO, J. C. P., MENTZ, L. A., & PETROVICK, P. R. Farmacognosia: da planta ao medicamento. (6th ed.). Porto Alegre: UFSC/ UFRGS, 2007.
STEVÍC, T.; BERIC, T.; SAVIKIN, K.; SOKOVIC, M.; GODEVAC, D.; DIMKIC, I.; STANKOVIC, S. Antifungal activity of selected essential oils against fungi isolatedfrom medicinal plant. Industrial Crops and Products, v. 55, p. 116-122, Apr. 2014.
TIAN, J.; BAN, X.; ZENG, H.; HE, J.; CHEN, Y.; WANG, Y. The mechanism of antifungal action of essential oil from dill (Anethum graveolens L.) on Aspergillus flavus. Plos One, v. 7, n. 1, p. e30147, Jan. 2012.
































