Análise de tintura de Plantago sp de regiões do Espírito Santo por método cromatográfico, ESI-(-) FT ICR MS e seu potencial antioxidante
ISBN 978-85-85905-21-7
Área
Produtos Naturais
Autores
Souza, L.S. (UFES) ; Ferreira, P.S. (IFES) ; Kuster, R.M. (UFES) ; França, H.S. (IFES)
Resumo
A planta Plantago sp é empregada pela cultura popular como também foi inserida na lista RENISUS, criada pelo SUS, com o interesse de inseri-la como recurso terapêutico para a população. O objetivo desse trabalho foi analisar a composição química desta planta medicinal bem como sua atividade antioxidante. Os resultados mostraram evidências de compostos fenólicos e óleos essenciais através da Cromatografia em Camada Delgada, a presença de triterpenos, por ESI-(-)FT ICR MS, como o ácido ursólico e/ou ácido oleanólico, [M-H]- 455,35 e ácidos graxos como o ácido α-linoléico, [M-H]- 277,21. A atividade antioxidante foi determinada pelo método DPPH.
Palavras chaves
Plantago sp; composição química; antioxidante
Introdução
O Brasil, tanto quanto o Estado do Espírito Santo, possuem uma grande variedade de plantas medicinais, além de variabilidade climática, que pode afetar a produção dos metabólitos de suas plantas (GOBBO-NETO, 2007). A Plantago sp, popularmente conhecida como tansagem ou transagem, tem indicações, conforme a Anvisa (2011), anti-inflamatória e antisséptica da cavidade oral. Possui como princípios ativos componentes fenólicos (derivados de ácido cafeico), flavonóides, alcaloides e terpenóides, além de vitamina C e agentes anti- inflamatórios (LORENZI & MATOS, 2002), sendo estes responsáveis por suas indicações. Esta planta está inserida na Relação Nacional de Plantas de Interesse ao SUS (RENISUS) de modo a garantir a necessária segurança, eficácia e qualidade dos medicamentos, garantindo o acesso da população àqueles considerados essenciais (BRASIL, 2007). Desta maneira, o objetivo desse trabalho foi de analisar a composição química dessa planta medicinal colhida no Estado do Espírito Santo, em diferentes localidades, como também a avaliação da sua atividade antioxidante.
Material e métodos
A planta foi coletada em duas regiões do Estado do Espírito Santo, Jucuruaba e Vargem Alta, entre os meses de março a julho de 2014. As folhas foram secas em estufa à temperatura de 40ºC por 48 horas, conforme orientação de Brasil (2011). As plantas secas foram trituradas e pesadas para obtenção de tinturas etanólicas, com etanol a 96%, preparadas numa proporção de 10% (m/v). Foi feita a determinação de resíduo seco, conforme Brasil (2010). Para a CCD, utilizou-se placas de gel de sílica 60 ALUGRAM® Xtra SIL G/UV254. O sistema de solvente usado para flavonóides foi acetato de etila:ácido fórmico:ácido acético glacial:água (100:11:11:26,v/v) e para óleos essenciais, tolueno:acetato de etila (93:7,v/v). O revelador para flavonóides partiu de NP, 1% em metanol, e PEG 4000, 5% em etanol. Os padrões usados foram Isoquercetina, Hyperosídeo, Quercetina e Quercetrina. O revelador usado para óleos essenciais partiu da Vanilina sulfúrica (SR) (1% de Vanilina e 10% de Ácido Sulfúrico concentrado). Após a revelação, as placas foram aquecidas a 105ºC por 10 minutos até o aparecimento das manchas (WAGNER e BLADT, 1996). Para a técnica FT-ICR-MS, as tinturas foram analisadas por infusão direta a uma taxa de fluxo de 5 µL.min-1 para a fonte de electrospray no modo negativo de aquisição de íons (ESI(-)). O tempo de acumulação de íons foi de 5.10-4 s, sendo que cada espectro foi adquirido pela acumulação de 32 scans com um domínio de tempo de 4 mega-point (COSTA et al., 2014). A atividade antioxidante foi avaliada por meio da reação de redução do radical livre 2,2-difenil-1-picril-hidrazila (DPPH). Foram preparadas soluções metanólicas das tinturas e do padrão ácido ascórbico em sete concentrações: 10%, 5%, 2,5%,1,25%; 0,62%; 0,31%; 0,15%.
Resultado e discussão
A tansagem de Vargem Alta apresentou o maior teor de resíduo seco, 1,38% e a de
Jucuruaba, 0,7%, sendo o mínimo de referência de 1,2%, pela Farmacopeia
Francesa. O perfil químico mostrou uma grande diferença entre as amostras
coletadas. A planta de Jucuruaba apresentou manchas azuis com Rf de 0,60. Na
amostra de Vargem Alta, manchas amarelas foram observadas. Manchas de coloração
azul foram vistas por Braz (2009) e associada ao ácido cafeico e clorogênico em
cromatogramas para identificação de flavonóides para a tansagem. Para óleos
essenciais, observou zonas amarelas podendo corresponder a piperitona e eugenol
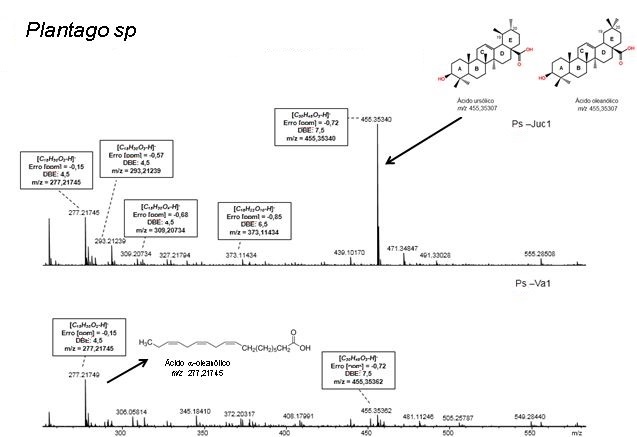
com Rf 0,35 e 0,47. O espectro de massas para a planta de Jucuruaba destacou a
presença do íon [M-H]- 455,35, referente ao triterpeno ácido ursólico ou ácido
oleanólico como também o íon [M-H]- 277,21 correspondendo ao ácido α-linoléico.
Os dois picos também foram observados para a planta de Vargem Alta. Simões et al
(2010) em estudos com P.lanceolata L. demonstraram a influência da variação
sazonal na concentração de catalpol e aucubina nas folhas, propondo meados de
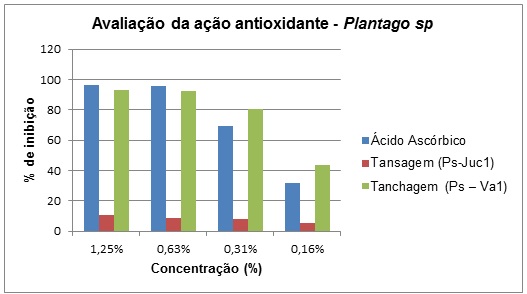
outono como o melhor período para a coleta. Para o teste de DPPH as duas
amostras apresentaram atividade antioxidante, sendo que a amostra de Vargem Alta
apresentou uma atividade bem próxima ao do padrão ácido ascórbico na
concentração de 1,25%. A amostra da tansagem foi menos ativa quando coletada em
Jucuruaba mostrando um poder de inibição quase nove vezes menor que o valor de
referência. O fato de uma atividade antioxidante ser maior em Vargem Alta pode
equivaler ao teor de resíduo seco desta localidade que foi de quase duas vezes
maior que a de Jucuruaba. Fatores ambientais também podem ter influenciado na
produção de compostos fenólicos, tornando a planta coletada em Vargem Alta mais
ativa.
Conclusões
Embora as análises das duas plantas coletadas em diferentes localidades tenham dado resultados bem distintos, as duas apresentaram indícios de compostos fenólicos, triterpenos e ácidos graxos, como também de atividade antioxidante. Essa diferença pode estar correlacionada com sua variabilidade regional, condições de plantio e a época que foi colhido o material.
Agradecimentos
Ao Laboratório de Espectrometria de Massas do Núcleo de Competências em Química do Petróleo. E a Juliana e Patrícia - UFES campus Maruípe.
Referências
BRASIL. Ministério da Saúde. Política Nacional de Plantas Medicinais e Fitoterápicos. Brasília: Ministério da Saúde. 2007.
BRASIL. Farmacopeia Brasileira. Agência Nacional de Vigilância Sanitária –Anvisa. Brasília, 2010. 2 v
BRASIL. Agência Nacional de Vigilância Sanitária. Formulário de Fitoterápicos da Farmacopeia Brasileira. Anvisa: Brasília, 2011, p. 44.
BRAZ, R. Contribuição ao protocolo de controle de qualidade de drogas vegetais. Tese de mestrado em Ciências Farmacêuticas. Universidade Estadual de Maringá, 2009.
COSTA, H. B., SOUZA, L. M., SOPRANI, L. C., OLIVEIRA, B. G., OGAWA, E. M., KORRES, A. M. N., VENTURA, J. A., ROMÃO, W. Monitoring thephysicochemical degradation of coconut water using ESI-FT-ICR MS. Food Chemistry, vol. 174, n. 12014, p. 139-146.
GOBBO-NETO, L., LOPES, N. P. Plantas medicinais: fatores de influência no conteúdo de metabólitos secundários. Química Nova, vol. 30, n. 2, 2007, p. 374-381.
LORENZI, H., MATOS, F. J. A. Plantas medicinais no Brasil – Nativas e exóticas. 2 ed. São Paulo: Instituto Plantarum, 2008. 2 v.
SIMÕES, C.M.O., SCHENKEL, E.P., GOSMANN, G., MELLO, J.C.P., MENTZ, L.A., PETROVIK, P.R. Farmacognosia: da Planta ao Medicamento. Editora UFRGS. Porto Alegre, 2010.
WAGNER, H. BLADT, S. Plant Drug Analysi - A thin Layer Chromatography Atlas. Ed. Springer, 2º edição. Munique, Março de 1996.
































