Reavaliação estrutural e da atividade biológica de morusin, flavonoide isolado de raízes de Morus alba L.
ISBN 978-85-85905-21-7
Área
Produtos Naturais
Autores
Martins, B.A. (UNIVERSIDADE FEDERAL DE MINAS GERAIS) ; Coelho, A.C.S. (UNIVERSIDADE FEDERAL DE MINAS GERAIS) ; Sande, D. (UNIVERSIDADE FEDERAL DE MINAS GERAIS) ; Solares, M.D. (UNIVERSIDAD DE MATANZAS) ; Takahashi, J.A. (UNIVERSIDADE FEDERAL DE MINAS GERAIS)
Resumo
A espécie Morus alba se trata de uma planta com reconhecidas propriedades farmacológicas, mas cuja maioria dos estudos fitoquímicos se restringe às suas folhas e frutos. O trabalho em questão visou a avaliação da presença de substâncias bioativas a partir da cromatografia do extrato de raízes desta espécie. O flavonoide isoprenilado morusin foi isolado, e a sua identificação foi possibilitada através da análise de experimentos de RMN 1D e 2D, em especial do espectro de HMBC, fundamental para a confirmação da estrutura química. A substância foi submetida ao ensaio de capacidade antioxidante de sequestro de radicais ABTS, apresentando EC50 de 172,02 ± 0,91 μg/mL.
Palavras chaves
[i]Morus alba[/i]; morusin; RMN bidimensional
Introdução
Diferentes flavonoides fazem parte da dieta humana. Estes compostos possuem considerável valor nutricional, sendo a classe de produtos naturais que fornece o maior vínculo entre dieta e prevenção de distúrbios crônicos, sendo, por exemplo, muito investigada sua contribuição na prevenção e tratamento de câncer (SAK, 2014). A atividade dos flavonoides é comumente associada à sua efetividade como antioxidantes e eliminadores de radicais livres (ANDERSEN & MARKHAM, 2006). As substâncias antioxidantes são responsáveis pelo retardo de envelhecimento das células humanas, estando presentes em diversas frutas e vegetais (MILANI et al., 2012), assim como podem também estar presentes nas raízes de algumas plantas. Morus alba, conhecida popularmente como amoreira branca, é uma planta originária da Ásia. Diversas propriedades farmacológicas e constituintes fitoquímicos já foram relatados a partir de extratos de diferentes partes desta espécie (SINGH et al., 2013), inclusive uma série de flavonoides que já foram isolados das cascas de suas raízes (NOMURA et al., 1976), demonstrando o potencial da espécie como planta medicinal. O presente trabalho objetiva a avaliação da presença de metabólitos bioativos em extratos de raízes de M. alba e a análise da capacidade antioxidante dos mesmos. Além disso, este trabalho também teve como objetivo utilizar técnicas bidimensionais de ressonância magnética nuclear (RMN) para a identificação inequívoca do flavonoide morusin.
Material e métodos
O extrato etanólico de raízes de uma variedade cubana de Morus alba L. foi submetido à sucessivas separações utilizando colunas cromatográficas em Sephadex LH-20, usando como eluente metanol, e em sílica gel, usando como eluente hexano-acetato de etila [70:30], levando ao isolamento do flavonoide morusin. A elucidação da estrutura química desta substância ocorreu por meio da análise de experimentos de RMN (CDCl3, 400 MHz) unidimensionais (1H, 13C e DEPT) e bidimensionais (COSY, HSQC e HMBC), sendo confirmada a partir de comparação com dados relatados na literatura. Para a avaliação da capacidade antioxidante de sequestro de radicais livres, utilizou-se a análise de ABTS (captura de radicais 2,2-azinobis-[3-etil- benzotiazolin-6-ácido sulfônico]), cuja metodologia foi adaptada de Sande et al. (2016). Esta consistiu na preparação de uma solução de ABTS (ABTS 7mM e persulfato de potássio 2,4 mM incubado por 12 h no escuro), diluída até a absorbância a 734 nm atingir 0,708 ± 0,001. O teste foi realizado em microplacas de 96 poços, em quadruplicada, sendo testadas cinco diferentes concentrações. Em cada poço, cerca de 160 µL da solução de ABTS foi misturada com 40 µL do extrato/padrão ácido ascórbico (100-6,25 μg/mL) e a reação ocorreu por 7 min no escuro, com subsequente leitura da absorbância a 734 nm. Os resultados foram processados por meio do software Excel, e expressos em termos de EC50.
Resultado e discussão
A análise do espectro de RMN 1H permitiu verificar a presença de
três sinais de hidrogênios metílicos na região de deslocamento químico entre
1,4 e 1,7 ppm, consistindo em dois simpletos integrando para 3H cada (1,46 e
1,64 ppm) e um simpleto integrando para 6H (1,45 ppm). Observou-se um
dupleto referente a hidrogênio metilênico em 3,13 ppm integrando para 2H,
além de um tripleto em 5,15 ppm e um dupleto em 5,50 ppm. Na região de
hidrogênios aromáticos, foram visualizados um simpleto em 6,24 ppm, um
multipleto próximo a 6,52 ppm integrando para 2H, região onde suspeitou-se
da ocorrência de uma sobreposição de sinais, e dois dupletos em 6,58 e 7,22
ppm. Observou-se ainda um simpleto em 12,94 ppm, que é recorrente quando a
substância em análise apresenta uma hidroxila quelada em sua estrutura. De
acordo com os valores de deslocamento químico, inferiu-se a presença de
aneis aromáticos substituídos. Dessa forma, poucos átomos de hidrogênio
estão presentes, dificultando uma atribuição confiável dos sinais nos
espectros unidimensionais. As sobreposições de sinais no espectro de RMN de
1H, assim como a possibilidade de constantes de acoplamento
pequenas que influem na multiplicidade prevista para os sinais, levaram a
três possíveis estruturas relatadas na literatura que poderiam corresponder
à substância isolada, sendo estas kuwanon A, kuwanon B (NOMURA et al.
, 1977) e morusin (NOMURA et al., 1976) (Figura 1). A atribuição
dos dados de RMN destas três substâncias é confusa na literatura, sendo que
a atribuição completa e inequívoca dos dados espectrais nem sempre é
relatada. Com o objetivo de confirmar as atribuições de sinais, os espectros
de RMN 2D se mostraram fundamentais. Verificaram-se as correlações carbono-
hidrogênio via HSQC e, através do HMBC, verificaram-se as correlações entre
núcleos de hidrogênio e de carbono que são separados por mais de uma
ligação. As correlações vistas entre os sinais de –CH de aromáticos foram
determinantes para concluir que a substância em questão se tratava de
morusin, uma vez que os sinais correspondentes aos carbonos C-3’, C-5’ e C-
6’ mostra que os mesmos pertencem ao mesmo anel aromático. Estas
correlações, assim como outras fundamentais para a confirmação da estrutura,
podem ser vistas na Figura 2. Morusin trata-se de um flavonoide isoprenilado
isolado das cascas das raízes de Morus alba pela primeira vez por
Nomura e colaboradores (1976). Possui relatada citotoxicidade in
vitro contra algumas células cancerígenas (LI et al., 2015) além
de considerável atividade antioxidante e antibacteriana (MAZIMBA et al.
, 2011).
O ensaio de capacidade antioxidante de sequestro de radicais livres ABTS da
substância isolada indicou uma EC50 de 172,02 ± 0,91 μg/mL. Sendo
baixa a concentração da substância necessária para induzir metade do efeito
máximo analisado, pode-se inferir, com este resultado, o potencial de
morusin como um agente antioxidante.

Possíveis estruturas químicas para a substância isolada.
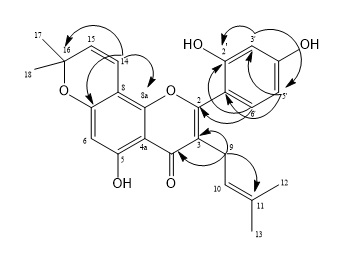
Correções visualizadas no mapa de contornos HMBC para morusin.
Conclusões
O estudo químico do extrato de raízes de Morus alba resultou no isolamento e subsequente identificação estrutural de morusin, por meio da utilização de ressonância magnética nuclear. Esta substância é retratada pela literatura como uma molécula bioativa, sendo de interesse uma caracterização mais detalhada da mesma para atribuição inequívoca, o que foi realizado no presente trabalho. Observou-se ainda o potencial deste flavonoide como agente eliminador de radicais livres.
Agradecimentos
À Universidade Federal de Minas Gerais, ao CNPq e a FAPEMIG, pela concessão de bolsas e financiamento do trabalho.
Referências
ANDERSEN, M. Ø.; MARKHAM, K. R. Flavonoids: chemistry, biochemistry, and applications. CRC Press, New York, 2006.
LI, H.; WANG, Q.; DONG, L.; LIU, C.; SUN, Z.; GAO, L.; WANG, X. Morusin suppresses breast cancer cell growth in vitro and in vivo through C/EBPβ and PPARγ mediated lipoapoptosis. Journal of Experimental and Clinical Cancer Research, v. 34, nº 137, 1-12, 2015.
MAZIMBA, O.; MAJINDA, R. R. T.; MOTLHANKA, D. Antioxidant and antibacterial constituents from Morus nigra. African Journal of Pharmacy and Pharmacology, v. 5, nº 6, 751-754, 2011.
MILANI, L. I. G.; TERRA, N. N.; FRIES, L. L. M.; CICHOSKI, A. J.; REZER, A. P. S.; BACKES, A. M.; PARODIA, C. G. Atividade antioxidante e antimicrobiana in vitro de extratos de caqui (Diospyros kaki L.) cultivar Rama Forte. Brazilian Journal of Food Technology, v. 15, n. 2, p. 118-124, 2012.
NOMURA T.; FUKAI T.; YAMADA S.; KATAYANAGAI M. Phenolic constituents of the cultivated mulberry tree (Morus alba L.). Chemical and Pharmaceutical Bulletin, v. 24, nº 11, 2898-2900, 1976.
NOMURA, T.; FUKAI, T.; KATAYANAGI, M. Kuwanon A, B, C and Oxydihydromorusin, Four New Flavones from the Root Bark of the Cultivated Mulberry Tree (Morus alba L.). Chemical and Pharmaceutical Bulletin, v. 25, nº 3, 529-532, 1977.
SAK, K. Cytotoxicity of dietary flavonoids on different human cancer types. Pharmacognosy Reviews, v. 8, nº 16, 122-146, 2014.
SANDE, D.; SOLARES, M. D.; RODRÍGUEZ, Y. E. M.; CABRERA, I. C.; CARBALLO, L. F.; PÉREZ, N. A.; MORALES, Y. L.; COLEN, G.; TAKAHASHI, J. A. Roots from mulberries (Morus alba) natural and hybrids varieties: phenolic contend and nutraceutical potential as antioxidant. Journal of Applied Pharmaceutical Science, v. 6, n. 11, p. 63-69, 2016.
SINGH, R.; BAGACHI, A.; SEMWAL, A.; BHARADWAJ, S.; BHARADWAJ, A. Tradicional uses, phytochemistry and pharmacology of Morus alba Linn.: A review. Journal of Medicinal Plants Research, v. 7, nº 9, 461-469, 2013.
































