Isolamento de chavibetol e metileugenol do óleo essencial de Pimenta pseudocaryophyllus por cromatografia líquida de alta eficiência
ISBN 978-85-85905-21-7
Área
Produtos Naturais
Autores
Niculau, E.S. (UFT) ; Ribeiro, L.P. (CEPAF/EPAGRIR) ; Ansante, T.F. (USP/ESALQ) ; Fernandes, J.B. (DQ/UFSCAR) ; Silva, M.F.G.F. (DQ/UFSCAR) ; Forim, M.R. (DQ/UFSCAR) ; Vieira, P.C. (DQ/UFSCAR) ; Vendramim, J.D. (USP/ESALQ)
Resumo
A cromatografia líquida de alta eficiência (CLAE) foi utilizada para o isolamento em escala semi-preparativa de chavibetol e metileugenol simultaneamente a partir do óleo essencial bruto das folhas de P. pseudocaryophyllus. A pureza dos compostos isolados e a quantificação foi realizada usando CG-DIC. O Chavibetol foi isolado em alta pureza (98,7%) e recuperação de massa (94,6%). A recuperação para metileugenol foi 86,4% e pureza de 85,3%. Ambos compostos foram identificados por CG-EM e RMN 1H e 13C. Os resultados sugerem que o método pode ser aplicado para isolar chavibetol com alta pureza, recuperação de massa e produtividade a partir do óleo essencial bruto, podendo ser utilizado em bioensaios e bioatividades.
Palavras chaves
Pimenta pseudocaryophyllu; chavibetol; isolamento por CLAE
Introdução
Pimenta pseudocaryophylus (Gomes) L.R. Landrum, popularmente conhecida como “cataia” e craveiro”, é uma mirtácea nativa do Brasil (LANDRUM e KAWASAKI, 1997). Espécies de Pimenta secretam óleos essenciais contendo metabólitos secundários com importantes atividades biológicas relatadas (STEFANELLO et al., 2011), incluindo efeitos contra insetos-praga: como ação inseticida (efeito knockdown), repelência, deterrência de alimentação e oviposição e inibição do desenvolvimento (EBADOLLAHI, 2013). O óleo essencial das folhas de P. pseudocaryophylus (Gomes) L.R. Landrum extraído durante este estudo, mostrou-se conter os fenilpropanóides chavibetol (5-alquil-2- metoxifenol) e metileugenol (4-alquil-1,2-dimetoxibenzeno) como componentes majoritários. Chavibetol e outros fenilpropanóides são relatados como compostos fungicidas (Evans et al., 1984) e antioxidante (RATHEE et al., 2006). Dos Santos et al. (2009) desenvolveram uma metodologia para isolamento do chavibetol a partir do óleo essencial bruto por cromatografia contra- corrente (CCC), porém é necessário utilizar outras metodologias e equipamentos que o isolem em alta pureza, recuperação de massa e produtividade. A cromatografia líquida de alta eficiência (CLAE) é pouco empregada para isolamento de compostos voláteis de óleos essenciais brutos ou fracionados, sendo que pelo nosso conhecimento nunca foi utilizada para isolamento de chavibetol e metileugenol, porém está técnica é extremamente útil para este fim. O objetivo deste trabalho foi isolar chavibetol, em alta pureza, recuperação de massa e produtividade, a partir do óleo essencial bruto de P. pseudocaryophylus utilizando CLAE, bem como caracterizá-lo por CG-EM e RMN 1H e 13C. Metileugenol também foi isolado do óleo essencial bruto.
Material e métodos
Folhas frescas P. pseudocaryophyllus foram individualizadas em amostras de 100 g cada, lavadas em água corrente, cortadas em pequenos pedaços e submetidas ao processo de hidrodestilação utilizando-se um aparelho do tipo Clevenger, por um período de 2 horas à temperatura de 110 °C. A mistura água + óleo obtida (hidrolato) foi separada por decantação e seca por meio da adição de Na2SO4. O óleo essencial (OE) obtido foi armazenado em freezer doméstico (~ -10 oC) até sua utilização. As análises de HPLC e o isolamento foram realizados em um HPLC Shimadzu com uma célula de fluxo analítica ou preparadora de célula de fluxo As condições analíticas foram otimizadas com diferentes proporções de hexano/etanol (10/90%, 70/30% e 92/8%). A cromatografia analítica ótima foi realizada sob condições isocráticas com a fase móvel constituído por hexano:etanol (92: 8) a vazão de 1,0 mL/min usando uma coluna de Phenomenex Luna amino (4,6 mm x 150 mm, 10 μm) e detecção em 230 nm. Os compostos foram isolados por condição semipreparativa no mesmo CLAE com uma coluna Phenomenex Luna amino (10 mm x 250 mm, 10 μm) operando na vazão de 6,0 mL/min na mesma fase móvel e detecção das condições analíticas. O solvente das frações obtidas foi evaporado sob vácuo e a pureza dos compostos isolados foi determinada por CG-DIC e quantificados utilizando este mesmo equipamento por padronização interna. A caracterização foi realizada por CG-EM com base nos índices de retenção, espectros de massas espectros existentes na literatura (ADAMS, 2007) e banco de dados do equipamento (NIST11, WILEY8, NIST05, NIST21 e NIST107). Análises por RMN 1H e 13C também foram realizadas.
Resultado e discussão
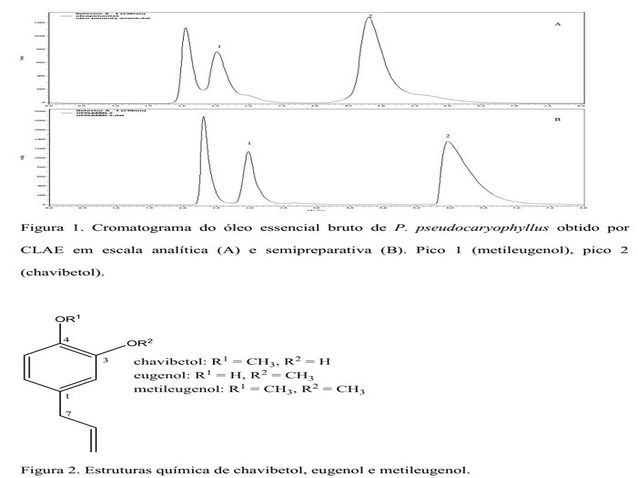
Após análise preliminar por CLAE (cromatograma não mostrado) do padrão
eugenol (Figura 2) foi observado que a banda com tempo de retenção 4,3 min a
partir do O. E no modo analítico (Figura 1A) deveria corresponder ao
chavibetol (CHA), pois por análise preliminar de RMN do óleo essencial (O.
E) notou-se que CHA (Figura 2) é o composto majoritário no mesmo. A partir
da condição analítica ótima foi realizado escalonamento da vazão a ser
utilizada no modo semipreparativo de análise, obtendo-se uma vazão de 6
mL/min em hexano:etanol (92:8%). Em escala semipreparativa, no modo normal
de eluição, foi possível isolar 102,7 mg de CHA (frações representadas pelo
pico 2 com tempo de retenção 6,1 min) e 27,9 mg de metileugenol (ME)
(frações representadas pelo pico 1 com tempo de retenção 3,0 min) (Figura
1B) (Tabela 1) após 11 injeções de 130 uL do O. E bruto de P.
pseudocaryophyllus na concentração de 143 mg/mL. As áreas percentuais
(calculadas pela curva analítica) de CHA e ME no O. E foram de 51,7% e
15,4%, respectivamente. Para o CHA a pureza determinada foi de 98,7% e para
o ME foi de 85,3%. As análises por CG-EM da fração contendo CHA, mostrou o
íon molecular com m/z 164. O índice de retenção calculado, 1367, está de
acordo com os relatados por Dos Santos et al. (2009), 1372, e por Pino et
al. (2006), 1374. A análise por 1H NMR mostrou as informações espectrais
descritas na Tabela 2. Estes dados estão de acordo com os publicados
anteriormente por Dos Santos et al. (2009); Momin et al. (2000) e Meepagala
et al. (2002). O espectro de massas da fração contendo ME, e o tempo de
retenção foram idênticos aos do padrão sigma. O índice de retenção
calculado, 1398, também está de acordo com 1403, relatado por Adams (2007).
Conclusões
A abordagem por CLAE permitiu com sucesso isolar CHA com alta pureza, recuperação e produtividade a partir do O. E bruto. ME também foi obtido a partir das mesmas injeções. A evaporação da fase móvel, por exemplo, hexano e etanol, são mais recomendas por ser mais voláteis que os usados no modo reverso de eluição. O isolamento dos compostos a partir do O. E bruto por CLAE reduz os custos de solventes e materiais, além de diminuir o tempo de análise se comparado aos métodos de isolamento convencional como cromatografia em coluna aberta e cromatografia em camada delgada preparativa.
Agradecimentos
Ao CNPq (INCT 573742/2008-1), FAPESP (INCT, 08/57859-5), CAPES, UFT e ao Programa Novos Pesquisadores da PROPES/UFT pelos auxílios financeiros.
Referências
ADAMS, R. P. Identification of essential oil components by gas chromatography/mass spectroscopy. Allured: Carol Stream, 2007. 804 p.
DOS SANTOS, B. C. B.; DA SILVA, J. C. T.; GUERRERO JR., P. G. et al. Isolation of chavibetol from essential oil of Pimenta pseudocaryophyllusleaf by high-speed counter-current chromatography. Journal of Chromatography A, v. 1216, p. 4303-4306, 2009.
EBADOLLAHI, E. Essential oils isolated from Myrtaceae family as natural insecticides. Annu. Rev. Res. Biol. v. 3, p. 148-175, 2013.
LANDRUM, L. R.; KAWASAKI, M. L. The genera of Myrtaceae in Brazil: an illustrated synoptic treatment and identification keys. Brittonia, v. 49, p. 508-36, 1997.
MEEPAGALA, K. M.; STURTZ, G.; WEDGE, D. E. Antifungal Constituents of the Essential Oil Fraction of Artemisia dracunculus L. Var. dracunculus. J. Agric. Food Chem. v. 50, p. 6989-6992, 2002.
MOMIN, R. A.; RAMSEWAK, R. S.; NAIR, M. G. Bioactive Compounds and 1,3-Di[(cis)-9-octadecenoyl]-2-[(cis,cis)-9,12-octadecadienoyl]glycerol from Apium Graveolens L. Seeds. J. Agric. Food Chem. v. 48, 3785-3788, 2000.
PINO, J. A.; MARBOT, R.; MARTÍN, M. P. Chemical Composition of the Essential Oil of Helenium amarum (Raf.) H. Rock from Cuba. J. Essent. Oil Res. v. 18, p. 438-439, 2006.
RATHEE, J. S.; PATRO, B. S.; MULA, S. et al. Antioxidant Activity of Piper betel Leaf Extract and Its Constituents. J. Agric. Food Chem. v. 54, p. 9046-9054, 2006.
STEFANELLO, M. E. A.; PASCOAL, A. C. R. F.; SALVADOR, M.J. Essential oils from Neotropical Myrtaceae: chemical diversity and biological properties. Chem. Biodiv. v. 8, p. 73-94, 2011.
































