Análise de cádmio em amostras reais sem utilização de cianeto: uma proposta para as aulas práticas de Química Analítica Qualitativa
ISBN 978-85-85905-21-7
Área
Ensino de Química
Autores
Pais, A.R. (UNIVERSIDADE FEDERAL DO TRIÂNGULO MINEIRO - UFTM) ; Alves, V.A. (UNIVERSIDADE FEDERAL DO TRIÂNGULO MINEIRO - UFTM)
Resumo
O presente trabalho tem como objetivo propor um procedimento experimental para determinação de cádmio em amostras reais, sem necessidade de utilizar cianeto. As bijuterias adquiridas foram classificadas como ligas à base de cobre ou de ferro. Quatro tipos de bijuterias foram classificadas como contendo cobre; a partir disso o cobre foi removido por eletrogravimetria e realizados testes qualitativos para identificação de cádmio. A remoção do cobre foi de suma importância para a análise qualitativa de cádmio, e também foi de grande utilidade para eliminação do uso do cianeto para mascarar a interferência do cobre; sabe-se que cianeto em meio ácido libera gás cianídrico. Esse trabalho pode ser útil para as aulas práticas de Química Analítica Qualitativa e Intrumental, em nível de graduação.
Palavras chaves
análise qualitativa; cádmio; cianeto
Introdução
A análise qualitativa de cádmio nos livros texto de Química Analítica Qualitativa (MUELLER; SOUZA, 2010; VOGEL, 2001) é baseada em procedimentos experimentais que utilizam sais de cianeto, uma substância altamente tóxica, principalmente nessa análise, em que o meio deve estar fortemente ácido, havendo formação de ácido cianídrico. As reações químicas envolvidas nesse teste qualitativo são dadas a seguir (VOGEL, 1981): 1) Cd2+(aq) + 2CN-(aq) ➝ Cd(CN)2(s), 2) Cd(CN)2(s) + 2CN-(aq) ➝ [Cd(CN)4]2-(aq) e 3) [Cd(CN)4]2- (aq) + Na2S(aq) ➝ CdS(s) + 2Na+(aq) + 4CN-(aq). O presente trabalho tem como objetivo propor um procedimento para a análise qualitativa de cádmio em amostras reais, onde não se utiliza sal de cianeto. Ao realizar a análise usando o procedimento da literatura, observou-se no caso de amostras que contêm alto teor de cádmio, que mesmo após a adição de um excesso de solução de KCN não ocorria a descoloração do meio reacional, que se encontrava predominantemente azul. Dessa forma, como o cobre é um potencial interferente, definiu-se proceder à remoção do cobre antes da realização do ensaio qualitativo para cádmio, utilizando a análise eletrogravimétrica. Aproveitou-se essa análise para quantificar o teor de cobre nas bijuterias. Esse procedimento poderá ser realizado durante as aulas práticas de Química Analítica Qualitativa em nível de graduação, onde a amostra utilizada pode ser encontrada no cotidiano dos estudantes, o que configura uma vantagem, já que pode incrementar o interesse dos mesmos no tocante à participação na aula. Além disso, esse procedimento agrega o uso de uma técnica analítica instrumental, a eletrogravimentria, que muitas vezes é vista pelos estudantes somente na parte teórica da disciplina Química Analítica Instrumental.
Material e métodos
A fim de se executar o presente trabalho, as seguintes etapas foram realizadas: aquisição de bijuterias oriundas da China; classificação da bijuteria adquirida quanto ao tipo de liga (ferrosa ou de cobre) (MUELLER; SOUZA, 2010); preparo das amostras das bijuterias; realização da eletrogravimetria para remoção de cobre e sua quantificação; e realização de ensaios químicos para identificação de cádmio. Para a limpeza das peças utilizou-se hexano, conforme recomendado pela literatura (MUELLER; SOUZA, 2010). As peças foram imersas em hexano, contido em um béquer, o qual foi levado para um banho de ultrasom, durante 5 min. Após limpeza foram deixadas para secar naturalmente. Foram realizados dois procedimentos para a identificação das ligas, um para as ligas à base de ferro e outro para ligas à base de cobre. Foram realizados testes qualitativos para identificar a presença de cádmio nas bijuterias classificadas como sendo baseadas em cobre. Segundo a literatura, apenas as ligas à base de cobre poderiam apresentar cádmio na sua composição química. Para a identificação do cádmio, o agente precipitante utilizado foi o íon sulfeto, que precipita o cádmio em meio ácido, na forma de sulfeto de cádmio, um sólido amarelo. Os potenciais interferentes nessa análise são o cobre, o cobalto, o níquel e o mercúrio (MUELLER; SOUZA, 2010). A identificação do cádmio na amostra, onde previamente havia sido realizada a remoção de cobre por eletrogravimetria, foi feita adicionando-se, gota a gota, uma solução de Na2S 30% (m/V) a 0,5 mL da solução contendo a amostra. A solução foi aquecida em banho maria, por alguns minutos, agitando constantemente; em caso de presença de cádmio ocorreu o aparecimento de um precipitado de cor amarela, confirmando a sua presença na amostra (MUELLER; SOUZA, 2010).
Resultado e discussão
As bijuterias foram classificadas quanto ao tipo de liga; os resultados
obtidos são apresentados na Tabela 1. Das 9 peças analisadas, 4 possuem
cobre na sua composição química e 5 são ferrosas. Os testes qualitativos
para a identificação de Cd só foram realizados nas amostras contendo Cu.
Segundo Muller, 2010, o cádmio possivelmente seria encontrado em pequenas
proporções ou até como elemento-traço apenas nas ligas contendo cobre. Após
a classificação das ligas, realizou-se os testes qualitativos para as ligas
contendo cobre na sua composição química (lembrando que o cobre, por ser
interferente, foi removido da solução contendo a amostra via
eletrogravimetria). Dessa forma, realizou-se a análise qualitativa para as
peças: 01-00, 04-00, 07-00 e 09-00. Os resultados dos testes qualitativos
são mostrados nas Fig. 1. A peça 09-00 apresentou a formação de um
precipitado amarelo intenso, indicando um resultado positivo para cádmio. A
Fig. 2 mostra os ensaios qualitativos para amostras da peça 09-00. Na foto
inferior, é mostrado que a adição direta de sulfeto de sódio à solução da
amostra, sem adição prévia de cianeto de potássio ou realização de análise
eletrogravimétrica para a remoção de cobre, resulta na formação de um
precipitado marrom (de CuS), que intefere na visualização do precipitado
amarelo intenso de CdS, por meio da adição de sulfeto de sódio.
Interessantemente, no tubo da direita, a adição de sulfeto de sódio foi
realizada sem a adição prévia de cianeto na solução, pois todo o cobre, o
principal interferente nessa análise, foi removido por eletrogravimetria,
gerando uma intensa coloração amarela (de CdS), indicando um teste positivo
para cádmio (sem necessidade do uso de cianeto de potássio!). A %Cu nas
amostras das peças analisadas é dada na Tabela 2.
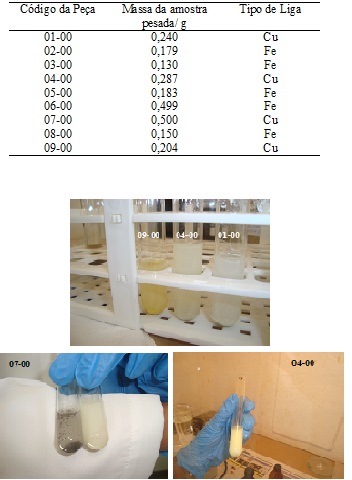
Tabela 1. Classificação das ligas. Figura 1.Testes qualitativos para Cd, após remoção do Cu. Exceto no tubo da esquerda, foto inferior esquerda.

Tabela 2. Porcentagem de cobre nas peças, por eletrogravimetria. Figura 2. Testes qualitativos para identificação de cádmio, para a peça 09-00.
Conclusões
Conseguimos aperfeiçoar a análise qualitativa do cádmio, no que tange a interferência do cobre. Isso foi feito utilizando a análise eletrogravimétrica para a remoção completa do cobre da solução da amostra. Essa etapa eliminou a necessidade do uso da solução de cianeto de potássio à solução ácida da amostra, antes da adição de sulfeto de sódio. Nessas condições (em meio ácido), pode haver geração de HCN, visto que o íon cianeto, a base conjugada de um ácido fraco, trata-se de uma base fraca, sofrendo hidrólise em solução aquosa, gerando o HCN, que é muito tóxico se inalado.
Agradecimentos
Curso e Depto. de Química/ICENE/UFTM. Rede Mineira de Química (RQ-MG)/FAPEMIG (Projetos: REDE-113/10; CEX - RED-00010-14).
Referências
MUELLER, H; SOUZA, D.; Química Analítica Qualitativa Clássica, Edifurb: Blumenau, 2010.
VOGEL, A. I. Química Analítica Qualitativa [tradução Antonio Gimeno; revisão G. Svehla], Mestre Jou: São Paulo, 1981.
































