Adsorção de Cobre(II), em solução aquosa, utilizando o Jatobá-do-cerrado (Hymenaea stigonocarpa) in natura como material adsorvente
ISBN 978-85-85905-21-7
Área
Físico-Química
Autores
Sales, C.S. (UEG) ; Signini, R. (UEG) ; Araújo, C.S.T. (UEG)
Resumo
Ações antrópicas tem levado a contaminação das águas, principalmente o que se refere ao lançamento de efluentes e tais como, agrotóxicos contendo metais tóxicos.Neste sentido, estudos envolvendo adsorção têm sido realizados apresentando-se como uma técnica viável.Entre eles a utilização de adsorventes naturais, no caso das cascas do Jatobá-do-cerrado (Hymenaea stigonocarpa) in natura.Estudos de adsorção foram realizados e construídas as isotermas de adsorção segundo os modelos de Freundlich e Langmüir.Foi possível determinar a Capacidade Máxima de Adsorção (CMA) no valor de 12,8 mg/g o fator de equilíbrio (RL) de 0,20, mostrou-se uma adsorção favorável.A isoterma que melhor se ajustou aos resultados experimentais foi a Freundlich, sugerindo que o processo ocorre em multicamadas.
Palavras chaves
Adsorção; Jatobá-do-cerrado; cobre(II)
Introdução
O crescimento industrial e o rápido desenvolvimento tecnológico têm sido uma das fontes potenciais de poluição ambiental. Efluentes industriais contêm alto teor de diversos íons de metais tóxicos, na sua maioria despejados em córregos, rios, mares sem nenhum tratamento prévio (AHMARUZZAMAN, 2011). O cobre (II) é um metal essencial à vida e a saúde humana, porém, mesmo em baixas concentrações é prejudicial aos seres vivos. É um metal largamente utilizado como: componente chave de várias enzimas responsáveis pela catalise de reações de oxidação-redução, micronutrientes na agricultura, fios condutores de eletricidade, galvanoplastia e outros. O Jatobá-do- cerrado (Hymenaea stigonocarpa) é fruto da família Leguminosae, espécie característica do bioma cerrado (DEFAVARI et al, 2009). Métodos convencionais tais como: troca iônica, oxidação-redução, precipitação química, filtração por membrana, floculação, osmose reversa e adsorção, são aplicados na remoção de metais tóxicos em águas (MISHRA; BALOMAJUMDER; AGARWAL, 2012). Tecnologias alternativas para remediação de ambientes aquosos contaminados com íons metálicos, que apresentam baixo custo operacional e alta eficiência. Neste contexto, a adsorção têm apresentado vantagens em relação aos métodos convencionais, devido à flexibilidade na operação, utilização de materiais de baixo custo e por ser uma técnica eficaz na remoção de metais (JIMÉNEZ-CEDILLO et al., 2013. Desta forma, materiais naturais com capacidade de remoção através da adsorção têm sido investigados na busca da remoção destes íons metálicos (MARQUES et al., 2012; SENTHILKUMAR et al., 2011). O presente trabalho avaliou a adsorção de íons de cobre(II) em cascas e polpas trituradas do Jatobá-do-cerrado (Hymenaea stigonocarpa) in natura.
Material e métodos
Os frutos do Jatobá-do-cerrado (Hymenaea stigonocarpa) foram obtidos em árvores no entorno da cidade de Anápolis-GO. As cascas foram separadas da polpa, lavadas, secas em estufa com circulação de ar a uma temperatura de 35ºC durante 24 h e trituradas em moinho de facas. A granulometria foi definida a uma faixa de 115 a 110 mesh com o uso de peneiras Tyler, o material foi acondicionado em frascos de polietileno à temperatura ambiente. Para a construção das isotermas de adsorção dos íons de cobre(II) em águas, foram utilizadas 250 mg Jatobá-do-cerrado (Hymenaea stigonocarpa) in natura (JIN). Em seguida foi adicionado 25 mL de solução de cobre(II) em concentrações variando de 20 mg/L a 100 mg/L, e o pH do sistema foi ajustado em 5,5. O sistema permaneceu sob agitação por 36h. Em seguida, a solução foi filtrada e o sobrenadante diluído 10 vezes, para análise no Espectrômetro de Absorção Atômica com chama (FAAS) AAnalyst 400 da Perkim Elmer, a fim de obter-se a quantidade de metal adsorvido. O comprimento de onda utilizado foi 324,75 cm-1. O experimento foi realizado em triplicata.
Resultado e discussão
Na Tabela 1 são mostrados os parâmetros obtidos no equilibrio, das isotermas
lineares de Langmüir e Freundlich para o processo de adsorção dos íons
cobre(II) em Jatobá in natura (JIN).
A Capacidade Máxima de Adsorção (CMA) observada para os íons cobre(II), foi
de 12,8 mg/g. O resultado mostra que o adsorvente apresenta afinidade com
os íons de cobre(II). A literatura reporta trabalhos para a adsorção de
íons cobre(II) em águas como: Senthilkumar e colaboradores(2011) utilizando
casca de castanha de caju como adsorvente, obteve um valor de qmáx igual a
20,0 mg g-1; Gorgievski e colaboradores (2013) utilizando palha de trigo,
obteve um valor igual a 4,30 mg/g. Observa-se que o valor de qmáx obtido
neste trabalho encontra-se coerente quando comparado com a literatura e
mostra-se que o adsorvente utilizando apresenta eficiência na adsorção de
íons cobre(II) em águas. O valor de RL obtido no processo de adsorção dos
íons de cobre(II) em JIN foi menor que 1 e maior que zero, indicando que o
processo de adsorção é favorável (ONG et al., 2009). O valor n encontrado
neste trabalho para a adsorção de íons de cobre(II) foi maior que 1,
sugerindo que o processo é físico, e favorável a uma concentração elevada,
mas desfavorável em concentrações menores (AL-DEGS et al., 2006; CRINI et
al., 2007).
Mediante o valor do coeficiente linear (R2), obtido a partir das isotermas
de adsorção para os íons cobre(II), o modelo que melhor se ajustou aos dados
foi o de Freundlich, sugerindo que o processo de adsorção ocorre em
multicamadas.
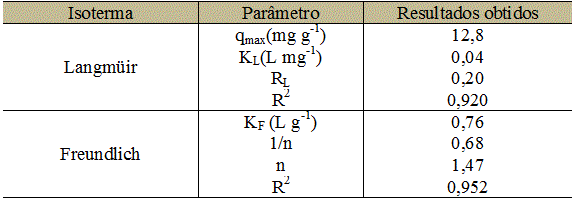
Parâmetros de Langmüir e Freundlich para a adsorção dos íons cobre(II) em águas e (JIN) como adsorvente.
Conclusões
De acordo com o valor da CMA, evidenciou que o material possui afinidade em adsorver os íons cobre (II). A partir do parâmetro n de Freundlich e o parâmetro de equilíbrio (RL) sugere que o processo de adsorção é favorável. O modelo de isoterma que melhor ajustou aos dados experimentais foi o de Freundlich, indicando que o processo de adsorção ocorre em multicamadas. Os resultados sugerem que o Jatobá-do-cerrado (Hymenaea stigonocarpa) possui capacidade em adsorver íons de cobre(II) em águas.
Agradecimentos
A CAPES pela bolsa concedida; Ao Programa de Concessão de Bolsa de Incentivo ao Pesquisador (BIP) instituído pela Lei Estadual n. 18.332/2013.
Referências
AHMARUZZAMAN, M. Industrial wastes as low-cost potential adsorbents for the treatment of wastewater laden with heavy metals. Advances in Colloid and Interface Science, v. 166, n. 1–2, p. 36–59, 2011.
AL-DEGS, Y. S.; EL-BARGHOUTHI, M. I.; ISSA, A. A.; KHRAISHEH, M. A.; WALKER, G. M. Sorption of Zn(II), Pb(II), and Co(II) using natural sorbents: Equilibrium and kinetic studies. Water Research, v. 40, n. 14, p. 2645–2658, 2006.
CRINI, G.; PEINDY, H. N.; GIMBERT, F.; ROBERT, C. Removal of C.I. Basic Green 4 (Malachite Green) from aqueous solutions by adsorption using cyclodextrin-based adsorbent: Kinetic and equilibrium studies. Separation and Purification Technology, v. 53, n. 1, p. 97–110, 2007.
DEFAVARI, G. R.; TARAZI, R.; MORENO, M. A.; FERRAZ, E. M.; GANDARA, F. B.; KAGEYAMA, P. Y. Estrutura genética espacial intrapopulacional de Hymenaea stigonocarpa Mart. ExHayne na Estação Ecológica de Itirapina, SP. Sci. For., Piracicaba, v. 37, p. 089-098, 2009.
JIMÉNEZ-CEDILLO, M. J.; OLGUÍN, M. T.; FALL, C.; COLIN-CRUZ, A. As ( III ) and As ( V ) sorption on iron-modi fi ed non-pyrolyzed and pyrolyzed biomass from Petroselinum crispum ( parsley ). Journal of Environmental Management, v. 117, p. 242–252, 2013.
MARQUES, T. L.; ALVES, V. N.; COELHO, L. M.; COELHO, N. M. M. Removal of Ni(II) from aqueous solution using Moringa oleifera seeds as a bioadsorbent. Water Science & Technology, v. 65, n. 8, p. 1435, mar. 2012.
MISHRA, V.; BALOMAJUMDER, C.; AGARWAL, V. K. Kinetics , Mechanistic and Thermodynamics of Zn ( II ) Ion Sorption : A Modeling Approach. CLEAR-Soil Air Water, v. 40, n. 7, p. 718–727, 2012.
ONG, S.-T.; TAY, E. H.; HA, S.-T.; LEE, W. N.; KENG, P.-S. Equilibrium and continuous flow studies on the sorption of Congo Red using ethylenediammine modified rice hulls. International Journal of Physical Sciences, v. 4, n. 11, p. 683–690, 2009.
SENTHILKUMAR, P.; RAMALINGAM, S.; SATHYASELVABALA, V.; KIRUPHA, S. D.; SIVANESAN, S. Removal of copper(II) ions from aqueous solution by adsorption using cashew nut shell. Desalination, v. 266, n. 1–3, p. 63–71, jan. 2011.
































