SÍNTESE DOS PEPTÍDEOS D E L- FENILSEPTINA PARA ESTUDOS DE INTERAÇÃO PEPTÍDEO-MEMBRANA E DE CITOTOXICIDADE EM CÉLULAS CANCERÍGENAS
ISBN 978-85-85905-21-7
Área
Bioquímica e Biotecnologia
Autores
Ferreira, C.S. (UFVJM) ; Araujo, P.R.Q. (UFMG) ; Rodrigues, A.L.P. (FUMEC) ; Cruz, J.S. (UFMG) ; Magalhães, M.T.Q. (UFMG) ; Munhoz, V.H.O. (UFVJM) ; Santos, T.L. (UFVJM) ; Verly, R.M. (UFVJM)
Resumo
O modo de ação de peptídeos antimicrobianos em grande parte ocorre através da interação com a membrana bacteriana, porém ainda não é totalmente definido. Dessa forma, faz-se necessários estudos da interação peptídeo-membrana com meios biomiméticos. Neste trabalho foram sintetizados e caracterizados dois peptídeos antimicrobianos, o D-fenilseptina e L-fenilseptina, para estudos da interação peptídeo-membrana por ITC e ensaios de citotoxicidade celular. Os resultados revelaram uma maior interação com meios miméticos de fosfotidilcolina de membrana do D-Phes quando comparado ao L-Phes, explicando assim a maior citotoxicidade apresentado por D-Phes em relação ao L-Phes frente a células de câncer de mama altamente metastático (MDA-MB-231).
Palavras chaves
Calorimetria; Citotoxidade; Peptídeo
Introdução
As fenilseptinas são peptídeos antimicrobianos isolados de Hypsiboas punctatus, uma espécie de anuro encontrada na América do Sul, constituídos por 17 resíduos de aminoácidos (FFFDTLKNLAGKVIGALT) diferenciando-se apenas na estereoquímica dos resíduos de Phe-2. As Phes possuem atividade contra bactérias Gram-positivas e Gram-negativas, porém ainda há muito a investigar sobre o espectro de atividade e o mecanismo de ação desses peptídeos (MAGALHÃES, 2011; MUNHOZ, 2012). Modelos atuais apontam para mecanismos que que envolvem a interação seguida da perturbação da membrana bacteriana. Alguns modelos enunciam que o modo de interação de peptídeos antimicrobianos depende de uma combinação de efeitos hidrofóbicos e eletrostáticos (Sanderson, 2005). Os peptídeos carregados positivamente, por exemplo, sofrem mudanças em suas conformações e adotam uma estrutura anfipática quando são atraídos pela superfície aniônica das membranas bacterianas (Bechinger, 2004). Entretanto, o modo de interação pode ser específico para diferentes moléculas de peptídeos (Bechinger, 1999; Shai, 2002; Bechinger e Lohner, 2006) e, portanto, é extremamente relevante a ampliação dos conhecimentos sobre o modo de interação peptídeo-membrana. Para isto, é comum a preparação de meios biomiméticos de composições químicas variáveis, porém compatíveis com os da célula alvo para estudos biofísicos das interações com peptídeos (VERLY et al., 2009). A calorimetria de titulação isotérmica (ITC) constitui-se em uma excelente técnica para caracterizar interações em solução, visto que é possível obter o perfil termodinâmico completo destas interações, mesmo sendo interações de afinidades baixas (Seelig, 1997; White et al., 1998). Visto que os processos químicos, físicos e bioquímicos ocorrem por absorção ou liberação de calor, essa técnica vem sendo muito utilizada para analisar, dentre outras coisas, a afinidade entre peptídeo e lipídeo para auxiliar na compreensão da atividade biológica e modo de interação com membranas, fornecendo em um único experimento a descrição termodinâmica da interação (∆G, ∆H, ∆S, constante de interação K e coeficiente estequiométrico n). A descrição termodinâmica é de extrema importância para a avaliação da atividade antimicrobiana dos peptídeos, visto que essa atividade está diretamente ligada à interação do peptídeo com a membrana bacteriana. Diante disso, esse trabalho traz o estudo da interação peptídeo-membrana dos estereoisômeros da fenilseptina, a D-Phes e L-Phes com meios biomiméticos vesiculares de fosfotidilcolina (POPC), utilizando como principal ferramenta de análise a calorimetria de titulação isotérmica (ITC). Esta técnica constitui-se como uma excelente ferramenta para caracterizar interações em solução, visto que é possível obter a descrição termodinâmica completa do sistema em análise, mesmo para interações de afinidades baixas (Seelig, 1997; White et al., 1998). Além disso, também é explorado neste trabalho a avaliação da citotoxicidade de D-Phes e L-Phes frente a células de câncer de mama altamente metastático (MDA-MB-231) e, dessa forma, propor uma relação estrutura-atividade desses peptídeos.
Material e métodos
Os peptídeos D-Phes e L-Phes foram obtidos pela síntese em fase sólida, via estratégia Fmoc (fluorenilmetiloxicarbonil), utilizando-se resina rink-amide (grau de substituição 0,79 mmol/g). Como ativadores foram utilizados, para cada acoplamento, 1-hidroxibenzotriazol (HOBt) anidro e N,N- diisopropilcarbodiimida (DIC). Ambos os peptídeos foram clivados empregando- se solução de 95,0% de ácido trifluoroacético (TFA), 2,5% de água deionizada (grau Milli-Q) e 2,5% de triisopropilsilano (TIS) seguindo o protocolo padrão de clivagem da estratégia de síntese Fmoc (Chan, 2000). A purificação dos peptídeos foi realizada por Cromatografia Líquida de Alta Eficiência (CLAE) em fase reversa empregando-se coluna Waters® C18 (7,8 x 300 mm). A caracterização foi realizada por espectrometria de massa (MALDI-ToF) em equipamento AutoFlex III na Universidade Federal de Minas Gerais. Como meio biomimético, foi preparada uma solução de vesículas de POPC (1-palmitoil-2- oleoil-fosfatidilcolina) em tampão Tris-HCl (20 mM) pH 8,5, contendo 100 mM de NaCl. As análises de ITC foram realizadas em microcalorímetro VP-ITC da Malvern®, a 25ºC no Laboratório de Síntese e Estrutura de Biomléculas (LASEB) da Universidade Federal dos Vales do Jequitinhonha e Mucuri. Os experimentos foram realizados pela titulação de solução 20 mM de vesículas de POPC em 24 micromolar de peptídeo. Os ensaois de citotoxicidade celular com MTT foram realizados com diferentes linhagens celulares cultivadas em meio de cultura DMEM suplementado com 10% de soro bovino fetal e 5% de antibiótico (com um tempo de attachment de 24 h). Após o tempo de exposição aos peptídeos, foi solução de MTT (5mg/ml) e a viabilidade celular (%) foi calculada a partir da absorvância medida em 540nm segundo a relação: viabilidade celular (%) = [A540 (amostra) / A540 (controle)] × 100.
Resultado e discussão
As amostras das sínteses dos peptídeos D-Phes e L-Phes foram analisadas por
CLAE e por espectrometria de massas MALDI-ToF. As figuras 1 mostram os
ionogramas obtidos por EM-MALDI-ToF das amostras brutas da síntese, onde
pode-se observar os íons [M+H]+, correspondendo ao L-Phes e ao D-Phes,
comprovando o sucesso das sínteses. Após a purificação das amostras, foram
realizados os ensaios de citotoxicidade e estudos termodinâmicos da
interação do peptídeo com membranas fosfolipídicas.
Os resultados de citotoxicidade em células de câncer de mama metastático,
mostram que a viabilidade celular não se altera ao longo do tempo de
incubação, ou seja, a ação dos peptídeos na membrana celular ocorre de forma
rápida (24 horas) não sendo potencializada pelo tempo de exposição aos
peptídeos. Outro fator observado foi que o efeito citotóxico de D-Phe é
maior do que (64- 128 µg/mL) do que o encontrado para L-Phes (128 - 256
µg/mL).
As Figura 2 apresenta isoterma de interação peptídeo-membrana envolvendo
solução de PC-LUVs (20 mmol.L-1) e soluções de D-Phes e L-Phes. Cada ponto
das isotermas corresponde ao calor envolvido na interação após adição de 5
μL de PC-LUVs à solução de L-Phes e D-Phes. A partir do ajuste das isotermas
foram extraídos os parâmetros termodinâmicos da interação peptídeo-membrana.
Os dados revelam maior interação do D-Phes (Kapp = 2340 M-1) com as PC-LUVs
quando comparado com a interação da L-Phes (Kapp = 1520 M-1), além de uma
maior estequiometria para o sistema fosfolipídio/D-Phes. Esta maior
interação pode estar relacionada a orientação das cadeias laterais das
fenilalaninas (F-1, F-2 e F-3) na D-Phes, estabilizada por interações pi dos
anéis fenílicos, permitindo maior inserção da região N-terminal da cadeias
peptídica da D-Phe na interface das membranas (Magalhães et al, 2013, Munhoz
2012).
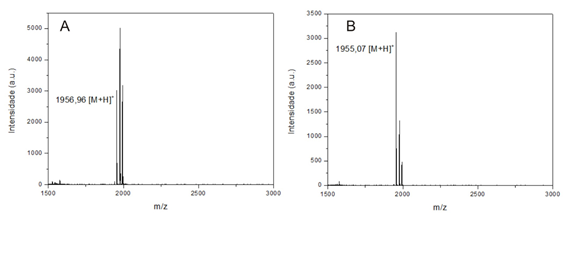
Ionogramas obtidos por EM-MALDI-ToF das amostras brutas da síntese de D-Phes (A) e L-Phes (B).
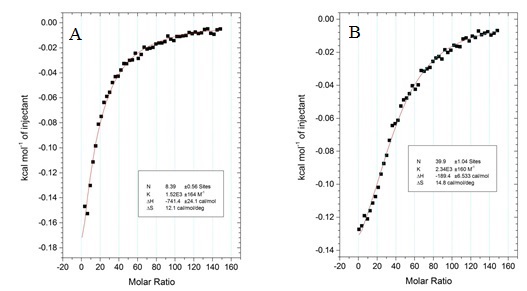
Isotermas de interação peptídeo-membrana de solução de PC-LUVs em soluções de L-Phes (A) e D- Phes (B).
Conclusões
Os estudos termodinâmicos, empregados para avaliar a interação dos peptídeos com meios biomiméticos de membrana, mostraram que as interações de L-Phes e D- Phes são predominantemente exotérmica. Contudo, D-Phes interage mais fortemente com as PC-LUVs do que o L-Phes, explicado em parte pela maior inserção do D-Phes na interface das membranas. Consequentemente, essa maior interação implica em uma maior perturbação da bicamada fosfolipídica, resultando também em uma maior citotoxicidade do D-Phes em comparação com o L- Phes frente às células de câncer de mama metastático.
Agradecimentos
CAPES, CNPQ, FAPEMIG e Rede Mineira de Química.
Referências
MAGALHÃES, M. T. Q. (2011). "Caracterização estrutural e funcional de Fenilseptinas: Peptídeos com atividade antimicrobiana e químico sensorial presentes na secreção cutânea de Hypsiboas punctatus". Tese (Doutorado em Biologia Molecular) – Instituto de Ciências Biológicas, Universidade de Brasília, Brasília.
MUNHOZ, V. H.O. (2012). "Análise Estrutural e Topológica de Peptídeos Bioativos em Meios Biomiméticos de Membranas". 183 f. Tese (Doutorado em Ciências – Química) – Instituto de Ciências Exatas, Universidade Federal de Minas Gerais, Belo Horizonte.
Sanderson, J. M. (2005)."Peptide–lipid interactions: insights and perspectives". Organic & Biomolecular Chemistry, v.3, n.2, p.201-212.
Bechinger, B. (2004)."Structure and function of membrane-lytic peptides". Critical Reviews in Plant Sciences, v.23, n.3, p.271-292.
Vogt, T. C. B. e Bechinger, B. (1999)."The interactions of histidine-containing amphipathic helical peptide antibiotics with lipid bilayers. The effects of charges and pH". Journal of Biological Chemistry, v.274, n.41, p.29115-29121.
Shai, Y. (2002)."Mode of action of membrane active antimicrobial peptides".
Biopolymers, v.66, n.4, p.236-248.
Bechinger, B. e Lohner, K. (2006)."Detergent-like actions of linear amphipathic cationic antimicrobial peptides". Biochimica et Biophysica Acta (BBA) - Biomembranes, v.1758, n.9, p.1529-1539.
Gallo, R.L., Murakami, M., Ohtake, T. e Zaiou, M. (2002). Biology and clinical relevance of naturally accuring antimicrobial peptides. Mol Mechan Inall and Clin Immunol, pages 823-831.
VERLY, R. M., (2010), "Peptídeos Antimicrobianos: Síntese, Ensaios
Biológicos, Estudos Termodinâmicos e Análise Estrutural por RMN em Meios Biomiméticos". Tese (Doutorado em Ciências-Química) - Instituto de Ciências Exatas, Universidade Federal de Minas Gerais, Belo Horizonte, MG.
Seelig, J. 1997. "Titration calorimetry of lipid-peptide interactions. Biochim. Biophys". Acta. 1331:103–116.
Mariana T. Q. de Magalhães, Eder A. Barbosa, Maura V. Prates, Rodrigo M. Verly, Victor Hugo O. Munhoz, Ivan E. de Araújo, Carlos Bloch Jr. (2012). "Conformational and Functional Effects Induced by D- and L-Amino Acid Epimerization on a Single Gene Encoded Peptide from the Skin Secretion of Hypsiboas punctatus". PLOS ONE, v.8, n 4, p. e59255.
































