CULTIVO DE [i]L. rhamnosus[/i] INCQS 00006 UTILIZANDO PERMEADO DE SORO E GLICEROL RESIDUAL COMO FONTES DE CARBONO ALTERNATIVAS PARA PRODUÇÃO DE ÁCIDO LÁTICO
ISBN 978-85-85905-21-7
Área
Bioquímica e Biotecnologia
Autores
Mattos, M.V.C.V. (UNIVERSIDADE FEDERAL DO RIO GRANDE) ; Munhoz, A.P. (UNIVERSIDADE FEDERAL DO RIO GRANDE) ; Trindade, R.A. (UNIVERSIDADE FEDERAL DO RIO GRANDE) ; Gautério, F.G.A. (UNIVERSIDADE FEDERAL DO PAMPA - CAMPUS BAGÉ) ; Burkert, C.A.V. (UNIVERSIDADE FEDERAL DO RIO GRANDE)
Resumo
O objetivo do presente trabalho foi avaliar os coprodutos agroindustriais permeado de soro e glicerol residual como fontes de carbono no cultivo de Lactobacillus rhamnosus INCQS 00006 para produção de ácido lático. Nos cultivos, foi utilizado o caldo MRS sem modificações (glicose como fonte de carbono) e com modificações, substituindo a glicose por glicerol residual ou permeado do soro, sendo retiradas alíquotas ao longo do tempo para determinações do pH e biomassa, sendo o ácido lático determinado ao final do cultivo. Os resultados mostraram que o permeado de soro possui grande potencial para substituição da glicose no meio de cultivo para produção de ácido lático, obtendo-se 19,59 g/L para o permeado e 20,50 g/L para a glicose.
Palavras chaves
Ácido lático; Lactobacilos; Coproduto agroindustrial
Introdução
Bactérias láticas são consideradas micro-organismos fastidiosos, requerendo nutrientes complexos para seu crescimento, tais como vitaminas do complexo B, minerais específicos e diversos aminoácidos (GUILHERME; PINTO; RODRIGUES, 2009; STANIER et al., 1986). O meio de cultivo Man, Rogosa e Sharp (MRS) tem sido frequentemente utilizado no preparo do inóculo destas bactérias (BERNARDO et al., 2016; LIMA; COELHO; CONTIERO, 2010), por ser um meio bastante completo, contendo os nutrientes necessários para o crescimento destes micro-organismos. Pelo fato destas bactérias serem reconhecidas como produtoras de ácido lático, diversos estudos têm abordado a substituição da glicose, presente no meio MRS, por coprodutos agroindustriais, como o melaço (OLIVEIRA et al., 2009), o soro de leite (BERNARDO et al., 2016) e o glicerol oriundo do biodiesel (RIVALDI et al., 2013). A utilização destes coprodutos em processos biotecnológicos possui vantagens significativas em relação aos custos do processo (CAPELLARI, 2010). Um dos grandes problemas enfrentados pelo setor industrial diz respeito ao destino a ser dado aos coprodutos gerados no processo, pois quando indevidamente tratados geram problemas ambientais. Sendo assim, a utilização do glicerol residual e permeado de soro é uma ótima alternativa para minimizar os danos de um possível descarte inadequado, além de diminuir os custos do processo. Com este intuito, o presente trabalho propõe a substituição da glicose, que é a fonte de carbono usual, pelo permeado de soro e glicerol residual no cultivo de Lactobacillus rhamnosus INCQS 00006, visando produzir ácido lático.
Material e métodos
A bactéria L. rhamnosus INCQS 00006 foi reativada a 37ºC em meio MRS (Man, Rogosa e Sharpe). Para o preparo do inóculo, a cultura microbiana foi raspada com 10 mL de água peptonada 0,1%, transferindo para Erlenmeyer de 500 mL contendo 90 mL de caldo MRS, incubada a 37ºC até atingir a densidade ótica 1,0. Os cultivos foram realizados em frascos Erlenmeyer de 500 mL contendo 200 mL de meio, inoculados com suspensão da bactéria em estudo (10%). Os frascos foram mantidos em incubadora refrigerada (Tecnal TE-424) a 37ºC, sem agitação, retirando-se alíquotas em tempos pré-determinados, sendo estas centrifugadas sob refrigeração para as determinações analíticas no sobrenadante (pH e ácido lático) e sedimento (biomassa). Nos cultivos, foi utilizado o caldo MRS sem modificações (glicose como fonte de carbono) e com modificações, substituindo a glicose por glicerol residual e permeado do soro na mesma concentração. O pH do sobrenadante foi medido diretamente em medidor de pH (Marte MB-10, Brasil) (AOAC, 2000). A biomassa foi monitorada pela absorbância a 600 nm do sedimento (PRIETO et al. 2008). Para determinação de acido lático às amostras foi adicionada acetona PA (1:3 v/v), para remoção de proteínas, sendo centrifugadas a 10.000 × g por 15 min, a acetona foi evaporada e as amostras devidamente diluídas, filtradas em membrana hidrofílica de 0,22 µm e transferidas para vials. O ácido lático foi quantificado por cromatografia líquida (Shimadzu, Japão), utilizando uma coluna Aminex HPX - 87H (300 x 7,8 mm) (Bio-Rad, EUA), de acordo com Oliveira, Buzato e Hauly (2005). Os dados obtidos foram submetidos à analise de variância e teste de Tukey, a fim de verificar a existência de diferenças significativas entre as fontes de carbono, a 95% de confiança.
Resultado e discussão
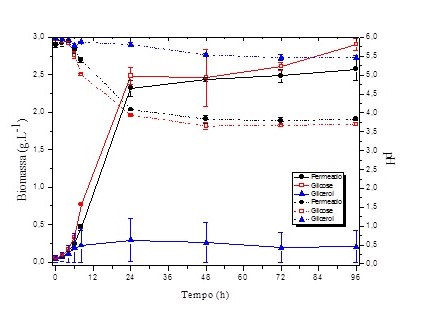
Ao observar-se a Figura 1 pode-se perceber que a bactéria foi capaz de
crescer no meio à base de permeado de soro, entretanto, quando o glicerol
residual foi a fonte de carbono utilizada o crescimento não foi
satisfatório. Os maiores valores de concentração de biomassa foram
encontrados em 96 h de cultivo utilizando glicose e permeado de soro, sendo
estes de 2,90 (± 0,08) e 2,58 (± 0,15) g/L, respectivamente, não
apresentando diferença significativa. Lavari et al. (2015) encontraram para
L. rhamnosus 64 uma concentração máxima de biomassa de 1,3 g/L ao
utilizar permeado de soro como fonte de carbono.O pH para permeado de soro,
inicialmente de 5,80 passou para 3,84, enquanto que para glicose de 5,95
para 3,70 e para o glicerol de 5,95 para 5,47, portanto o pHapresentou um
decréscimo mais acentuado quando a glicose e o permeado de soro foram
utilizados como fonte de carbono, e ao utilizar o glicerol residual o pH
manteve-se praticamente constante, indicando uma baixa atividade metabólica
do micro-organismo com esta fonte de carbono. De acordo com Dakin e Radwell
(1971), Lactobacillus possuem a capacidade de fermentar hexoses e
pentoses em ácido lático, o que explicaria a queda de pH nos meios compostos
por glicose e lactose. A concentração de ácido lático no cultivo com
permeado de soro foi de 19,59 (± 0,65) g/L, já no cultivo contendo glicose
foi de 20,50 (± 1,2) g/L, não havendo diferenças significativas (p>0,05).
Zhang e Vadlani (2015) encontraram para L. plantarum 24,3 g/L de AL
utilizando o meio MRS modificado, sendo usado como fonte de carbono 25,5 g/L
de uma mistura de glicose e xilose (3:1), sendo a glicose completamente
consumida em 24 h de cultivo, resultado semelhante aos encontrados no
presente trabalho.
Conclusões
O glicerol residual não tem potencial para utilização no cultivo do microrganismo estudado. No entanto, permeado de soro mostrou-se como uma fonte de carbono alternativa à glicose e promissora para cultivo da bactéria para produção de ácido lático.
Agradecimentos
Os autores agradecem FAPERGS, CNPq e CAPES pelo apoio financeiro.
Referências
AOAC, Official Methods of Analysis (17th edn). Washington: Association of Official Analytical Chemists, 2000. CD-ROM.
BERNARDO, M. P.; COELHO, L. F.; SASS, D. C.; CONTIERO, J. L-(+)-lactic acid production by Lactobacillus rhamnosus B103 from dairy industry waste. Brazilian Journal of Microbiology, v. 47, n. 3, p. 640–646, 2016.
CAPELLARI, J. Biossíntese de ácido lático por Lactobacillus amylovorus a partir de resíduos agroindustriais. 70 f. Dissertação (Mestrado em Engenharia de Processos), Universidade da Região de Joinville, Joinville, 2010.
DAKIN, J. C.; RADWELL, J. Y. Lactobacilli causing spoilage of acetic acid preserves. Journal of Applied Bacteriology, v.34, p. 541-545, 1971.
GUILHERME, A. A., PINTO, G. A. S.; RODRIGUES, S. Avaliação da produção de ácido lático por Leuconostoc mesenteroides B512 F em xarope de caju. Ciência e Tecnologia de Alimentos, v. 29, p. 738-747, 2009.
LIMA, C. J. B.; COELHO, L. F.; CONTIERO, J. The use of response surface methodology in optimization of lactic acid production: focus on medium, supplementation, temperature and pH control. Food Technology and Biotechnology, v.48, n. 2, p. 175-181, 2010.
OLIVEIRA, A. R.; BUZATO, J. B.; HAULY, M. C. O. Produção contínua de ácido láctico por Lactobacillus curvatus a partir de melaço de cana-de-açúcar suplementado. Semina: Ciências Agrárias, v. 26, n. 1, p. 53-60, 2005.
OLIVEIRA, R. F.; SOUSDALEFF, M.; LIMA, M. V. S.; LIMA, H. O. S. Produção fermentativa de ácido lático a partir do melaço da cana-de-açúcar por Lactobacillus casei. Brazilian Journal of Food Technology, VII BMCFB, p. 34-40, 2009.
PRIETO, L. M.; MICHELON, M.; BURKERT, J. F. M.; KALIL, S. J.; BURKERT, C. A. V. The production of rhamnolipid by a Pseudomonas aeruginosa strain isolated from a southern coastal zone in Brazil. Chemosphere, v. 71, p. 1781-1785, 2008.
RIVALDI, J. D.; SILVA, M. L. C. S.; DUARTE, L. C.; FERREIRA, A. E. N.; CORDEIRO, C.; FELIPE, M. G. A.; FREIRE, A. P.; MANCILHA, I. M. Metabolism of biodiesel derived glycerol in probiotic Lactobacillus strains. Applied Microbiology and Biotechnology, v. 97, p. 1735-1743, 2013.
STANIER, R.Y.; INGRAHAM, J.L.; WHEELIS, J.L.; PAINTER, P.R. General microbiology. 5th ed. London, England: Macmillan Education, 1986.
































